2. 深圳市宝安区福永人民医院重症医学科, 深圳 518103
梗阻性休克仅占所有休克患者的2%,临床相对少见。左室流出道动态梗阻(dynamic left ventricular outflow tract obstruction, DLVOTO)导致休克,是由于心脏形态异常或功能异常而诱发梗阻,表现为左心室流出道与主动脉峰值压力阶差(left ventricular outflow tract gradient, LVOTG) > 25 mmHg(1 mm Hg=0.133 kPa)。心脏超声是诊断DLVOTO的最重要工具,以龙虾爪征为典型表现而诊断DLVOTO的报道少见。现对深圳大学附属第二医院重症医学科两例典型龙虾爪征诊断DLVOTO患者进行回顾分析,以加强临床医师对其认识。
1 病例资料病例1,患者女性,86岁,因“反复腹痛1年余,再发2 d,呕吐后气促4 h”于2018年2月4日收入本院。入科查体:体温36.5℃,脉搏90次/min,呼吸45次/min,血压120/90 mmHg;外周动脉氧饱和度83%,吸入氧体积分数(FiO2)40%。神志意识模糊,被动体位,急性病面容,查体不能配合。气促明显,双肺呼吸音粗,可闻及痰鸣及少量干性啰音。心界不大,心率90次/min,心音低顿,心律齐,各瓣膜听诊区未闻及病理性杂音。腹平,腹肌软,全腹无明显压痛、反跳痛,墨菲征可疑阳性。双下肢废用性萎缩,肌力检查无法配合。既往有胆囊结石并胆囊炎、高血压病、冠心病、癫痫、脑梗后遗症、老年痴呆病史。
2018年2月3日外院动脉血气pH值7.43,二氧化碳分压43 mmHg,动脉氧分压72 mmHg(FiO2 35%),动脉血氧饱和度95%,血乳酸2.4 mmol/L。本院肺部CT提示双肺散在分布斑片状、云絮状渗出病灶,考虑肺部感染;腹部CT提示胆囊结石并急性胆囊炎、胆总管扩张,胆总管下段疑似结石影。
考虑患者误吸导致肺部感染,予以气管插管机械通气;纤支镜见左、右支气管内可见中等量黄色脓痰。完善血培养、痰培养等相关检查;经验性应用头孢哌酮舒巴坦抗感染。
入科后患者肌钙蛋白由0.4 ng/mL升至3.9 ng/mL;氨基末端脑钠肽前体(N terminal pro‐B type natriuretic peptide, NT-ProBNP) > 5 000 pg/mL。2月4日心脏超声提示:左心室肥厚(室间隔13 mm,左心室后壁13 mm),左心室收缩功能正常,左心室射血分数58%,舒张功能降低。心电图提示胸前导联ST-T改变。留置脉波指示连续心排血量监测,心输出量3.2 L/min,每搏量26 mL/次,全心舒张末期容积指数946 mL/m2,全身血管阻力指数4 398 dyn/s/cm5/m2。结合病史,考虑患者脓毒症导致脓毒性心肌病可能性大。2月4日尝试多巴酚丁胺[2 μg/(kg·min)]强心治疗,心率升至130次/min后,动脉血压降至66/44 mmHg;心脏超声提示典型龙虾爪征,左室流出道峰流速达4.4 m/s(图 1)。予以停用多巴酚丁胺后,患者心率降至108次/min,血压恢复至130/69 mmHg。患者抗感染、液体负平衡,复查肌钙蛋白、NT-ProBNP持续下降至正常。2月22日床旁经皮气管切开,并脱离呼吸机。3月1日出院,居家继续康复、护理。随访未再发明显血压波动。
|
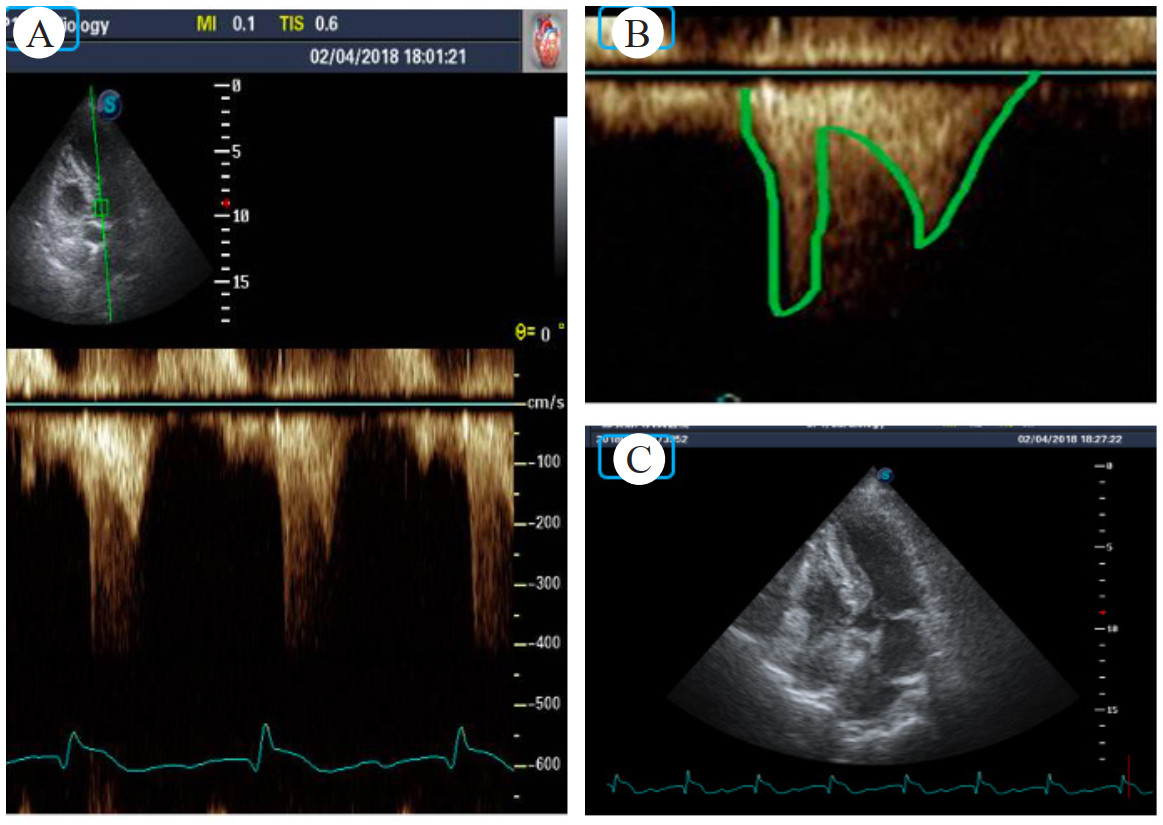
| A、B: 心脏超声左室流出道呈龙虾爪征; C: 二尖瓣前叶收缩期前移 图 1 病例1的超声检查结果 |
|
|
病例2,患者男性,68岁,因“左侧肢体无力伴肌肉萎缩9个月,呼吸困难1 d”于2019年1月16日收入本院神经内科。患者于9个月前外院肌电图提示神经源性损害,拟诊“运动神经元病”,并逐渐出现左侧肢体肌肉萎缩,左手掌萎缩明显,左手无力加重。近1 d患者无明显诱因出现呼吸困难,无明显发热、咳嗽、咳痰等。既往有高血压病、颈椎病、反流性食管炎病史。
入院后患者神志呈昏睡状,查动脉血气pH值7.16,二氧化碳分压123 mmHg,动脉氧分压238 mmHg(FiO2 35%),碳酸氢根43.8 mmol/L,动脉血氧饱和度98%,血乳酸0.7 mmol/L。考虑患者二氧化碳潴留,肺性脑病,请本科气管插管,呼吸机辅助呼吸,留置深静脉后转入ICU。
转入情况:体温不升,呼吸25次/min,心率117次/min,血压65/32 mmHg[去甲肾上腺素1 μg/(kg·min)]。外周动脉血氧饱和度97%,FiO2 65%。神志呈昏睡状。经口气管插管,呼吸机辅助呼吸。心肺腹查体无明显异常。
患者入科后监测二氧化碳逐渐下降,患者逐渐清醒。但持续低血压,需要大剂量[2.5μg/(kg·min)]去甲肾上腺素维持血压。而且血压波动极大,观察血压降低与患者心率增快明显相关,心率91次/min,有创动脉血压155/100 mmHg;心率升至107次/min,有创动脉血压下降至87/66 mmHg。
留置脉波指示连续心排血量监测,提示患者心率与心输出量呈反比。患者心率93次/min,每搏量40 mL/次,心输出量3.7 L/min,全身血管阻力指数2 949 dyn/s/cm5/m2,全心舒张末期容积指数1 110 mL/m2。心率升至103次/min,每搏量22 mL/次,心输出量2.3 L/分,全身血管阻力指数5 943 dyn/s/cm5/m2,全心舒张末期容积指数973 mL/m2。患者家属提供病史患者激动后容易晕厥,考虑不能排除左室流出道动态梗阻。行多巴酚丁胺负荷试验,静推2 mg多巴酚丁胺后心率升至155次/min,血压由145/65 mmHg降至65/32 mmHg,左室流出道峰流速由1 m/s增快至约3 m/s,收缩期二尖瓣前叶前移,有典型龙虾爪表现(图 2),符合流出道动态梗阻导致梗阻性休克,加用右美托咪定后患者心率缓慢降至92次/min,血压回升至155/75 mmHg;加用美托洛尔47.5 mg qd、依法布雷定2.5 mg qd鼻饲控制心室率,患者血压稳定并停用去甲肾上腺素;监测左室流出道峰流速波动在1.3~1.4 m/s(图 3)。
|
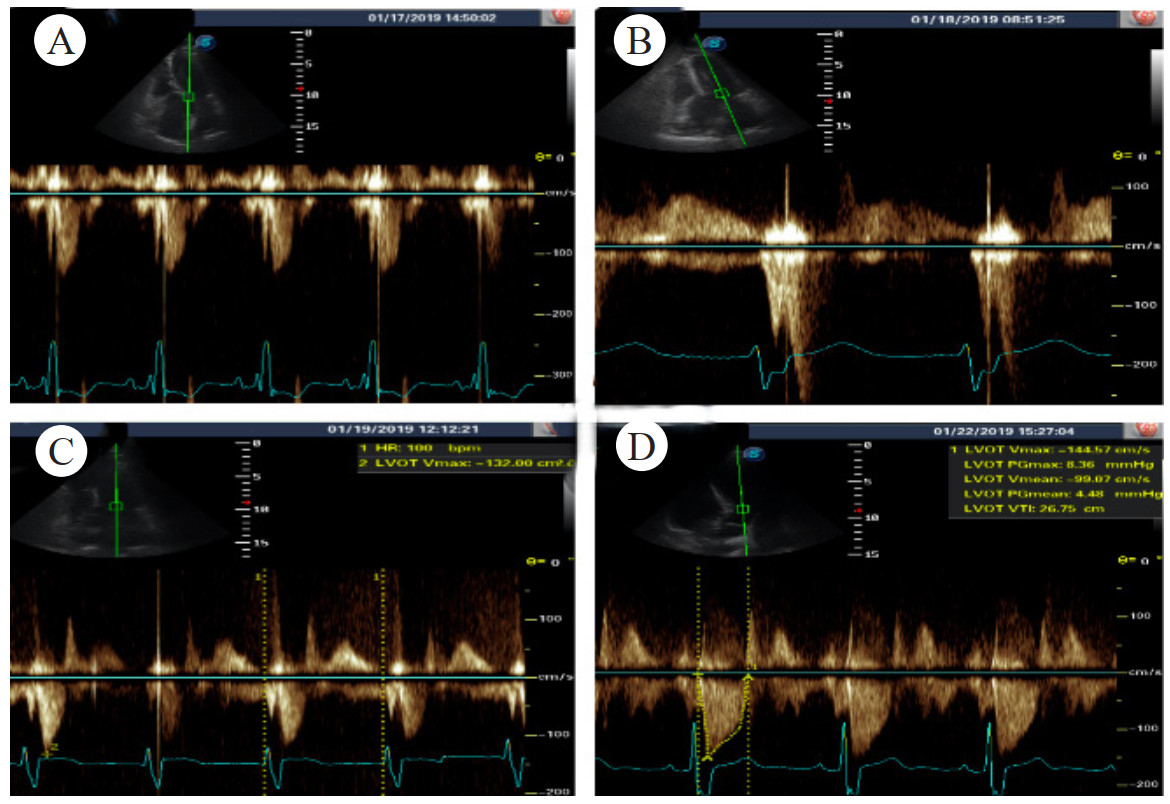
| A: 1月17日左室流出道峰流速约1.1 m/s; B: 1月18日多巴酚丁胺后左室流出道峰流速约3 m/s; C、D: 1月19和22日左室流出道峰流速分别1.3 m/s、1.4 m/s 图 2 病例2心脏超声左室流出道峰流速变化 |
|
|
|
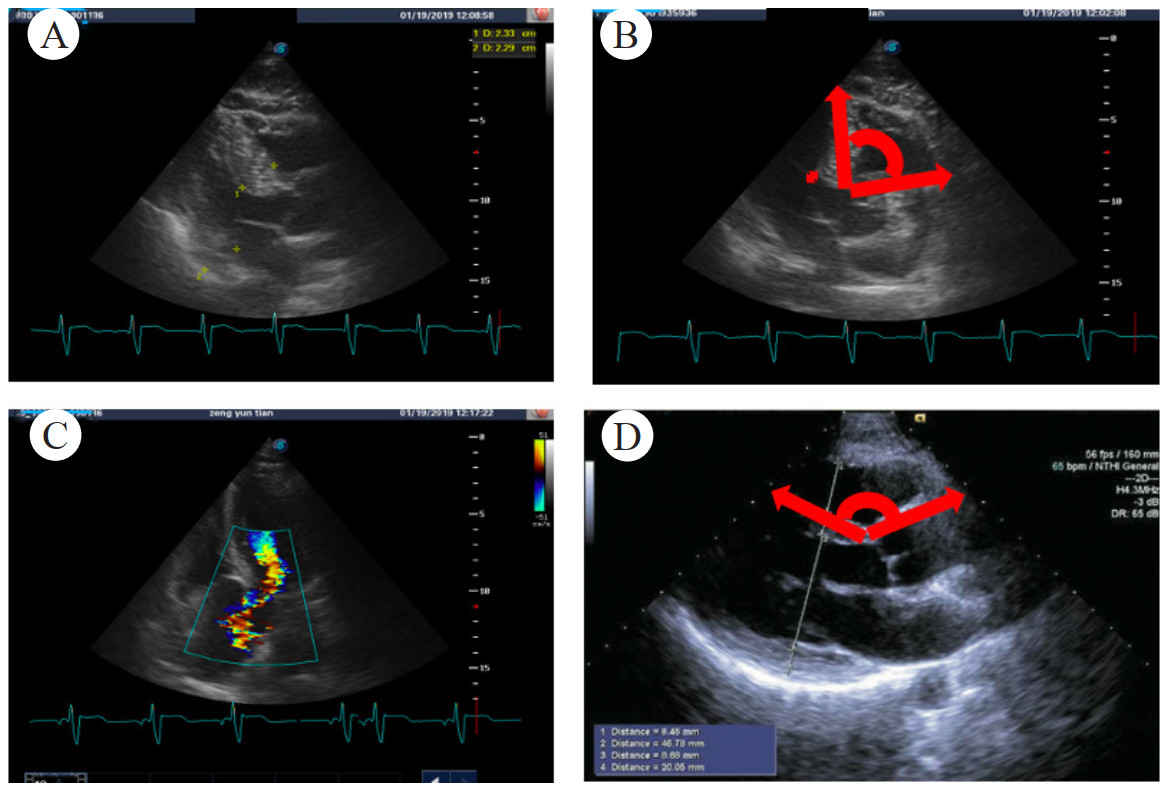
| A: 胸骨旁长轴左心室明显增厚; B: 胸骨旁长轴室间隔和升主动脉夹角; C: 心尖4腔心左室流出道血流速增快; D: 正常患者室间隔和升主动脉夹角 图 3 病例2的超声检查结果 |
|
|
患者1月28日行气管切开,2月12日转至普通病房,并于6月25日出院,随访长期鼻饲美托洛尔,血压稳定。
2 讨论梗阻性休克仅占所有休克患者的2%[1];但其产生的血流动力学改变最为急剧,危害也最大,需要快速明确梗阻的部位并解除梗阻[2]。
广义的左室流出道(Left ventricular outflow tract,LVOT)包括主动脉瓣下、主动脉瓣、主动脉瓣上3个部位,而狭义的LVOT一般指的是主动脉瓣环水平至二尖瓣前叶或腱索的这段范围[3]。DLVOTO定义为左心室流出道与主动脉峰值压力阶差(left ventricular outflow tract gradient,LVOTG) > 25mmHg [4];也称为动力性梗阻,在肥厚性心肌病也称为隐匿性梗阻[5],或动态收缩功能不全[6];即LVOTG安静时正常,负荷运动时≥30 mmHg。因此DLVOTO诊断标准不一,本文中2例患者按照简化伯努利公式,LVOTG分别为64 mmHg和25 mmHg;但两例患者明确有血压下降,心输出量下降,因此DLVOTO诊断明确。
DLVOTO可由于心脏形态异常(左心室肥厚、S型室间隔、二尖瓣前叶过长、乳头肌突出),或功能异常(低血容量、低后负荷、心脏高动力、儿茶酚胺)诱发[7]。既往研究发现,73例左室流出道梗阻患者(LVOTG > 50 mmHg)中梗阻性肥厚性心肌病是最常见病因(占74%);其他包括高血压左心室肥厚9%,开胸术后7%,S型室间隔4%,左心室高动力3%,应激性心肌病1.5%,主动脉瓣下隔膜1.5%[8]。脓毒性休克患者由于液体大量渗漏,加上各种刺激导致心肌收缩增强,约有1.9%患者合并严重DLVOTO,LVOTG 78(56~123)mmHg,包括收缩期二尖瓣前叶前移(systolic anteriormitral valve motion, SAM)、严重二尖瓣反流和肺水肿[7]。大量输血和促凝血治疗导致二尖瓣血栓形成也可导致DLVOTO[9]。
DLVOTO发病主要机制有两种:(1)二尖瓣部分装置收缩期向左室流出道移位;(2)左室心肌收缩力随药物、运动、心脏前后负荷的改变而改变,其梗阻程度是不固定的[3]。因此DLVOTO常合并SAM征,继而导致二尖瓣反流,从而诱发血流动力学不稳定[4]。研究证实DLOVTO患者91%有SAM征,61%患者为严重SAM,即室间隔与二尖瓣前叶或键索接触,如图 3病例2情况。44%患者有中度以上二尖瓣反流[8]。86%患者表现为左心室较小[左心室舒张末内径(41±6)mm,收缩末内径(24±5)mm];还有左心室不对称性肥厚[室间隔(16±4)mm,左心室后壁(12±3)mm];左心房轻度扩大[左心房内径(42±9)mm;左心房面积指数(24±6)cm2/m2];以及左心室高动力[左心室射血分数(74±9)%]等表现[8]。本文中两例患者均有SAM征,无二尖瓣反流;病例1基底部室间隔为13 mm,左室后壁13 mm;病例2底部室间隔为12 mm,左室后壁11 mm。而且两例患者左心室高动力表现(左心室射血分数分别为58%和72%),均在使用多巴酚丁胺后诱发DLVOTO。而超声科报告中提示患者左心室收缩功能正常,常误导诊断。
心脏超声是DLVOTO诊断首选方法[4],室间隔基底部厚度和“SAM”征可能是决定DLVOTO程度的重要解剖特征[3]。龙虾爪征表现为多普勒频谱射血流速收缩中期凹陷。收缩早期,左心室流出道无梗阻,峰流速持续上升。由于收缩期二尖瓣前叶前移和室间隔接触,升高的压差导致左心室流出道变窄,反之进一步加大压差。二尖瓣和室间隔接触在连续多普勒表现为转折点。如果梗阻非常严重,左心室射血流速可能下降大于50%,在脉冲多普勒表现为第一次峰流速下降(收缩中期凹陷),此时达到压差最大值。左心室面对突然增高的后负荷不能维持射血,导致其长轴收缩短暂停止,主动脉瓣叶关闭。当压差降低后左心室再次射血,表现为峰流速再次升高,最终表现为龙虾爪征。当压差 > 60 mmHg,脉冲多普勒在左室流出道表现为龙虾爪征[10]。
DLVOTO超声表现需要和主动脉瓣狭窄、二尖瓣反流、高动力左心室等鉴别。主动脉狭窄为全收缩期固定狭窄,连续多普勒表现为射血峰值位于收缩早中期,且加速度近乎不变。当LVOT流速 > 5.0~5.5 m/s需怀疑是否合并二尖瓣反流,二尖瓣反流图形呈钟形对称。高动力左心室排空,连续多普勒表现为非对称性,下降支较慢,上升支较快[10]。本文两例患者有SAM征,龙虾爪征等典型表现,容易与上述鉴别。
此外还需注意基底部室间隔肥厚,主要在既往有高血压病史老年人,心脏超声表现为单纯S型室间隔肥厚(基底部室间隔≥14 mm,基底部/中部室间隔≥1.3)。由于左心室和升主动脉夹角增大(图 3),有可能诱发动态梗阻性基底部室间隔肥厚;表现为(1)劳累后呼吸困难,接近晕厥和胸部不适等左室流出道梗阻表现;(2)运动后LVOTG > 30 mmHg;(3)经β受体阻滞剂或其他负性肌力药物治疗后症状改善[11]。本文两位都有高血压病史的老年患者,因此考虑长期高血压导致左心室和升主动脉夹角增大是患者本次发病诱因之一(图 3)。
左心室流出道与主动脉之间的LVOTG是动态变化的,受各种改变心肌收缩力和负荷因素(如脱水、饮酒、饱食、运动、体位、用药等)的影响,运动负荷或药物激发(亚硝酸异戊酯、多巴酚丁胺、异丙肾上腺素)试验和Valsalva试验,以排除DLVOTO[5]。多巴酚丁胺负荷超声心动图可监测左心室流出道血流速度和压力阶差。在42例患者行多巴酚丁胺负荷超声心动图,14例患者左心室流出道血流速度明显增快,且14例患者均有左心室肥厚,其中不对称性以室间隔基底部肥厚10例,对称性肥厚者4例。相关分析显示,室间隔厚度与负荷后左心室流出道血流速度呈显著相关性,以室间隔基底肥厚更为显著(r=0.61,P < 0.001)[12]。本文中两例患者患者均使用多巴酚丁胺,超声提示LVOTG明显升高,伴有血压明显下降,经停用多巴酚丁胺后血压恢复。因此检查时及恢复过程中应密切观注患者的症状、血压、心率、LVOTG的变化以及有无新发的心律失常等情况[5]。
DLVOTO治疗目前无指南推荐,可参考肥厚性心肌病和应激性心肌病指南[5, 13]。DLVOTO患者予强心药会增加左心室基底部心肌收缩力,利尿剂导致容量不足,两者都可增加LVOTG而恶化血流动力学,导致急性心衰和心源性休克[4]。应激性心肌病指南建议合并LVOTO患者避免利尿、硝酸酯类和主动脉球囊反博治疗,可考虑静脉补液(无心衰患者),短效β受体阻滞剂和左心室辅助[13]。在肥厚性心肌病有左心室流出道梗阻的患者,我国指南推荐一线治疗方案为无血管扩张作用的β受体阻滞剂(剂量可加至最大耐受剂量),以改善症状[5]。本文例1患者停用多巴酚丁胺,例2患者给予美托洛尔后均未再出现血压波动;而例1患者有脓毒性休克,未加用β受体阻滞剂。但在脓毒性休克合并DLVOTO患者中,艾司洛尔可作为挽救性治疗措施[14]。
肥厚性心肌病指南推荐,梗阻性肥厚性心肌病患者急性低血压时,采用多巴胺、多巴酚丁胺、去甲肾上腺素和其他静脉应用的正性肌力药可能有害(Ⅲ,B);对液体输入无反应,推荐静脉用苯肾上腺素(或其他单纯血管收缩剂)(Ⅰ,B)[5]。因此在顽固性休克患者中及时诊断DLVOTO,避免正性肌力药物非常重要。
DLVOTO可由于心脏形态异常或功能异常而诱发,尤其在有基础心脏形态改变患者,有导致心脏前后负荷降低、心肌收缩力增强等诱因,需要注意筛查。心脏超声可及时发现LVOTG和频谱改变,龙虾爪征、SAM征等是DLVOTO重要表现。
利益冲突 所有作者声明无利益冲突
| [1] | Vincent JL, De Backer D. Circulatory shock[J]. N Engl J Med, 2013, 369(18): 1726-1734. DOI:10.1056/NEJMra1208943 |
| [2] | 管向东, 司向. 休克定义及分型的再思考[J]. 协和医学杂志, 2019, 10(5): 438-441. DOI:10.3969/j.issn.1674-9081.2019.05.002 |
| [3] | 鄢磊, 阮琴韵, 屈朝阳, 等. 超声心动图对左心室流出道梗阻解剖形态与血流动力学特征的分析[J]. 中华超声影像学杂志, 2016, 25(10): 844-847. DOI:10.3760/cma.j.issn.1004-4477.2016.10.006 |
| [4] | Citro R, Okura H, Ghadri JR, et al. Multimodality imaging in takotsubo syndrome: a joint consensus document of the European Association of Cardiovascular Imaging (EACVI) and the Japanese Society of Echocardiography (JSE)[J]. J Echocardiogr, 2020, 18(4): 199-224. DOI:10.1007/s12574-020-00480-y |
| [5] | 中华医学会心血管病学分会中国成人肥厚型心肌病诊断与治疗指南编写组, 中华心血管病杂志编辑委员会. 中国成人肥厚型心肌病诊断与治疗指南[J]. 中华心血管病杂志, 2017, 45(12): 1015-1032. DOI:10.3760/cma.j.issn.0253-3758.2017.12.005 |
| [6] | Ormerod JOM, Frenneaux MP, Sherrid MV. Myocardial energy depletion and dynamic systolic dysfunction in hypertrophic cardiomyopathy[J]. Nat Rev Cardiol, 2016, 13(11): 677-687. DOI:10.1038/nrcardio.2016.98 |
| [7] | Balik M, Novotny A, Suk D, et al. Vasopressin in patients with septic shock and dynamic left ventricular outflow tract obstruction[J]. Cardiovasc Drugs Ther, 2020, 34(5): 685-688. DOI:10.1007/s10557-020-06998-8 |
| [8] | Kobayashi S, Sakai Y, Taguchi I, et al. Causes of an increased pressure gradient through the left ventricular outflow tract: a West Coast experience[J]. J Echocardiogr, 2018, 16(1): 34-41. DOI:10.1007/s12574-017-0352-6 |
| [9] | Skrypnikov V, Rosenthal C, Weber-Carstens S, et al. Dynamic thromboembolic left ventricular outflow tract obstruction after aggressive procoagulant treatment in hemorrhagic shock: a case report[J]. J Med Case Rep, 2021, 15(1): 269. DOI:10.1186/s13256-021-02840-3 |
| [10] | Sen-Chowdhry S, Jacoby D, Moon JC, et al. Update on hypertrophic cardiomyopathy and a guide to the guidelines[J]. Nat Rev Cardiol, 2016, 13(11): 651-675. DOI:10.1038/nrcardio.2016.140 |
| [11] | Pearson AC. The evolution of basal septal hypertrophy: from benign and age-related normal variant to potentially obstructive and symptomatic cardiomyopathy[J]. Echocardiography, 2017, 34(7): 1062-1072. DOI:10.1111/echo.13588 |
| [12] | 葛均波, 徐永健, 王辰. 内科学[M]. 第9版. 北京: 人民卫生出版社, 2018: 167. |
| [13] | Ghadri JR, Wittstein IS, Prasad A, et al. International expert consensus document on takotsubo syndrome (part II): diagnostic workup, outcome, and management[J]. Eur Heart J, 2018, 39(22): 2047-2062. DOI:10.1093/eurheartj/ehy077 |
| [14] | Pablo CR, David AO, Carlos V, et al. Beta blockers as salvage treatment in refractory septic shock complicated with dynamic left ventricular outflow tract obstruction: a rare case presentation[J]. J Investig Med High Impact Case Rep, 2021, 9: 23247096211056491. DOI:10.1177/23247096211056491 |
 2024, Vol. 33
2024, Vol. 33