肺移植是治疗终末期肺部疾病的有效手段,近年来全球肺移植数量呈稳步增长态势,受者短期生存率显著提升。但受者病情逐渐复杂,手术及术前术后管理难度增大,一旦出现的严重心肺功能障碍等并发症,将直接影响患者预后[1]。
ECMO在肺移植围术期起重要作用。对于术前心肺功能严重障碍且无法通过常规治疗手段维持生命的患者,ECMO可作为“桥梁”,为患者提供足够的氧合和循环支持,维持患者的生命以等待肺移植;对于术中出现的氧合、循环不稳定,ECMO可提供心肺支持,保障手术平稳进行;在术后,ECMO帮助患者平稳度过手术后的关键时期,可作为原发性移植物功能障碍、急性排斥反应、感染或心力衰竭等严重并发症的治疗手段,改善预后。ECMO技术在肺移植中已得到广泛应用,ISHLT报告数据显示,全球注册记录的肺移植术中ECMO开展量占总肺移植人数的29%[2]。据《中国器官捐献和移植发展报告》指出,2022年我国肺移植患者术前使用ECMO的比例为5.9%。ECMO术前平均桥接时间为120 h;77.6%的手术使用了术中ECMO辅助;转流方式以静脉-静脉(veno-venous, V-V)ECMO(61.1%)和静脉-动脉(veno-arterial,V-A)ECMO(33.6%)为主。2023年成人术中ECMO使用率达到79.7%,儿童为77.3%[3]。然而,目前关于ECMO在肺移植围手术期的管理缺乏标准化的诊疗规范,尚无统一的应用指南。因此,中华医学会器官移植学分会肺移植学组组织国内相关多学科专家,组织编写了《体外膜肺氧合在肺移植围手术期的应用指南》,以期为我国肺移植相关临床科室的ECMO规范使用提供指导。
1 指南制定方法本指南的制订工作组由肺移植科、重症医学科、麻醉科、护理部等学科专家组成。所有制订工作组成员均声明不存在与本指南相关的经济或非经济利益冲突。本指南已在国际实践指南注册与透明化平台(Practice Guide Registration for TransPAREncy, PREPARE)上以中英双语注册(注册号:PREPARE-2024CN362)。
临床问题调研与遴选:指南工作组对国内外该领域发表的指南和共识进行比对,针对既往指南中涉及和有研究进展的内容及临床医生重点关注的内容,经过问卷调查和专家组会议讨论,最终形成14个临床问题,主要涉及到ECMO在肺移植术前、术中、术后等方面。
证据检索与筛选:按照人群、干预、对照、结局(population、intervention、comparison、outcome,PICO)原则,证据评价组对需解决的14个临床问题进行解构,然后分别制定包含主题词和自由词的检索策略,并进行系统检索。全面检索国内外文献数据库,文献的检索时间主要为近20年:2000年1月至2024年12月。完成证据检索后,每个临床问题均由指南专家组成员按照题目、摘要和全文的顺序逐级独立筛选文献,确定纳入符合具体临床问题的文献,完成筛选后两人进行核对,如存在分歧,则通过共同讨论或咨询第三方协商确定。经过筛选后由指南撰写小组进行证据整合和评价相关材料后形成条目,指南制定小组的每位专家成员先选择1~2个条目,综合考虑证据以及我国医患的偏好与价值观、干预措施的成本和利弊等因素后,指南工作组提出符合我国临床诊疗实践的条推荐意见,形成指南初稿。
证据分级和推荐强度分级:本指南使用2009版牛津大学循证医学中心的证据分级与推荐强度标准对每个临床问题的证据质量和推荐强度进行分级(表 1)。
| 推荐强度 | 证据级别 | 治疗或危害 |
| A | 1a分级 | RCT的系统评价 |
| 1b | 结果可信区间小的RCT | |
| 1c | 显示“全或无效应”的任何证据 | |
| B | 2a | 队列研究的系统评价 |
| 2b | 单个的队列研究(包括低质量的RCT,如失访率>20%者) | |
| 2c | 基于患者结局的研究 | |
| 3a | 病例对照研究的系统评价 | |
| 3b | 单个病例对照研究 | |
| C | 4 | 病例系列报告、低质量队列研究和低质量病例对照研究 |
| D | 5 | 专家意见(即无临床研究支持的仅依据基础研究或临床经验的推测) |
推荐意见的形成:指南初稿撰写完成后提交外审组专家进行审阅,根据其反馈意见对初稿进行修改,初稿确定后指南组组织审稿专家组集体讨论审定,最后经过中华医学会器官移植学分会常委会通过,形成《体外膜肺氧合在肺移植围手术期的应用指南》。
2 推荐意见及说明本指南围绕临床实践提出14个问题,形成45条推荐意见,主要包含ECMO在肺移植术前、术中、术后相关临床问题,并出了详细的推荐强度和证据评分。
问题1:对于肺移植多学科诊疗(Multi-Disciplinary Treatment,MDT)团队及ECMO团队建设的建议?
推荐意见1:在肺移植临床实践中,应加强多学科团队协作下的肺移植围术期管理,包括手术、麻醉和重症医学管理,并组建专业、结构合理的ECMO快速反应团队,明确职责分工,确保团队高效协作。(推荐强度:B证据等级:2)
推荐意见说明:目前,随着肺移植手术被更多的人认识并接受,选择肺移植的受者的病情逐渐复杂化。与此同时,使用扩展标准和欠理想的供体的增多,使肺移植的发展面临诸多挑战。肺移植传统的医患关系模式正逐渐从单一专科主导,转向多学科团队(MDT)共同参与、以患者为中心的诊疗决策模式[4]。在这一模式下,患者的评估、治疗规划及围手术期管理均需由多学科团队协作完成。尽管传统上外科医生是这多学科合作的核心成员,但麻醉医生和重症监护医生越来越多地参与移植MDT,协助完成手术决策、风险分层并制定个体化围手术期管理方案,这对降低手术与麻醉相关风险具有重要意义[4-7]。
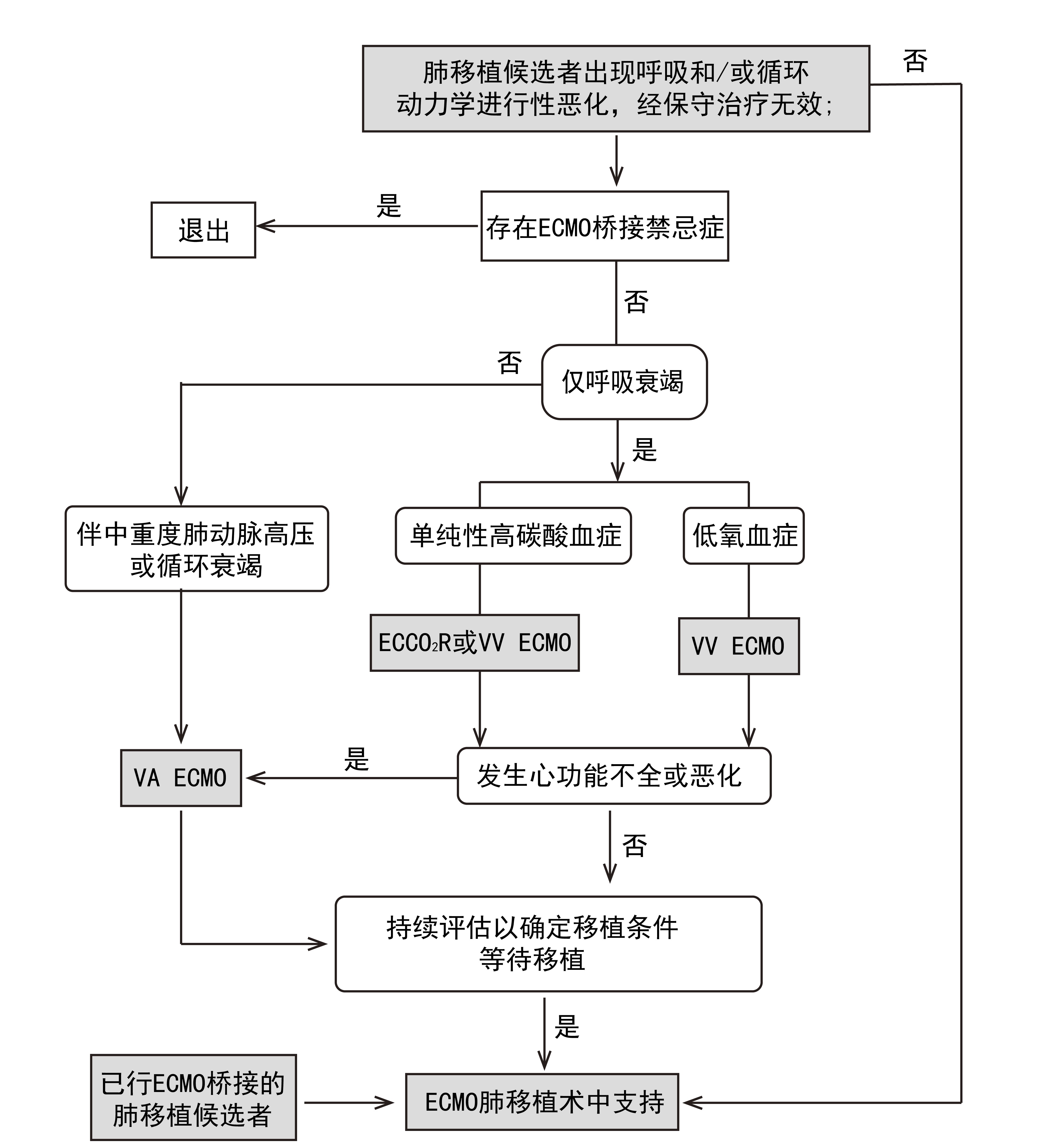
ECMO技术的成功开展依赖于专业的ECMO快速反应团队[8]。团队应优化完善自身ECMO技术能力,保证成员在面对突发应急状况时均具有良好快速反应能力,从而高效提供院内、院外救治工作[9]。为了确保肺移植患者在术前、术中和术后的治疗效果,建议ECMO团队应与肺移植多学科团队密切合作,确保团队人员的合理配置。ECMO团队应包括具有丰富经验的负责人、技术操作人员以及设备和信息管理员。团队成员应定期接受ECMO技术及相关急救培训,确保能够应对肺移植过程中可能出现的突发情况。通过优化人员分工和强化专业培训,提升团队在肺移植围术期中的快速响应能力和救治水平,从而确保患者获得最佳的治疗效果。见图 1。
|
| 注:ECMO:体外膜肺氧合;ECCOR:体外二氧化碳清除;W: 静脉-静脉;VA:静脉-动脉;VAV:静脉-动脉-静脉;PA-LA旁路:肺动脉-右心房旁路 图 1 肺移植受者术前体外膜式氧合(ECMO)桥接流程图 |
|
|
问题2:哪些患者适合术前ECMO桥接治疗?
推荐意见2:在肺移植评估过程中或已纳入等待名单的患者,出现呼吸和(或)血流动力学恶化,经常规治疗无效时,如无新发肺移植及ECMO禁忌证,建议使用ECMO桥接。(推荐强度:B证据等级:2a)
推荐意见3:新转诊的急性心肺功能衰竭患者,高度依赖ECMO且肺移植是唯一治疗方案的患者,可使用ECMO桥接。(推荐强度:B证据等级:2)
推荐意见说明:ECMO作为肺移植术前的桥接技术,提供有效的心肺功能支持,维持患者的氧合和循环功能[10]。Chiumello等[11]对在2010至2014年发表的14项研究中ECMO桥接肺移植患者的1年生存率进行了回顾性分析,肺移植前ECMO的桥接中位时间为3~16 d。其中,5项研究报告生存率为50%~70%,4项研究报告生存率为70%~90%,2项研究报告生存率高达90%[11]。ECMO桥接移植的成功通常取决于中心在ECMO和肺移植方面的经验,通常由外科医生、麻醉医生、ECMO专家和内科医生组成的多学科团队选择合适的潜在受者[12]。潜在可接受ECMO支持作为肺移植桥梁的患者可分为两类。第一类包括已经列入肺移植等待名单或评估过程中的患者,在等待期间出现呼吸和/或血流动力学恶化,因此需要呼吸和(或)循环支持直至完成肺移植。第二类包括新携带ECMO转诊至肺移植中心的患者,此类患者高度依赖ECMO支持无法脱机,且由于不可逆的呼吸衰竭,肺移植仍是唯一的治疗选择[10, 13-15]。当术前使用ECMO桥接时,依据患者具体病情,可在术中延续V-V ECMO或V-A ECMO,或更改模式为中心插管VV-A ECMO或VAV-ECMO。
问题3:清醒ECMO的适用人群及实施措施?
推荐意见3:意识清醒、呼吸驱动正常、配合度高,血流动力学基本稳定,有较好气道保护能力的患者,可实施清醒ECMO。(推荐强度:B证据等级:2b)
推荐意见4:清醒ECMO患者,需要密切监测其血流动力学及呼吸功能,并根据患者耐受程度积极进行行走和/或康复训练。(推荐强度:B证据等级:2b)
推荐意见说明:清醒ECMO是指在不进行气管插管的情况下,对意识清醒且能够自主呼吸的患者实施ECMO支持。清醒ECMO具有诸多优势,例如:允许患者进行身体活动,保持肌肉质量和力量;保留自主呼吸可锻炼呼吸肌和膈肌功能;降低因气管插管导致的呼吸机相关性肺炎风险;减少镇静镇痛药物用量,进而降低谵妄发生率。因此,对于意识清醒、配合度高、血流动力学基本稳定,有较好气道保护能力(可自主咳痰、误吸风险小)的患者可考虑将清醒ECMO作为首选策略[16]。研究表明,术前清醒ECMO已显示出良好的结果。Tipograf等[14]通过倾向评分匹配调整了基线特征后发现,70例接受清醒ECMO的患者与未接受桥接治疗的患者在肺移植后的生存率差异无统计学意义(log-rank P=0.53)。Kim等[17]最近报道,与接受传统镇静ECMO的患者相比,清醒ECMO组在肺移植术后所需的机械通气时间更短,ICU住院天数更少,且术后行走能力与肺功能恢复更佳。
对于清醒ECMO的患者,积极的物理治疗(包括行走训练)与提高移植成功率、改善术后生存率及功能恢复密切相关。研究表明,在多学科团队的密切监护下实施清醒ECMO及相关康复活动是安全的[18]。康复活动应从简单、被动的方式开始,并根据患者的耐受情况,逐步过渡到更复杂、主动的训练。在清醒ECMO期间,必须警惕管路移位或血流不畅可能引发的严重低氧血症等危及生命的并发症。因此在康复活动期间,医务人员需仔细观察管路情况,并监测因体位改变可能导致的ECMO流量变化[19]。医务人员应密切监测患者生命体征,以确定是否继续或调整康复活动。肺移植前的呼吸康复训练有助于维持呼吸肌功能,减少分泌物潴留,降低术后并发症的风险[20]。在开始呼吸康复之前,应对患者进行全面的呼吸功能评估,包括胸部影像学检查、气道状态(是否行气管切开)、胸廓和膈肌的运动、呼吸频率和肺部听诊等。此外,为ECMO患者指定呼吸治疗方案时,还需综合考虑其ECMO插管位置、肺顺应性、抗凝水平和原发疾病。由于设备和管路的存在可能引起患者的焦虑躁动情绪,增加呼吸功和耗氧量,并加重低氧血症,因此可使用低剂量的镇痛镇静药物予以缓解。此外,随着患者活动度增加,也需警惕诸如导管移位、管路破损或泵故障等ECMO相关技术性并发症的风险。
问题4:如何选择术前ECMO模式?
推荐意见5:单纯缺氧和/或高碳酸血症,血流动力学稳定或无右心衰竭患者的术前桥接,首选V-V ECMO。(推荐强度:B证据等级:2b)
推荐意见6:当终末期肺病伴肺动脉高压合并右心衰竭,引发严重血流动力学障碍及呼吸衰竭时,应优先考虑V-A ECMO或V-A-V ECMO。(推荐强度:B证据等级:2b)
推荐意见7:高碳酸血症呼吸衰竭患者可选择体外CO2清除装置(ECCO2R)。(推荐强度:B证据等级:2c)
推荐意见说明:对于因单纯性缺氧和/或高碳酸血症而需术前桥接、且不伴有血流动力学不稳定或右心衰竭的呼吸衰竭患者,应首选V-V ECMO模式。V-V ECMO置管相对简单、方便,相对直接,适用于床边或手术室置管,也可应用于紧急抢救性ECMO支持治疗,降低患者在等待供体期间的病死率[21]。研究表明,对于单纯性呼吸衰竭患者,初始支持方式选择V-V ECMO的预后优于V-A ECMO [22-23]。此外,在V-V ECMO支持期间,若晚期才识别出右心功能不全,可能导致显著的发病率和病死率升高。因此,应定期进行血流动力学评估,并通过超声心动图和/或肺动脉导管监测右心室功能。
对于终末期肺动脉高压和(或)合并右心衰竭、并由此导致严重血流动力学障碍的呼吸衰竭患者,应优先考虑V-A ECMO桥接。其应用指征包括:(1)常规血管活性药物效果不佳,出现血流动力学障碍。(2)心脏指数<2 L/(m2·min)持续3 h以上。外周V-A ECMO置管首选股动静脉,以右侧为优。中心V-A ECMO通常选择右心房及升主动脉进行置管。该方式需在开胸手术下直视完成,操作创伤较大,因此常在手术室中实施,主要用于肺移植术中的ECMO支持[24]。采用VAV ECMO是预防股动脉插管患者发生上半身缺氧的一种有价值的选择。
对于仅存在高碳酸血症的呼吸衰竭患者,高碳酸血症主要由肺泡通气不足(如COPD急性加重、严重哮喘)或死腔通气增加(如ARDS)导致,本质是二氧化碳清除障碍而非氧合衰竭。针对此类患者,可选择体外CO2清除(ECCO2R)装置。该技术通过低流量(0.5~1.5 L/min)体外循环高效清除二氧化碳(清除率可达50~100 mL/min),能直接纠正呼吸性酸中毒。
问题5:术前长程ECMO的管理要点有哪些?
推荐意见8:术前长程ECMO管理的关键在于对感染、出血、血栓、肢体缺血坏死、营养不良和肌无力等并发症的防治。(推荐强度:B证据等级:2b)
推荐意见说明:多项研究表明,ECMO桥接时间的长短并不影响患者的短期及长期生存率[25-26]。但需注意的是,长程ECMO支持常伴随并发症发生率的增加,因此其管理关键在于常见并发症的防治。对于病情相对稳定的患者,可通过俯卧位通气[27]改善痰液引流,预防呼吸机相关性肺炎并减轻呼吸机相关肺损伤。研究表明,在ECMO支持时间达30~40 d的患者中,导管相关性血流感染的发生率可高达91% [28]。为防治此类血流感染,推荐常规使用经外周静脉置入的中心静脉导管(PICC)替代传统中心静脉导管(CVC)[29],并减少对氧合器及ECMO管路的非必要操作。若患者出现不明原因发热、临床上高度怀疑导管相关性血流感染,或穿刺部位皮肤破溃明显、溢脓时,应及时更换相关导管,切莫因等待病原学结果而延误导管更换时机[30]。对于长程ECMO带来的出血风险,在排除可纠正的非抗凝相关因素后,可将活化部分凝血活酶时间(APTT)的抗凝目标值维持在40~55 s。该目标范围有助于降低出血风险,同时未显著增加血栓形成风险 [31]。
对于计划接受肺移植的长程ECMO桥接患者,应定期评估患者的呼吸与循环功能、营养水平、心理状态,以及对ECMO的耐受性。定期对ECMO管路、氧合器等设备进行检查和维护,以预防意外事件的发生。应密切监测患者的病情变化,并据此制定个性化的治疗方案,涵盖药物治疗、营养支持与康复训练等多维度措施。同时,需进行手术风险评估、指定详细的手术计划,以准确把握手术时机。通过全面、细致的医疗团队协作,确保患者在手术前获得最佳的生命支持和治疗效果。
问题6:肺移植术中体外生命支持方法有哪些?
推荐意见9:对于需要体外生命支持的患者,建议使用ECMO代替体外循环(cardiopulmonary bypass,CPB)。(推荐强度:B证据等级:2b)
推荐意见10:外周V-V ECMO患者术中出现低氧血症、继发性心力衰竭、肺叶移植时,可将模式转换为中心插管V-A-V ECMO/V-V-A ECMO, 手术结束时再逐步降低流量,更改为外周V-V ECMO、V-A ECMO或外周V-A-V ECMO模式。(推荐强度:C证据等级:4)
推荐意见11:V-A ECMO患者出现差异性缺氧时,可转换为外周VAV ECMO。(推荐强度:C证据等级:4)
推荐意见12:当同期需要进行心脏手术(心脏缺损修复、瓣膜手术等)的肺移植时,需要CPB支持。心脏手术完成后心脏复跳,CPB可转换为中心插管ECMO,肺移植完成后,可撤离中心插管,改为外周ECMO支持。(推荐强度:B证据等级:2c)
推荐意见说明:尽管目前ECMO在肺移植中应用广泛,但并非所有患者均需要接受术中ECMO辅助下肺移植。对于术前心功能良好、肺动脉压基本正常且能够耐受单肺通气的受者,术中可无需ECMO支持[32]。多项研究表明,与体外循环(CPB)相比,ECMO支持可获得更优的预后指标[33]。Ius等[34]比较了92名分别在ECMO或者CPB支持下接受移植的患者,结果发现CPB组患者PGD的发病率更高,且需要再次机械支持的比例也更高。此外,Dell’Amore等[35]对比了21例与17例分别接受ECMO与CPB支持的肺动脉高压患者,结果显示CPB组患者肾功能损害的发生率与PGD严重程度更高,而ECMO组的住院病死率更低。在肺移植术中,CPB支持还会增加输血需求,这与其可能引发的纤溶亢进、血小板功能障碍和凝血因子稀释有关[36]。在小儿肺移植中,Parikh等[37]比较了术中接受ECMO(n=13)和CPB(n=22)支持的患儿,发现ECMO组需要输注的新鲜冷冻血浆、血小板及红细胞制品均更少。因此,ECMO是肺移植首选的体外支持方式。
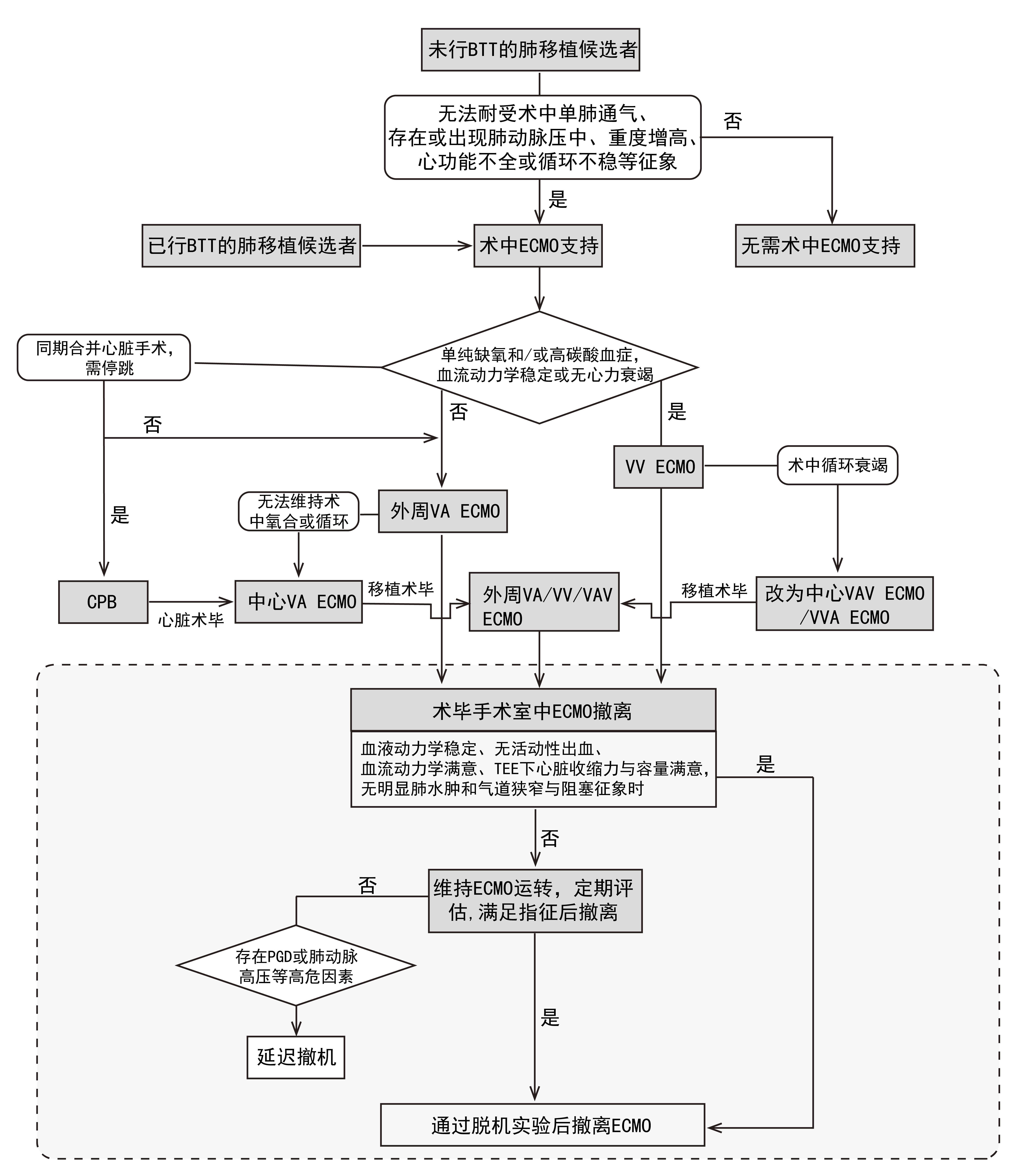
尽管ECMO可部分替代心肺功能,但不同支持模式下的ECMO仍存在不足。V-V ECMO支持的并发症之一是流量供应不足。合并严重呼吸衰竭的患者常伴有心输出量代偿性增高,甚至达到超生理水平。V-V ECMO的流量通常被限制在5~6 L/min以内,可能无法为循环提供充足氧合。因此,即使接受了V-V ECMO支持,患者仍可能持续存在低氧血症。此外,对于初始采用外周V-V ECMO支持的患者,若术中发生顽固性低氧血症、继发性心力衰竭或仅进行肺叶移植时,可将模式转换为经中心插管的VAV ECMO/VVA ECMO,以有效减轻右心负荷、降低右心室壁张力,手术结束时再逐步降低流量,更改为外周V-V ECMO、V-A ECMO或外周V-A-V ECMO模式[38]。对于V-A ECMO支持但仍存在引流不足的患者,在排除管路因素(如扭结、阻塞、移位等)、患者因素(如张力性气胸、心包填塞等)并纠正血容量不足后,则需考虑可能存在引流插管管径过细或所置血管管腔容积不足,此时需要额外的引流插管。此外,由于逆流的V-A ECMO血流量可能无法与自身心脏左心室输出的血流相对抗,这导致患者身体出现差异性缺氧,也称为Harlequin综合征或南北综合征。当V-A ECMO患者出现继发性肺功能障碍、上半身缺氧,在调整通气设置(FiO2、PEEP)及积极利尿无效时,可采用V-A-V ECMO,通过减少无氧血液返回左心,增加体循环含氧血灌注,改善上半身缺氧[39]。但应密切记录流量差,避免氧合血优先回流到低阻力的肺循环而非体循环。由于CPB可完全控制患者的血流动力学,从而更易于处理肺移植过程中的关键事件。因此,对于需同期进行心脏手术(如心脏缺损修复、瓣膜手术等)的肺移植病例时,通常需要CPB支持。待心脏手术完成、心脏复跳后,可将CPB支持转换为经中心插管的ECMO模式。待肺移植完成后,再撤离中心插管,转而建立外周ECMO支持。见图 2。
|
| 图 2 肺移植受者术中及术后体外膜式氧合(ECMO)应用流程图 |
|
|
问题7:肺移植术中ECMO管理的要点?
推荐意见13:术中需通过多种手段,如Swan-Ganz导管、食道超声、血气分析等监测血流动力学状态及导管位置。(推荐强度:B证据等级:2c)
推荐意见14:术中应保证ECMO流量稳定,在改变体位、压迫心脏或肺动脉开放等阶段,需关注ECMO流量、流速、氧体积分数,并根据血流动力学状态及通气需求调整。(推荐强度:C证据等级:4)
推荐意见说明:完成外周ECMO置管后,应立即通过超声或X线影像学检查确认引流管头端位置,以排除导管异位风险,避免因引流不畅导致的流量波动或负压损伤。经确认流量持续稳定(通常维持>2.5 L/min且负压平稳)后再行牢靠固定。在ECMO运转过程中,其流量主要依据容量、组织氧供/氧耗比、生命体征、混合静脉血氧饱和度等监测指标动态调节,一般维持50~80 mL/(kg·min)的流量,混合静脉氧饱和度(SvO2)>70%可满足需要,达到既能满足氧供、又不增加右心室后负荷的目标[40]。因此,术中需通过多种手段,如Swan-Ganz导管、食道超声、血气分析等监测血流动力学状态及导管位置。无锡市人民医院金宽哲等[41]的一项回顾性研究表明,ECMO支持肺移植手术中流量维持在(2.8±0.6)L/min,术中低氧状况均有良好改善,移植受者均顺利完成手术,氧合支持效果理想。
术中应确保ECMO流量稳定,在改变体位、牵拉纵隔、压迫心脏或阻断肺动脉及移植完成开放肺动脉等各种阶段,均需关注ECMO流量、流速、氧体积分数,并根据血流动力学状态及通气需求调整[24]。同时,移植肺本身的营养依赖于肺循环,V-A ECMO可分流肺动脉血流,因此应保持V-A ECMO处于部分流量的辅助状态而不是全流的替代状态,保持适当右心室做功,以保证移植肺自身的血供。
问题8:术毕手术室中撤离ECMO指征?
推荐意见15:术毕血液动力学稳定、无活动性出血、血气满意、直视与经食管超声心动图(trans esophageal echocardiography,TEE)下心脏收缩力与容量满意,无明显肺水肿和气道狭窄与阻塞征象,且不存在术后PGD的供受体高危因素,可逐渐降低ECMO流量至0.5 L/min,撤除ECMO。(推荐强度:B证据等级:3b)
推荐意见16:术中循环不稳定或移植肺水肿氧合差,ECMO可延迟撤离,或将中心ECMO改为外周ECMO。(推荐强度:B证据等级:2a)
推荐意见说明:部分术中接受ECMO支持的患者在移植术毕,若情况稳定,可顺利撤离ECMO。手术结束时,观察受者状态,如患者血流动力学稳定、无活动性出血、血气满意、血管与气道吻合口通畅、直视下心脏收缩有力且容量状态满意、无明显肺水肿和气道狭窄与阻塞征象且不存在术后PGD的供受体高危因素,在与麻醉医生共同决策后,可将ECMO流量逐渐降低至0.5 L/min,并试行撤离。撤离的ECMO机器仍需保持内循环模式以备随时启用。胸腔内插管可直接拔除,然后用无菌接头连接动静脉环路继续ECMO内循环。内循环期间,需向管路内加入4 000 U肝素,并将流量维持在约2 L/min,以防止管路内血栓形成。如果出现需要高剂量升压药维持的血流动力学不稳定或通过经食管超声心动图发现心脏功能下降的迹象,则需要V-A ECMO维持。若患者血流动力学稳定,但仍存在缺氧,则应维持V-V ECMO支持以提供呼吸辅助[42]。
严重的PGD仍是肺移植术后早期死亡的主要原因,其发病率在15%~25%之间[43-44]。几项回顾性单中心研究已经证明了ECMO在大多数严重PGD患者中支持性治疗的有效性[45]。当出现移植肺功能障碍时,在手术结束时选择继续维持ECMO,有助于逐渐恢复肺功能,提高患者的早期生存率。若术中因PGD而建立ECMO支持,则应在术后继续维持,直至移植肺功能恢复[46]。研究表明,术后应用V-V ECMO技术,可显著提高术后发生严重PGD患者的生存率[47-48]。尽管导致严重PGD的决定性因素尚不明确,但有证据表明,ECMO介入越早,对移植物存活率和患者生存率的改善效果越显著[49-50]。
问题9:肺移植术后ECMO撤机的指征是什么?
推荐意见17:术后循环稳定、氧合满意,详细评估心肺功能情况后,可择期撤除V-A或V-V ECMO。(推荐强度:B证据等级:2b)
推荐意见说明:肺移植术后,一旦患者的呼吸与循环功能趋于稳定,应考虑尽快撤离ECMO,以降低ECMO相关并发症的发生风险。对于肺移植术后患者,如为V-V ECMO模式,逐渐减低ECMO血流量至1 L/min,然后逐步减低ECMO通气量,氧合仍维持满意,无二氧化碳潴留,血气内环境稳定,影像学改善明显,可考虑脱离V-V ECMO[51-52]。6 h短暂性停止V-V ECMO供气,患者氧合在完全脱离ECMO的支持条件下仍能维持满意,则预示着成功撤离V-V ECMO的可能性较高[53]。对于V-A ECMO模式,除肺功能恢复之外,还需充分评估心功能恢复情况,通常的心功能恢复指标包括:低剂量血管活性药即可维持血流动力学稳定、自身脉压差≥20 mmHg、床旁超声指标改善(包括心脏每博排出量、心室大小、主动脉速度时间积分、射血分数等)[54]。
问题10:术后应用ECMO上机指征及注意要点有哪些?
推荐意见18:严重PGD患者可接受TEE检查,以排除左心室功能障碍、心内分流、肺静脉吻合口狭窄或血栓形成等可逆性病因。(推荐强度:B证据等级:3)
推荐意见19:当PGD主要表现为单纯性呼吸衰竭(顽固性低氧血症或高碳酸血症)且患者血流动力学稳定时,优先选择V-V ECMO。(推荐强度:A证据等级:2b)
推荐意见20:若接受ECMO支持的严重PGD患者在短期内未出现肺功能改善,可经多学科团队讨论决定是否需二次移植。(推荐强度:C证据等级:2a)
推荐意见21:严重PGD患者可接受TEE检查,以排除左心室功能障碍、心内分流、肺静脉吻合口狭窄或血栓形成等可逆性病因。(推荐强度:B证据等级:3)
推荐意见说明:移植术后早期可出现各种原因导致的急性呼吸衰竭,包括PGD、肺动脉高压患者术后急性心功能不全、胸腔积液、感染、急性排斥反应、肺动脉或静脉吻合口狭窄等手术并发症,临床表现为低氧血症、严重呼吸性酸中毒、肺动脉压力增高、肺顺应性下降。常规治疗无效时,建议行ECMO辅助支持治疗。基于不同的临床情况及病理生理状况,研究报道的ECMO启动时机不一,但早期建立ECMO至关重要。回顾性显示,与延迟ECMO相比,早期应用ECMO可降低PGD发生率,并提高早期和长期存活率[49, 55-56]。ECMO能够提供充分的气体交换支持,为移植物从缺血-再灌注损伤中恢复创造了关键窗口期,临床研究显示及时干预可降低继发多器官功能障碍的风险,并为后续治疗争取时间[50, 57-58]。当PGD主要表现为单纯性呼吸衰竭时,选择V-V ECMO的核心优势在于规避动脉插管带来的风险。股动脉插管导致的肢体缺血发生率可达10%~33%[59],且可能引发上半身差异性缺氧;而V-V ECMO仅需静脉通路,显著降低血管损伤和神经并发症风险[60]。ECMO支持超过2周将显著增加导管相关感染、不可控出血及氧合器血栓形成的风险,而肺功能无改善者再移植后的存活率较低[61-63]。此类患者可经多学科团队讨论决定是否需二次移植。
约15%~20%的PGD临床表现源于非原发性因素:肺动脉高压患者术后可能出现左心室舒张功能失代偿[64-65];未闭合的卵圆孔可导致右向左分流加重低氧[66];而肺静脉吻合口并发症(如狭窄或血栓)可能直接引发移植物梗死[67-68]。TEE能实时评估心脏收缩/舒张功能、房间隔完整性及肺静脉血流动力学,对机械通气患者具有不可替代的诊断价值[69]。早期识别此类病变可指导紧急干预(如血栓清除或手术修复),避免因误诊为原发性PGD而过度延长ECMO支持。
问题11:肺动脉高压移植患者的ECMO管理特殊要点?
推荐意见22:对于严重肺动脉高压患者,建议麻醉诱导前采用清醒ECMO,以期维持血流动力学稳定。(推荐强度:D证据等级:5)
推荐意见23:对于中度至重度继发性肺动脉高压的患者,根据患者术前心功能情况,肺移植手术时应首选外周或中心V-A ECMO。(推荐强度:B证据等级:2a)
推荐意见24:肺动脉高压患者术后需动态监测心功能,持续监测肺动脉压,并根据心肺功能延长V-A ECMO辅助时间,促进心脏逐渐逆向重塑。(推荐强度:B证据等级:2b)
推荐意见说明:肺动脉高压患者发生严重右心衰竭,需要综合治疗,包括处理诱发或加重心衰的因素、精细液体管理以及应用改善心功能的措施。若在充分药物优化治疗后,患者临床病程仍然提示存在严重的右心衰竭,则应启动ECMO。V-A ECMO支持适用于因肺血管阻力增加而导致右心室衰竭进而发生血流动力学恶化的患者[22-23, 70-72]。因此,对于联合呼吸衰竭和右心室衰竭,建议使用V-A ECMO支持进行术前桥接[73]。
对于严重肺动脉高压患者,麻醉诱导前预置“清醒ECMO”是一种关键的预防性策略,旨在规避诱导过程中因麻醉药物抑制心肌、降低全身血管阻力及正压通气增加肺血管阻力所引发的呼吸循环衰竭。ECMO在诱导前建立,可提供即时的心肺支持,维持体循环压力和冠状动脉灌注,保证氧合,从而打破右心衰竭-低血压的恶性循环,确保麻醉诱导和手术过程的安全平稳[74]。此外,多项研究表明,肺动脉压力升高需要术中ECMO支持[75]。一些学者[76]提出将肺动脉收缩压的临界值定为50 mmHg,表明患者很可能无法耐受肺动脉钳夹,需要进行ECMO支持。对于既往存在中度至高度继发性肺动脉高压的肺移植受者,术中首选外周或中心插管V-A ECMO支持。
肺动脉高压也是肺移植后PGD的独立危险因素。因此,建议术后延迟V-A ECMO撤机时间,通过主动调控肺血管阻力、减轻新移植肺的毛细血管应激性渗漏,同时提供充分氧合以降低缺血-再灌注损伤,从而显著抑制严重PGD的发生,并为右心功能恢复及移植物早期适应赢得关键时间窗,促进心脏逆向重塑,最终改善术后生存率与器官功能预后[77]。由于缺血-再灌注过程中的肺对左心房压力的细微变化十分敏感,移植完成后的最初72 h至关重要[64]。
问题12:V-V ECMO单管双腔置管(double lumen catheter,DLC)的注意要点?
推荐意见25:单管双腔置管可用于肺移植术前清醒桥接,常用部位是右侧颈内静脉。(推荐强度:B证据等级:3)
推荐意见26:DLC可通过TEE或X线等影像学来指导置管定位, 运行期间可通过体表超声声学造影定位。(推荐强度:B证据等级:3)
推荐意见说明:单管双腔插管(DLC)通过在TEE下或X线下将其置于颈内静脉,要求插管引流端位于下腔入房口,灌注孔正对三尖瓣。该技术仅在颈静脉置入单根导管,其具有以下优势:单部位插管减少插管损伤以及出血和感染的风险;双腔颈内插管血流路径短、降低再循环分数,提升ECMO效率;预防远端缺血;单部位置管减少股静脉置管,为更多通路提供可能,也不限制下肢活动,患者的压力减少、舒适度提升,有利于患者早期康复治疗,改善患者的预后。此种插管方式可用于肺移植围术期患者呼吸循环支持,有助于患者的清醒、行走和早期活动[78],亦可用作术中支持。单管双腔插管的劣势在于置入时需在影像学引导下确认导管的准确位置,包括插管深度和旋转角度,对置管定位要求较高,最好在TEE或DSA监测下进行,保证其位置和功能。法国的全国性多中心回顾性研究显示DLC置入过程中超声引导置管占据主导地位,其中TEE引导占67%、TTE引导占25%、透视引导占4%、未经引导占4%[79]。由于TEE超声探头放置于心脏后方,避免了胸壁和肺部气体的干扰,良好的分辨率为心脏、大血管结构提供了清晰的视野。因此,与TTE相比,TEE在双腔插管中应用更为普遍。
问题13:肺移植围手术期ECMO的抗凝管理?
推荐意见27:ECMO管道置入时进行全身肝素化,普通肝素是首选的抗凝剂,初始剂量一般为50~100 U/kg,对于即刻开始手术的可减少至无肝素抗凝或低剂量抗凝。(推荐强度:B证据等级:2b)
推荐意见28:术中建议对ACT、APTT、血栓弹力图等凝血指标进行监测,调整抗凝药物用量。(推荐强度:B证据等级:2)
推荐意见29:对于术中广泛黏连,出血风险大的患者,可适当降低肝素钠用量。(推荐强度:B证据等级:2)
推荐意见30:围术期ECMO支持的患者输注血液制品时,应密切监测ECMO膜肺功能及血栓情况。
推荐意见说明:抗凝和出血预防贯穿ECMO应用的全过程,ECMO的抗凝是降低血栓风险和维持系统运转的关键。由于ECMO管路的非生物表面特性、转流的机械损伤等因素[80],肺移植患者围手术期应用ECMO需常规给予外源性抗凝。随着材料学的进步,现有的ECMO管路多采用肝素化涂层,能起到一定的抗凝作用,但仍推荐在ECMO管道置入时进行全身肝素化,普通肝素是ECMO运行期间首选的抗凝剂,其成本低、作用迅速,且有快速可用的拮抗剂(鱼精蛋白),初始剂量一般为50~100 U/kg[81]。在移植术中可不给予抗凝应用,但仍需要在术中根据ACT、APTT、血栓弹力图等凝血指标进行监测,调整抗凝药物用量。
在ECMO辅助过程中,根据患者基础疾病、手术创面渗出情况和血红蛋白水平制定抗凝目标,防止发生出血,必要时补充血小板及凝血因子。肺与胸壁间致密黏连者,可适当降低肝素钠用量,防止黏连分离处广泛渗血。V-V ECMO对抗凝要求较低,依据术中具体情况,必要时可不用肝素钠维持,但应维持足够的ECMO流量。也有报道对术中黏连严重或凝血功能严重紊乱的患者采用无肝素抗凝方案[82-83],但应严格掌握无肝素抗凝的适应证,权衡血栓和出血的风险,监测各项凝血功能指标,密切监测膜肺血栓及血栓性疾病等并发症的出现。V-A ECMO在维持足够流量的前提下,采用较低剂量的肝素抗凝(≤60 IU/kg)不会增加血栓形成,且有助于降低术后出血风险[84]。
值得注意的是,术中输注血液制品(尤其是血小板和冷沉淀)会显著改变患者的凝血状态[85-86],一方面可能诱发高凝性血栓,导致膜肺纤维丝沉积、气体交换效率骤降及跨膜压差的改变,甚至造成环路栓塞或失效;另一方面也可能加重凝血因子消耗,增加出血风险[87]。因此,围术期ECMO支持的患者输注血液制品时,应严密监测旨在实时评估膜肺功能(如观察血栓形成、血浆渗漏及氧合变差等情况),及时调整抗凝策略与支持方案,从而在维持有效氧合与循环支持的同时,预防危及生命的血栓或出血事件。
问题14:如何避免和应对肺移植ECMO支持期间可能出现的出血、血栓、肢体缺血等并发症?
推荐意见31:建立急性出血的多学科应急流程,快速明确病因并制定干预方案。(推荐强度:C证据等级:3)
推荐意见32:对于术后出现不明原因的移植物功能不全,应优先考虑移植肺血管血栓形成的可能。(推荐强度:B证据等级:2b)
推荐意见33:为预防肢体缺血,建议应用偏细型号导管在股浅动脉置入侧支灌注管,实现再灌注。(推荐强度:B证据等级:2b)
推荐意见说明:出血是ECMO运行过程中一种常见的并发症[88],也是导致早期ECMO被迫终止的最常见原因,会增加患者死亡风险[89]。临床可直接表现为血液通过切口渗出至体表或流至体腔,还可间接表现为血红蛋白浓度进行性降低、静脉引流量下降、中心静脉压降低、脉压降低和心率增快等。肺移植术后一旦发生活动性出血,应立即启动由外科、麻醉、ECMO团队共同参与的评估流程,首要任务是快速鉴别外科性出血与非外科性(凝血性)出血,查找并评估潜在病因,明确出血部位(插管位置、胸腔、气管、手术创面等),监测凝血指标。发生出血时,通常应降低ACT目标范围,如可将ACT目标范围调整为170~190 s[90-91];活动性出血患者可维持流量>3 L/min,暂停肝素抗凝,密切监测ACT和APTT[92-94]。可根据血栓弹力图(thrombelastography,TEG)或旋转血栓弹性检测(rotational thromboelastometry,ROTEM)或特定凝血因子检测的结果,针对性输注新鲜冰冻血浆、凝血酶原复合物、纤维蛋白原浓缩物/冷沉淀或血小板。
ECMO辅助期间,患者常处于持续高凝状态,加之体外管路缺乏血管内皮覆盖及局部血流存在湍流等因素,易促使血栓形成,亦成为ECMO支持过程中常见的并发症[95-96]。对于ECMO管路中的血栓,可采用手电筒照射管路,通过肉眼观察管路中是否存在血栓,同时也可常规检查所有接口并监测氧合器前后的压力梯度,若压力梯度突然改变提示血栓形成。常规监测D-二聚体,如出现临床不能解释的D-二聚体水平显著升高,则高度提示存在血栓的可能[97]。若发现膜肺大面积血栓形成特别是合并严重溶血征象,应考虑更换管路。肺栓塞可导致缺血性吻合口并发症甚至移植物功能不全(PGD),但由于其症状易与再灌注水肿或急性排异混淆,故需保持高度警惕。一旦术后出现不明原因的氧合恶化、顺应性下降或血流动力学不稳定,应优先考虑该并发症。推荐将床旁超声心动图作为一线筛查工具,用于评估肺静脉血流及心内血栓[98];若高度可疑,需在患者条件允许时及时行CT肺动脉造影(CTPA)以明确诊断,为后续的强化抗凝、溶栓或手术取栓提供依据,从而最大可能挽救移植肺功能[99]。
ECMO支持下的患者发生肢体末端缺血的原因可能为插管口径选择不当、置管后管路阻塞、非搏动血流、全身情况或药物引起的外周血管收缩、静脉血流淤滞等[100]。医护人员应常规观察ECMO患者双侧肢体情况,重点关注置管侧肢体的皮温、周径、张力、皮肤颜色,以及是否出现水疱或足部坏死征象,有条件可借助超声监测下肢动脉血流。可以通过早期应用合适的远端灌注管建立远端下肢供血灌注,预防肢体缺血坏死[101]。对于清醒的患者,可定期询问有无肢端感觉异常,如痛觉消失等。再灌注管必须始终通过透明敷贴固定,以便护士能够观察是否存在扭曲、血凝块和/或纤维素样物质。
3 总结本指南的核心在于通过动态化、个体化的ECMO管理策略,结合多学科协作与精细化操作,最大程度发挥ECMO在肺移植围手术期的救治价值,同时规避相关技术风险。通过建立标准化流程、细化风险分层及动态评估体系,填补围手术期ECMO应用的策略空白,为临床提供兼具科学性与实操性的决策框架,同时强调多学科协作对降低并发症的核心价值。
执笔作者:朱港归(浙江大学医学院附属第二医院)徐永山(浙江大学医学院附属第二医院)杨修成(浙江大学医学院附属第二医院)
参编作者:林慧如(浙江大学医学院附属第二医院)万胡强(浙江大学医学院附属第二医院)周瑜(浙江大学医学院附属第二医院)江贤亮(中国科学技术大学附属第一医院)
主审专家:陈静瑜(浙江大学医学院附属第二医院)黄曼(浙江大学医学院附属第二医院)
审稿专家(按姓名拼音排序):陈惠明(香港玛丽医院)陈琨(金华市中心医院)程周(中山市人民医院)冯敏(郑州大学第一附属医院)郭震(上海交通大学医学院附属胸科医院)何小军(浙江大学医学院附属第二医院)洪小杨(中国人民解放军总医院第七医学中心)吉冰洋(中国医学科学院阜外医院)柯立(中国科学技术大学附属第一医院)李敏(中日友好医院)李平(华中科技大学同济医学院附属协和医院)李双磊(中国人民解放军总医院)李欣(复旦大学附属中山医院)李洋(吉林大学第一医院)林茹(浙江大学医学院附属儿童医院)刘金平(武汉大学中南医院)刘松桥(东南大学附属中大医院)卢安东(兰州大学第一医院)卢安卫(树兰(杭州)医院)乔坤(深圳市第三人民医院)施丽萍(浙江大学医学院附属第一医院)孙兵(首都医科大学附属北京朝阳医院)王大鹏(南京医科大学附属无锡人民医院)卫栋(南京医科大学附属无锡人民医院)吴波(南京医科大学附属无锡人民医院)药晨(中国人民解放军总医院)张国强(中日友好医院)张文平(河南省人民医院)赵高峰(重庆医科大学附属第一医院)周成斌(广东省人民医院)
利益冲突 所有作者声明无利益冲突
| [1] | Chambers DC, Perch M, Zuckermann A, et al. The International Thoracic Organ Transplant Registry of the International Society for Heart and Lung Transplantation: Thirty-eighth adult lung transplantation report: 2021; Focus on recipient characteristics[J]. J Heart Lung Transplant, 2021, 40(10): 1060-1072. DOI:10.1016/j.healun.2021.07.021 |
| [2] | Kirklin JK, Cantor R, Mohacsi P, et al. First annual IMACS report: a global international society for heart and lung transplantation registry for mechanical circulatory support[J]. J Heart Lung Transplant, 2016, 35(4): 407-412. DOI:10.1016/j.healun.2016.01.002 |
| [3] | 黄洁夫. 中国器官捐献和移植发展报告(2023)[M]. 北京: 清华大学出版社, 2025. |
| [4] | Martin AK, Shah SZ, Guru PK, et al. Multidisciplinary approach for lung transplantation due to COVID-19[J]. Mayo Clin Proc Innov Qual Outcomes, 2022, 6(3): 200-208. DOI:10.1016/j.mayocpiqo.2022.02.003 |
| [5] | Martin AK, Yalamuri SM, Wilkey BJ, et al. The impact of anesthetic management on perioperative outcomes in lung transplantation[J]. J Cardiothorac Vasc Anesth, 2020, 34(6): 1669-1680. DOI:10.1053/j.jvca.2019.08.037 |
| [6] | Marczin N, de Waal EEC, Hopkins PMA, et al. International consensus recommendations for anesthetic and intensive care management of lung transplantation. An EACTAIC, SCA, ISHLT, ESOT, ESTS, and AST approved document[J]. J Heart Lung Transplant, 2021, 40(11): 1327-1348. DOI:10.1016/j.healun.2021.07.012 |
| [7] | Chou PL, Liu KS, Chao YK, et al. The impact of surgical learning curve on short-term outcomes after bilateral lung transplantation: results from a multidisciplinary surgical team[J]. Eur J Cardio Thorac Surg, 2023, 64: ezad227. DOI:10.1093/ejcts/ezad227 |
| [8] | 黄雅丽, 蔡淑红, 王谢磊, 等. 转运标准化流程管理在儿科体外膜肺氧合快速反应团队中的应用[J]. 中华急危重症护理杂志, 2024, 5(4): 305-311. |
| [9] | 张婷智, 李颖, 汪晶, 等. 标准化流程干预用于OPCAB术后心肺功能衰竭行ECMO支持患者的护理价值[J]. 中国临床研究, 2024, 37(4): 644-647. DOI:10.13429/j.cnki.cjcr.2024.04.033 |
| [10] | Rando HJ, Fanning JP, Cho SM, et al. Extracorporeal membrane oxygenation as a bridge to lung transplantation: Practice patterns and patient outcomes[J]. J Heart Lung Transplant, 2024, 43(1): 77-84. DOI:10.1016/j.healun.2023.06.016 |
| [11] | Chiumello D, Coppola S, Froio S, et al. Extracorporeal life support as bridge to lung transplantation: a systematic review[J]. Crit Care, 2015, 19(1): 19. DOI:10.1186/s13054-014-0686-7 |
| [12] | Leard LE, Holm AM, Valapour M, et al. Consensus document for the selection of lung transplant candidates: an update from the International Society for Heart and Lung Transplantation[J]. J Heart Lung Transplant, 2021, 40(11): 1349-1379. DOI:10.1016/j.healun.2021.07.005 |
| [13] | Ius F, Natanov R, Salman J, et al. Extracorporeal membrane oxygenation as a bridge to lung transplantation may not impact overall mortality risk after transplantation: results from a 7-year single-centre experience[J]. Eur J Cardio Thorac Surg, 2018, 54(2): 334-340. DOI:10.1093/ejcts/ezy036 |
| [14] | Tipograf Y, Salna M, Minko E, et al. Outcomes of extracorporeal membrane oxygenation as a bridge to lung transplantation[J]. Ann Thorac Surg, 2019, 107(5): 1456-1463. DOI:10.1016/j.athoracsur.2019.01.032 |
| [15] | Deitz RL, Emerel L, Chan EG, et al. Waitlist mortality and extracorporeal membrane oxygenation bridge to lung transplant[J]. Ann Thorac Surg, 2023, 116(1): 156-162. DOI:10.1016/j.athoracsur.2023.02.062 |
| [16] | Ponholzer F, Schwarz S, Jaksch P, et al. Duration of extracorporeal life support bridging delineates differences in the outcome between awake and sedated bridge-to-transplant patients[J]. Eur J Cardio Thorac Surg, 2022, 62(3): ezac363. DOI:10.1093/ejcts/ezac363 |
| [17] | Kim NE, Woo A, Kim SY, et al. Long- and short-term clinical impact of awake extracorporeal membrane oxygenation as bridging therapy for lung transplantation[J]. Respir Res, 2021, 22(1): 306. DOI:10.1186/s12931-021-01905-7 |
| [18] | Wells CL, Forrester J, Vogel J, et al. Safety and feasibility of early physical therapy for patients on extracorporeal membrane oxygenator: university of Maryland medical center experience[J]. Crit Care Med, 2018, 46(1): 53-59. DOI:10.1097/ccm.0000000000002770 |
| [19] | Eden A, Purkiss C, Cork G, et al. In-patient physiotherapy for adults on veno-venous extracorporeal membrane oxygenation–United Kingdom ECMO Physiotherapy Network: a consensus agreement for best practice[J]. J Intensive Care Soc, 2017, 18(3): 212-220. DOI:10.1177/1751143717705801 |
| [20] | Jang MH, Shin MJ, Shin YB. Pulmonary and physical rehabilitation in critically ill patients[J]. Acute Crit Care, 2019, 34(1): 1-13. DOI:10.4266/acc.2019.00444 |
| [21] | Shah P, Neujahr DC. Lung transplantation: candidate selection and timing of transplant[J]. Curr Opin Organ Transplant, 2021, 26(3): 302-308. DOI:10.1097/mot.0000000000000879 |
| [22] | Biscotti M, Gannon WD, Agerstrand C, et al. Awake extracorporeal membrane oxygenation as bridge to lung transplantation: a 9-year experience[J]. Ann Thorac Surg, 2017, 104(2): 412-419. DOI:10.1016/j.athoracsur.2016.11.056 |
| [23] | Hoetzenecker K, Donahoe L, Yeung JC, et al. Extracorporeal life support as a bridge to lung transplantation–experience of a high-volume transplant center[J]. J Thorac Cardiovasc Surg, 2018, 155(3): 1316-1328.e1. DOI:10.1016/j.jtcvs.2017.09.161 |
| [24] | 陈静瑜, 毛文君, 杨柯佳, 等. 肺移植围手术期体外膜肺氧合应用指南(2019版)[J]. 器官移植, 2019, 10(4): 402-409. DOI:10.3969/j.issn.1674-7445.2019.04.009 |
| [25] | Na SJ, Jung JS, Hong SB, et al. Clinical outcomes of patients receiving prolonged extracorporeal membrane oxygenation for respiratory support[J]. Ther Adv Respir Dis, 2019, 13: 1753466619848941. DOI:10.1177/1753466619848941 |
| [26] | Bojic A, Schellongowski P, Robak O, et al. Long-term respiratory extracorporeal membrane oxygenation and prognosis: a retrospective analysis[J]. ASAIO J, 2021, 67(3): 345-352. DOI:10.1097/mat.0000000000001225 |
| [27] | Kipping V, Weber-Carstens S, Lojewski C, et al. Prone position during ECMO is safe and improves oxygenation[J]. Int J Artif Organs, 2013, 36(11): 821-832. DOI:10.5301/ijao.5000254 |
| [28] | Burket JS, Bartlett RH, Vander Hyde K, et al. Nosocomial infections in adult patients undergoing extracorporeal membrane oxygenation[J]. Clin Infect Dis, 1999, 28(4): 828-833. DOI:10.1086/515200 |
| [29] | Yamaguchi RS, Noritomi DT, Degaspare NV, et al. Peripherally inserted central catheters are associated with lower risk of bloodstream infection compared with central venous catheters in paediatric intensive care patients: a propensity-adjusted analysis[J]. Intensive Care Med, 2017, 43(8): 1097-1104. DOI:10.1007/s00134-017-4852-7 |
| [30] | 黄琳娜, 王一民, 黄絮, 等. 长程静脉-静脉体外膜式氧合救治重度急性呼吸窘迫综合征患者四例[J]. 中华结核和呼吸杂志, 2019, 42(8): 630-634. DOI:10.3760/cma.j.issn.1001-0939.2019.08.015 |
| [31] | MacLaren G, Combes A, Bartlett RH. Contemporary extracorporeal membrane oxygenation for adult respiratory failure: life support in the new era[J]. Intensive Care Med, 2012, 38(2): 210-220. DOI:10.1007/s00134-011-2439-2 |
| [32] | Ius F, Sommer W, Tudorache I, et al. Five-year experience with intraoperative extracorporeal membrane oxygenation in lung transplantation: Indications and midterm results[J]. J Heart Lung Transplant, 2016, 35(1): 49-58. DOI:10.1016/j.healun.2015.08.016 |
| [33] | da Nobrega Oliveira REN, Passos FS, Pessoa BM. Extracorporeal membrane oxygenation vs cardiopulmonary bypass in lung transplantation: an updated meta-analysis[J]. Gen Thorac Cardiovasc Surg, 2025, 73(3): 137-146. DOI:10.1007/s11748-024-02114-x |
| [34] | Ius F, Kuehn C, Tudorache I, et al. Lung transplantation on cardiopulmonary support: Venoarterial extracorporeal membrane oxygenation outperformed cardiopulmonary bypass[J]. J Thorac Cardiovasc Surg, 2012, 144(6): 1510-1516. DOI:10.1016/j.jtcvs.2012.07.095 |
| [35] | Dell'Amore A, Campisi A, Congiu S, et al. Extracorporeal life support during and after bilateral sequential lung transplantation in patients with pulmonary artery hypertension[J]. Artif Organs, 2020, 44(6): 628-637. DOI:10.1111/aor.13628 |
| [36] | 王宋, 刘敏, 许红阳. 体外膜肺氧合在肺移植手术中的应用进展[J]. 临床麻醉学杂志, 2023, 39(8): 863-867. DOI:10.12089/jca.2023.08.015 |
| [37] | Parikh AN, Merritt TC, Carvajal HG, et al. A comparison of cardiopulmonary bypass versus extracorporeal membrane oxygenation: Does intraoperative circulatory support strategy affect outcomes in pediatric lung transplantation?[J]. Clin Transplant, 2021, 35(6): e14289. DOI:10.1111/ctr.14289 |
| [38] | Pavlushkov E, Berman M, Valchanov K. Cannulation techniques for extracorporeal life support[J]. Ann Transl Med, 2017, 5(4): 70. DOI:10.21037/atm.2016.11.47 |
| [39] | Napp LC, Kühn C, Hoeper MM, et al. Cannulation strategies for percutaneous extracorporeal membrane oxygenation in adults[J]. Clin Res Cardiol, 2016, 105(4): 283-296. DOI:10.1007/s00392-015-0941-1 |
| [40] | Lorusso R. Are two crutches better than one? The ongoing dilemma on the effects and need for left ventricular unloading during veno-arterial extracorporeal membrane oxygenation[J]. European J Heart Fail, 2017, 19(3): 413-415. DOI:10.1002/ejhf.695 |
| [41] | 金宽哲, 胡春晓, 陈静瑜, 等. 肺移植围手术期ECMO动脉-静脉与静脉-静脉转流应用效果对比观察[J]. 山东医药, 2023, 63(13): 70-73. DOI:10.3969/j.issn.1002-266X.2023.13.017 |
| [42] | Assenzo V, Assenzo C, Filippo R, et al. The feasibility of extubation in the operating room after bilateral lung transplantation in adult emphysema patients: an observational retrospective study[J]. Eur J Cardio Thorac Surg, 2018, 54(6): 1128-1133. DOI:10.1093/ejcts/ezy196 |
| [43] | Samano MN, Fernandes LM, Baranauskas JCB, et al. Risk factors and survival impact of primary graft dysfunction after lung transplantation in a single institution[J]. Transplant Proc, 2012, 44(8): 2462-2468. DOI:10.1016/j.transproceed.2012.07.134 |
| [44] | Kreisel D, Krupnick AS, Puri V, et al. Short- and long-term outcomes of 1000 adult lung transplant recipients at a single center[J]. J Thorac Cardiovasc Surg, 2011, 141(1): 215-222. DOI:10.1016/j.jtcvs.2010.09.009 |
| [45] | Van Raemdonck D, Hartwig MG, Hertz MI, et al. Report of the ISHLT Working Group on primary lung graft dysfunction Part Ⅳ: Prevention and treatment: a 2016 Consensus Group statement of the International Society for Heart and Lung Transplantation[J]. J Heart Lung Transplant, 2017, 36(10): 1121-1136. DOI:10.1016/j.healun.2017.07.013 |
| [46] | Hoetzenecker K, Schwarz S, Muckenhuber M, et al. Intraoperative extracorporeal membrane oxygenation and the possibility of postoperative prolongation improve survival in bilateral lung transplantation[J]. J Thorac Cardiovasc Surg, 2018, 155(5): 2193-2206.e3. DOI:10.1016/j.jtcvs.2017.10.144 |
| [47] | Zenati M, Pham SM, Keenan RJ, et al. Extracorporeal membrane oxygenation for lung transplant recipients with primary severe donor lung dysfunction[J]. Transpl Int, 1996, 9(3): 227-230. DOI:10.1007/bf00335390 |
| [48] | Dahlberg PS, Prekker ME, Herrington CS, et al. Medium-term results of extracorporeal membrane oxygenation for severe acute lung injury after lung transplantation[J]. J Heart Lung Transplant, 2004, 23(8): 979-984. DOI:10.1016/j.healun.2003.08.021 |
| [49] | Marasco SF, Vale M, Preovolos A, et al. Institution of extracorporeal membrane oxygenation late after lung transplantation–a futile exercise?[J]. Clin Transplant, 2012, 26(1): E71-77. DOI:10.1111/j.1399-0012.2011.01562.x |
| [50] | Harano T, Ryan JP, Morrell MR, et al. Extracorporeal membrane oxygenation for primary graft dysfunction after lung transplantation[J]. ASAIO J, 2021, 67(9): 1071-1078. DOI:10.1097/mat.0000000000001350 |
| [51] | Liu MQ, Li XS, Xu B, et al. A retrospective analysis for risk factors and early prognosis of delayed withdrawal extracorporeal membrane oxygenation after lung transplantation[J]. Transplantation, 2021, 105(4): 867-875. DOI:10.1097/tp.0000000000003290 |
| [52] | Tonna JE, Bailey M, Abrams D, et al. Predictors of early mobilization in patients requiring VV ECMO for greater than 7 days: an international cohort study[J]. Heart Lung, 2023, 62: 57-63. DOI:10.1016/j.hrtlng.2023.05.022 |
| [53] | Marasco SF, Lukas G, McDonald M, et al. Review of ECMO (extra corporeal membrane oxygenation) support in critically ill adult patients[J]. Heart Lung Circ, 2008, 17: S41-S47. DOI:10.1016/j.hlc.2008.08.009 |
| [54] | 闵苏, 敖虎山. 不同情况下成人体外膜肺氧合临床应用专家共识(2020版)[J]. 中国循环杂志, 2020, 35(11): 1052-1063. DOI:10.3969/j.issn.1000-3614.2020.11.002 |
| [55] | Hoetzenecker K, Schwarz S, Muckenhuber M, et al. Intraoperative extracorporeal membrane oxygenation and the possibility of postoperative prolongation improve survival in bilateral lung transplantation[J]. J Thorac Cardiovasc Surg, 2018, 155(5): 2193-2206.e3. DOI:10.1016/j.jtcvs.2017.10.144 |
| [56] | Moser B, Jaksch P, Taghavi S, et al. Lung transplantation for idiopathic pulmonary arterial hypertension on intraoperative and postoperatively prolonged extracorporeal membrane oxygenation provides optimally controlled reperfusion and excellent outcome[J]. Eur J Cardio Thorac Surg, 2018, 53(1): 178-185. DOI:10.1093/ejcts/ezx212 |
| [57] | Mulvihill MS, Yerokun BA, Davis RP, et al. Extracorporeal membrane oxygenation following lung transplantation: indications and survival[J]. J Heart Lung Transplant, 2018, 37(2): 259-267. DOI:10.1016/j.healun.2017.06.014 |
| [58] | Mason DP, Boffa DJ, Murthy SC, et al. Extended use of extracorporeal membrane oxygenation after lung transplantation[J]. J Thorac Cardiovasc Surg, 2006, 132(4): 954-960. DOI:10.1016/j.jtcvs.2006.06.010 |
| [59] | Blakeslee-Carter J, Shao C, LaGrone R, et al. Vascular complications based on mode of extracorporeal membrane oxygenation[J]. J Vasc Surg, 2022, 75(6): 2037-2046.e2. DOI:10.1016/j.jvs.2022.01.078 |
| [60] | Hartwig MG, Appel JZ Ⅲ, Cantu E Ⅲ, et al. Improved results treating lung allograft failure with venovenous extracorporeal membrane oxygenation[J]. Ann Thorac Surg, 2005, 80(5): 1872-1880. DOI:10.1016/j.athoracsur.2005.04.063 |
| [61] | Warnecke G, Haverich A. Lung re-transplantation: review[J]. Curr Opin Organ Transplant, 2012, 17(5): 485-489. DOI:10.1097/mot.0b013e328357d8ba |
| [62] | Schaheen L, D′ Cunha J. Re-do lung transplantation: keys to success[J]. J Thorac Dis, 2019, 11(12): 5691-5693. DOI:10.21037/jtd.2019.12.104 |
| [63] | Inci I, Ehrsam JP, Van Raemdonck D, et al. Extracorporeal life support as a bridge to pulmonary retransplantation: prognostic factors for survival in a multicentre cohort analysis[J]. Eur J Cardio Thorac Surg, 2022, 61(2): 405-412. DOI:10.1093/ejcts/ezab514 |
| [64] | Porteous MK, Ky B, Kirkpatrick JN, et al. Diastolic dysfunction increases the risk of primary graft dysfunction after lung transplant[J]. Am J Respir Crit Care Med, 2016, 193(12): 1392-1400. DOI:10.1164/rccm.201508-1522oc |
| [65] | Tudorache I, Sommer W, Kühn C, et al. Lung transplantation for severe pulmonary hypertension: awake extracorporeal membrane oxygenation for postoperative left ventricular remodelling[J]. Transplantation, 2015, 99(2): 451-458. DOI:10.1097/tp.0000000000000348 |
| [66] | Augoustides JGT, Ochroch EA. Assessment of intracardiac shunts[J]. Int Anesthesiol Clin, 2008, 46(2): 83-103. DOI:10.1097/aia.0b013e31806add4a |
| [67] | González-Fernández C, González-Castro A, Rodríguez-Borregán JC, et al. Pulmonary venous obstruction after lung transplantation. Diagnostic advantages of transesophageal echocardiography[J]. Clin Transplant, 2009, 23(6): 975-980. DOI:10.1111/j.1399-0012.2009.01078.x |
| [68] | Cartwright BL, Jackson A, Cooper J. Intraoperative pulmonary vein examination by transesophageal echocardiography: an anatomic update and review of utility[J]. J Cardiothorac Vasc Anesth, 2013, 27(1): 111-120. DOI:10.1053/j.jvca.2012.06.019 |
| [69] | Abrams BA, Melnyk V, Allen WL, et al. TEE for lung transplantation: a case series and discussion of vascular complications[J]. J Cardiothorac Vasc Anesth, 2020, 34(3): 733-740. DOI:10.1053/j.jvca.2019.09.005 |
| [70] | Benazzo A, Schwarz S, Frommlet F, et al. Twenty-year experience with extracorporeal life support as bridge to lung transplantation[J]. J Thorac Cardiovasc Surg, 2019, 157(6): 2515-2525.e10. DOI:10.1016/j.jtcvs.2019.02.048 |
| [71] | Lansink-Hartgring AO, van der Bij W, Verschuuren EA, et al. Extracorporeal life support as a bridge to lung transplantation: a single-center experience with an emphasis on health-related quality of life[J]. Respir Care, 2017, 62(5): 588-594. DOI:10.4187/respcare.05300 |
| [72] | Toyoda Y, Bhama JK, Shigemura N, et al. Efficacy of extracorporeal membrane oxygenation as a bridge to lung transplantation[J]. J Thorac Cardiovasc Surg, 2013, 145(4): 1065-1071. DOI:10.1016/j.jtcvs.2012.12.067 |
| [73] | Biscotti M, Sonett J, Bacchetta M. ECMO as bridge to lung transplant[J]. Thorac Surg Clin, 2015, 25(1): 17-25. DOI:10.1016/j.thorsurg.2014.09.010 |
| [74] | Kolaitis NA, Barnes H, Levine DJ, et al. Approach to lung transplantation in pulmonary arterial hypertension: a Delphi consensus on behalf of the transplant task force of the pulmonary vascular research institute[J]. Pulm Circ, 2025, 15(2): e70088. DOI:10.1002/pul2.70088 |
| [75] | Nasir BS, Klapper J, Hartwig M. Lung transplant from ECMO: current results and predictors of post-transplant mortality[J]. Curr Transplant Rep, 2021, 8(2): 140-150. DOI:10.1007/s40472-021-00323-4 |
| [76] | Shah PR, Boisen ML, Winger DG, et al. Extracorporeal support during bilateral sequential lung transplantation in patients with pulmonary hypertension: risk factors and outcomes[J]. J Cardiothorac Vasc Anesth, 2017, 31(2): 418-425. DOI:10.1053/j.jvca.2016.08.021 |
| [77] | Jack T, Carlens J, Diekmann F, et al. Bilateral lung transplantation for pediatric pulmonary arterial hypertension: perioperative management and one-year follow-up[J]. Front Cardiovasc Med, 2023, 10: 1193326. DOI:10.3389/fcvm.2023.1193326 |
| [78] | Reeb J, Falcoz PE, Santelmo N, et al. Double lumen bi-Cava cannula for veno-venous extracorporeal membrane oxygenation as bridge to lung transplantation in non-intubated patient[J]. Interact CardioVascular Thorac Surg, 2012, 14(1): 125-127. DOI:10.1093/icvts/ivr046 |
| [79] | Chimot L, Marqué S, Gros A, et al. Avalon? bicaval dual-lumen Cannula for venovenous extracorporeal membrane oxygenation: survey of Cannula use in France[J]. ASAIO J, 2013, 59(2): 157-161. DOI:10.1097/mat.0b013e31827db6f3 |
| [80] | 杨冰心, 李敏, 周蓉, 等. 围手术期无抗凝体外膜肺氧合辅助肺移植治疗8例分析[J]. 器官移植, 2018, 9(2): 152-155. DOI:10.3969/j.issn.1674-7445.2018.02.011 |
| [81] | Jiritano F, Serraino GF, ten Cate H, et al. Platelets and extra-corporeal membrane oxygenation in adult patients: a systematic review and meta-analysis[J]. Intensive Care Med, 2020, 46(6): 1154-1169. DOI:10.1007/s00134-020-06031-4 |
| [82] | Kurihara C, Walter JM, Karim A, et al. Feasibility of venovenous extracorporeal membrane oxygenation without systemic anticoagulation[J]. Ann Thorac Surg, 2020, 110(4): 1209-1215. DOI:10.1016/j.athoracsur.2020.02.011 |
| [83] | Scaravilli V, Fumagalli J, Rosso L, et al. Heparin-free lung transplantation on venovenous extracorporeal membrane oxygenation bridge[J]. ASAIO J, 2021, 67(11): e191-e197. DOI:10.1097/mat.0000000000001371 |
| [84] | Vajter J, Holubova G, Novysedlak R, et al. Anaesthesiologic considerations for intraoperative ECMO anticoagulation during lung transplantation: a single-centre, retrospective, observational study[J]. Transpl Int, 2024, 37: 12752. DOI:10.3389/ti.2024.12752 |
| [85] | Mazzeffi MA, Tanaka K, Roberts A, et al. Bleeding, thrombosis, and transfusion with two heparin anticoagulation protocols in venoarterial ECMO patients[J]. J Cardiothorac Vasc Anesth, 2019, 33(5): 1216-1220. DOI:10.1053/j.jvca.2018.07.045 |
| [86] | Mazzeffi M, Rabin J, Deatrick K, et al. Platelet transfusion and in-hospital mortality in veno-arterial extracorporeal membrane oxygenation patients[J]. ASAIO J, 2022, 68(10): 1249-1255. DOI:10.1097/mat.0000000000001643 |
| [87] | Yaw HP, Van Den Helm S, MacLaren G, et al. Platelet phenotype and function in the setting of pediatric extracorporeal membrane oxygenation (ECMO): a systematic review[J]. Front Cardiovasc Med, 2019, 6: 137. DOI:10.3389/fcvm.2019.00137 |
| [88] | Jacob S, Lima B, Gonzalez-Stawinski GV, et al. Extracorporeal membrane oxygenation as a salvage therapy for patients with severe primary graft dysfunction after heart transplant[J]. Clin Transplant, 2019, 33(5): e13538. DOI:10.1111/ctr.13538 |
| [89] | Lamb K, Cowan SW, Evans N, et al. Successful management of bleeding complications in patients supported with extracorporeal membrane oxygenation with primary respiratory failure[J]. Perfusion, 2013, 28(2): 125-131. DOI:10.1177/0267659112464096 |
| [90] | Figueroa Villalba CA, McMullan DM, Reed RC, et al. Thrombosis in extracorporeal membrane oxygenation (ECMO) circuits[J]. ASAIO J, 2022, 68(8): 1083-1092. DOI:10.1097/mat.0000000000001605 |
| [91] | 龙村. 体外膜肺氧合循环支持专家共识[J]. 中国体外循环杂志, 2014, 12(2): 65-67. DOI:10.13498/j.cnki.chin.j.ecc.2014.02.01 |
| [92] | Abrams D, MacLaren G, Lorusso R, et al. Extracorporeal cardiopulmonary resuscitation in adults: evidence and implications[J]. Intensive Care Med, 2022, 48(1): 1-15. DOI:10.1007/s00134-021-06514-y |
| [93] | Lorusso R, Whitman G, Milojevic M, et al. 2020 EACTS/ELSO/STS/AATS expert consensus on post-cardiotomy extracorporeal life support in adult patients[J]. Eur J Cardio Thorac Surg, 2021, 59(1): 12-53. DOI:10.1093/ejcts/ezaa283 |
| [94] | Guglin M, Zucker MJ, Bazan VM, et al. Venoarterial ECMO for adults[J]. J Am Coll Cardiol, 2019, 73(6): 698-716. DOI:10.1016/j.jacc.2018.11.038 |
| [95] | Levy D, Saura O, Passarelli MT, et al. Thrombolysis before venoarterial ECMO for high-risk pulmonary embolism: a retrospective cohort study[J]. Intensive Care Med, 2024, 50(8): 1287-1297. DOI:10.1007/s00134-024-07501-9 |
| [96] | Bali AD, Sharma T, Villela MA, et al. Interventional therapies and mechanical circulatory support for acute pulmonary embolism[J]. J Card Fail, 2024, 30(10): 1319-1329. DOI:10.1016/j.cardfail.2024.07.012 |
| [97] | Chandel A, Patolia S, Looby M, et al. Association of D-dimer and fibrinogen with hypercoagulability in COVID-19 requiring extracorporeal membrane oxygenation[J]. J Intensive Care Med, 2021, 36(6): 689-695. DOI:10.1177/0885066621997039 |
| [98] | Taguchi A, Kai S, Kimura K, et al. Intraoperative diagnosis of bronchovenous fistula during lung transplantation using transesophageal echocardiography[J]. J Cardiothorac Vasc Anesth, 2022, 36(8): 2572-2574. DOI:10.1053/j.jvca.2021.09.015 |
| [99] | Sunder T, Thangaraj PR, Kuppusamy MK. Venous thromboembolism following lung transplantation[J]. World J Transplant, 2025, 15(2): 99241. DOI:10.5500/wjt.v15.i2.99241 |
| [100] | Bonicolini E, Martucci G, Simons J, et al. Limb ischemia in peripheral veno-arterial extracorporeal membrane oxygenation: a narrative review of incidence, prevention, monitoring, and treatment[J]. Crit Care, 2019, 23(1): 266. DOI:10.1186/s13054-019-2541-3 |
| [101] | Wheeler CR, Bullock KJ. Extracorporeal membrane oxygenation[J]. Respir Care, 2023, 68(8): 1158-1170. DOI:10.4187/respcare.10929 |
 2026, Vol. 35
2026, Vol. 35