肺移植是终末期肺病成熟的治疗手段。近年来在我国开展数量持续增长。据《中国器官捐献和移植发展报告(2023)》统计,自2015年以来,我国累计肺移植手术近6 000例,成人受体术后30 d存活率为83.6%,30 d内主要死亡原因为多脏器功能衰竭(29.4%)、感染(17.5%)、失血性休克(11.1%)和原发性移植物功能障碍(primary graft dysfunction, PGD)(6.3%)等[1],因此,围术期管理对于肺移植患者生存预后至关重要。
肺移植手术复杂,术后并发症风险高,加之我国肺移植患者中老年患者比例高,60岁以上患者占47.8%,常合并多系统基础疾病,且普遍存在就医延迟、病情复杂等特点,这使围术期管理面临更多挑战。通过规范围移植监护管理,制定个体化的综合治疗方案,包括呼吸支持、血流动力学稳定、镇痛镇静、感染防控、营养支持等,可以提高围术期生存率[2-3]。
目前,国内在肺移植围术期重症管理方面尚缺乏系统、统一的专业指南,不同中心实践存在差异,部分环节缺乏循证依据。为提升管理水平,推动标准化建设,我们采用德尔菲法,汇聚国内专家意见,结合最新循证研究与临床经验,制定本指南。旨在为肺移植术后监护管理提供科学、规范、切实可行的实践参考,提升整体治疗质量,改善患者结局。
来自全国的肺移植科、重症医学科(intensive care unit, ICU)、麻醉科、呼吸及危重症医学科、护理等多学科的专家共同组成工作组,参与本指南的制定和撰写。工作组分为:(1)指南指导组,负责整体设计、组织专家、计划监督等;(2)指南专家组,确定临床问题,确定文献纳入人群、干预措施、对照和结局,并为初稿的撰写提供意见等;(3)方法学组,负责方法学质控、文献检索、证据整理、质量评价等;(4)执笔者,进行共识文章的撰写;(5)指南秘书组,负责专家联络、整体执行等。采用德尔菲法确定指南涵盖的临床问题,主要包括肺移植围术期呼吸、循环、感染、肾脏、营养等板块问题。本指南已在国际实践指南注册与透明化平台(Practice Guide Registration for TransPAREncy, PREPARE)上以中英双语注册(PREPARE-2024CN402)。
根据临床问题进行证据检索和文献筛选,指南制定小组全面检索了PubMed、EMBASE、Web of Science、Cochrane图书馆、中国知网数据库和万方数据知识服务平台等,以“lung transplantation”结合“perioperative management”,“intensive care”,“multidisciplinary collaboration”,“mechanical ventilation”,“hemodynamic monitoring”等相关关键词,检索文献1 200余篇,人工筛选出145篇与主题密切相关的研究或综述进行总结,最终凝练肺移植围术期管理问题13个,共33条推荐意见。此外,汇总肺移植患者入ICU后第一个小时集束化监测内容及每日监护项目清单,以供参考,具体总结见表 1和表 2。
| 监测系统 | 监测内容 |
| 生命体征 | 体温、心率、脉搏、血压、中心静脉压、外周血氧饱和度、瞳孔、肺动脉楔压、胸腔引流量、尿量 |
| 检验指标 | 血气分析、血常规、肝肾功能、心肌酶谱、凝血功能、血栓弹力图、感染指标(C-反应蛋白、降钙素原、肝素结合蛋白、白介素-6等) |
| 检查项目 | 心电图、床边胸片、纤支镜、超声心动图 |
| 机械通气 | 气囊压力、气管插管深度、呼吸机参数(氧体积分数,潮气量,PEEP,气道峰压和平台压)、肺顺应性 |
| ECMO | 管路位置、渗血情况、转速/流量、ACT |
| 脏器/功能 | ICU每日监测项目 |
| 肺脏 | 肺部体征、胸腔引流(量、性状、常规、生化、培养)、手术切口、呼吸机、外周氧饱和度、血气分析(PaO2、PaCO2)、胸片、肺部超声、纤支镜、PICCO(EVLW) |
| 神经 | 神志、GCS、瞳孔、镇痛镇静药物、动态脑电监测、经颅多普勒超声 |
| 循环 | 水肿(结膜、低垂部位)、血压、中心静脉压、肺动脉楔压、Pro-BNP/BNP、乳酸、心肌酶谱、心电图、超声心动图、下腔静脉/颈静脉充盈程度、PICCO(CO、dPmax、GEDV、PVPI等)、血管活性药物 |
| 感染 | 体温、痰液性状、感染指标(白细胞计数、中性细胞比例、C-反应蛋白、降钙素原、白介素-6等)、内毒素、供+受体培养结果(痰、血、尿、粪)、G+GM试验、巨细胞/EB病毒抗体+DNA、血/肺泡灌洗液NGS、抗生素方案 |
| 免疫 | 激素用量、FK506浓度/剂量、淋巴细胞绝对值、细胞免疫+体液免疫状态 |
| 肾脏 | 每小时尿量、肌酐、尿素氮、血清胱抑素、血气分析(pH、BE、HCO3-)、电解质、血/尿渗透压、内生肌酐清除率、肾脏损害药物 |
| 肝脏 | 皮肤颜色、腹部体征、肝功能(胆红素和肝酶指标)、肝损药物、乙肝病毒抗体+DNA |
| 凝血 | 皮肤出血点、隐血试验(胃内容物、粪便)、凝血谱、血栓弹力图、抗凝药物 |
| 营养 | 腹部体征、腹内压、粪便性状、BMI、血糖、胰岛素使用量、前白蛋白、视黄醇结合蛋白、转铁蛋白、饮水试验、热卡摄入(进食、肠内营养、肠外营养)、营养代谢车 |
| 康复 | 四肢肌力、咳嗽反射、膈肌厚度和活动度(拔管后) |
| 管路 | 动脉置管、PICCO、肺动脉导管、深静脉置管、CRRT置管、ECMO置管、气管插管、胃管、鼻肠管、导尿管、胸腔引流管、外周静脉置管、PICC管 |
推荐意见1:建议根据医院实际结构,建立以重症医学科为核心,联合肺移植科、麻醉科、呼吸及危重症医学科、康复医学科、临床免疫科、临床营养科及专科护理团队的多学科协作模式(MDT),共同参与肺移植围手术期患者的管理和决策。(推荐强度D,证据等级5)
推荐说明:对于终末期肺病患者,在其他治疗失败时,肺移植是最有效的治疗选择。但肺移植手术复杂,术后管理难度高于其他实体器官移植。加拿大多伦多移植中心建议组建专门的多学科团队,以优化肺移植受者ICU住院期间复杂的术后管理[2]。在日本,对于复杂的肺移植术后管理,提倡应充分利用心脏和胸外科专家的经验、技术和专业知识[4]。我国肺移植起步较晚,肺移植围术期专业团队的管理经验相对缺乏。
肺移植围术期管理涉及多阶段、多学科的复杂协作,包括从麻醉科至ICU,再过渡至肺移植专科、呼吸及危重症医学科及胸外科普通病房的全流程。各科室职责并非彼此独立,尤其在术后关键时期,多学科团队(multidisciplinary team, MDT)协作对于全面把握患者病情变化、及时处理并发症以及建立稳固的医患信任关系至关重要。尽管围术期患者病情监测与处理多由ICU医师主导,但外科团队在手术相关并发症防治方面更具专业优势,而内科团队亦应早期参与,为后续接收患者做好准备。此外,建议在患者列入肺移植等待名单前,ICU团队即应提前介入,评估其脏器功能、康复潜力及心理状态,为可能发生的围术期并发症做好预案准备[5]。
2 肺移植围术期外科并发症处理要点?推荐意见2:术后出血,可疑的肺动脉狭窄、梗阻、扭曲、肺静脉梗阻、肺扭转等外科并发症,应加强早期识别诊断,必要时手术干预。(推荐强度B,证据等级2b)
推荐说明: 肺移植围术期外科并发症往往起病迅速,病情凶险,应积极组织多学科讨论,尽快明确处理方案。术后出血曾是肺移植术后早期最为常见的并发症之一。在肺移植技术开展初期,出血情况较为普遍,据统计,约四分之一接受体外循环下双肺移植的患者需要再次手术止血。随着术式改进,采用后外侧切口进行单肺移植以及蛤壳式切口进行双肺移植,显著改善了术野暴露并减少了术中出血。另外,术中采用体外膜肺氧合(extracorporeal membrane oxygenation, ECMO)替代传统体外循环进行血流动力学支持,因肝素用量减少,也在一定程度上降低了术中及术后出血的风险[6]。
肺移植术后血管吻合口并发症的发生率约为1.75%[7],可发生于肺动脉或心房吻合口处。常见原因包括供体与受体血管尺寸不匹配、吻合技术问题、血管扭转或血栓形成等,其中肺动脉相关并发症更为常见。肺动脉走向不良、吻合口狭窄或血管过长导致的扭曲均可能引发此类问题。若术后患者出现原因不明的低氧血症或肺水肿表现,应高度怀疑是否存在血管吻合问题,建议进行胸部CT、肺灌注显像及血管造影等评估。此外,术中应用经食管超声心动图(transesophageal echocardiography, TEE)检查对早期识别血管并发症具有重要价值。
推荐意见3:肺移植术后吻合口并发症(如裂开、瘘口形成、狭窄等)的处理需根据发生时间、类型及严重程度个体化选择干预方案,围术期优先考虑手术修复,在此基础上,结合调整呼吸机参数、积极抗感染治疗,以及在必要时谨慎气道介入治疗,以控制局部损害。(推荐强度B,证据等级2a)
推荐说明:肺移植术后气道并发症发生时点各异。吻合口瘘(包括支气管胸膜瘘、支气管纵隔瘘及支气管血管瘘)属急性病变,可发生于移植术后任何阶段。相对而言,吻合口软化和狭窄多呈慢性病变,一般见于术后数月,少数可自围术期起迁延不愈。
术后早期出现的吻合口裂开或瘘,病死率高,但早期感染率较低,且手术修复成功率较高,建议外科积极评估干预。对于术后数月出现的并发症,多与持续正压通气、血管活性药物致吻合口缺血或反复病原菌感染等相关,需要综合处理,包括适当降低正压通气条件,甚至尝试强制脱机,并强化抗感染治疗与体位引流。多项回顾性研究证实,对于症状不明显或裂开较小的患者,可考虑支气管镜下置入短期金属支架介入覆盖缺口,同时强化营养治疗,促进缺口的愈合[8]。但需要注意的是,支架需要在适当时机取出,一旦新生肉芽组织覆盖,可能会加速形成狭窄,在取出时加重出血风险。避免不必要的支架置入,是临床医生需要多方面衡量的内容[9]。支气管胸膜瘘伴随脓胸患者需加强穿刺引流,必要时冲洗,手术处理包括直接缝合加皮瓣加强、经胸骨支气管闭合或胸廓成形术。支气管纵隔瘘如内科抗感染治疗无效可考虑纵隔清创。而支气管血管瘘,只在个别病例中成功地进行了肺叶切除和全肺切除手术。
3 肺移植围术期机械通气管理的要点有哪些?推荐意见4:建议术后保护性通气策略,包括限制潮气量(≤6 mL/kg)、控制平台压(≤30 cm2, 1 cm2=0.098 kPa)、维持适当呼气末正压。通气参数建议基于供体的理想体重设定,关注患者预测总肺活量(pTLC)比值,以减少肺损伤风险。(推荐强度B,证据等级2a)
推荐说明: 肺移植术后机械通气需按照患者特点调整呼吸机参数。鉴于小潮气量在急性呼吸窘迫患者的成功应用,肺保护性通气策略也适用于肺移植术后患者[10-12]。具体策略包括:限制潮气量≤6 mL/kg(供肺的预测理想体重),控制平台压≤30 cm2,维持氧饱和度>90%和pH>7.25下尽可能降低氧体积分数,维持呼气末正压(positive end expiratory pressure, PEEP)5~10 cm2(不超过12 cm2),允许性高碳酸血症。避免高压力通气能减少气压伤和支气管吻合口并发症。此外,肺保护性通气策略也是治疗PGD的重要手段[12]。
当移植肺存在减容、翻转,或供受体不匹配时,需根据供体肺大小动态调整呼吸机参数以获得更合适的功能状态[13],预测总肺活量(pTLC)比值(供体总肺活量/受体总肺活量)是需要考虑的变量[14]。Eberlein等开展的一项基于812名患者的多中心回顾性研究发现,供受体不匹配时,pTLC>1可能和更低的PGD发生率相关[14]。若供体肺体积偏小,仍依据受体参数设定潮气量,也可能增加PGD的发生风险[15];而采用基于供体理想体重设定的保护性通气策略,则可降低术后48~72 h内重度PGD的发生率,并有助于改善患者1年生存率[16]。
推荐意见5:建议术后尽早评估肺功能状态,在具备拔管条件的情况下,尽早撤机。拔管前应完善胸部影像(如X线或CT)、动脉血气分析、支气管镜检查等综合评估,以确保肺复张充分、气道通畅、氧合和通气功能稳定。反复撤机失败的患者,可尽早评估气管切开。(推荐强度B,证据等级2b)
推荐说明:肺移植术后的早期拔管能够使患者获益,大部分移植后没有通气困难的患者,可在术后数小时至数日内撤离呼吸机。Beer等的国际性横断面调查研究发现,85%的肺移植中心机械通气持续时间为48 h,其中32%在24 h内脱机[7]。部分患者因早期并发症可考虑延迟撤机,包括PGD、原发性肺动脉高压、严重出血、严重心律失常、急性肺部感染、吻合口和胸膜并发症、肺外器官功能衰竭等[17-20]。
建议机械通气撤离的具体标准包括:①受体肺功能恢复,床边纤维支气管镜提示气道壁水肿改善、无明显或极少量水肿,胸片提示肺部无渗出或渗出明显减少且PGD风险较低。②肺移植术后早期允许一定程度高碳酸血症(pH>7.25)。③氧合指数:PaO2/FiO2>200 mmHg[2]。④血流动力学稳定,无明显低血压[不需要或小剂量血管活性药物,如多巴胺或多巴酚丁胺<5~10 μg/(kg·min),去甲肾上腺素<0.1 μg/(kg·min)]。此外,拔管前应进行支气管镜检查,评估支气管吻合情况,清除气道黏液、淤血和分泌物。前瞻性多中心观察研究发现,供体机械通气动态顺应性及受体通气参数(包括吸气峰压和氧合指数)可预测机械通气时长,亦可为撤机提供参考[21-22]。
对于病程长,全身情况差的患者,必须预料到中长程的机械通气时间。在这种情况下,早期气管切开术是需要考虑的。此外,对于反复撤机失败的患者,也可尽早评估气管切开。Feltracco等[23]学者对126例肺移植患者进行回顾性分析,气管切开占比24.6%(31例),其中27例是在肺移植术后8 d内完成的,术后早期未见气胸、纵隔气肿、低血压、低氧血症或心律失常。Miyoshi等[24]开展的另一项研究中,患者气切的选择更加积极,他们将早期气管切开定义为术后3 d,数据表明相较于延迟气管切开,肺移植后的早期气管切开允许患者更早开始行走和经口进食,缩短了ICU住院时间和总住院时间,和未气切患者相比,二者住院时间亦无明显区别。
推荐意见6:对拔管后的患者,针对不同病种及术前状态个体化选择无创通气(NIV)及经鼻高流量湿化氧疗(HFNC)作为过渡支持手段,以降低再插管风险,对于存在肺动脉高压、膈肌功能障碍或心功能不全的患者,优先选择短期无创通气,具体选择应基于个体病情评估。(推荐强度B,证据等级2a)
推荐说明:无创机械通气(non-invasive mechanical ventilation, NIV)是一种常见的拔除气管插管后的过渡通气方式,在心肺手术围术期应用较多。研究证实其能够有效降低再次插管的风险[25-27]。其主要的益处包括:缓解呼吸肌疲劳、降低呼吸频率、缓解呼吸困难及改善通气/血流比值异常。肺移植术后膈神经损伤的发生率较高,NIV有助于改善术后膈神经功能障碍,预防术后气道损伤和感染。同时NIV也能够在俯卧位时进行有效的呼吸机支持。因此,序贯NIV脱机有利于术后肌力恢复,也有利于移植肺复张。但需要警惕的是,无法完全配合的NIV可能会造成吻合口损伤、气压伤,临床需关注患者配合程度,综合评估[28-29]。
经鼻高流量湿化氧疗(high-flow nasal cannula oxygen therapy,HFNC)是一种应用越来越广泛的氧疗方式。大量的研究指出,对于急性呼吸衰竭、拔管后过渡、心脏及胸腔手术后严重低氧血症患者,HFNC在降低插管率上优于常规氧疗,但和NIV相比并无明显优势[30-31]。HFNC能提高患者的肺泡通气量、减少呼吸功,并能够降低无效腔,同时具有加温和湿化功能,对比NIV更加舒适,耐受性好,避免腹胀、吸入性肺炎等。同时HFNC也有局限性,包括气道压不恒定,张口时效果下降等。
推荐意见7:对于单肺移植术后患者,尤其合并慢性阻塞性肺疾病(COPD)者,应高度警惕急性自体肺过度通气综合征(ANLH)。建议避免使用高PEEP,鼓励早期拔管。对于严重自体肺过度通气可在严格监测下短期试用差异性肺通气(DLV)改善氧合,但需权衡其可能延长机械通气时间的风险,临床决策需个体化评估。(推荐强度B,证据等级2b)
推荐说明:单肺移植术后,移植肺和自体肺有不同的顺应性,当两肺以相同的压力通气时,一侧肺过度膨胀,而另一侧肺可能膨胀不全。对于间质性肺病患者,移植肺膨胀比自体肺显著,有利于通气改善,但对于慢性阻塞性肺病(chronic obstructive pulmonary disease, COPD)患者,单肺移植后由于自体肺的顺应性好,保障移植肺进行充分气体交换的通气量即可导致自体肺过度膨胀,因纵隔移位、静脉回流和心输出量减少引起循环波动,甚至需要血管活性药物维持,该疾病被称为急性自体肺过度通气综合征(acute native lung hyperinflation, ANLH)[32-33]。明显的纵隔移位导致移植肺受压,导致肺不张、低氧血症和高碳酸血症。对于COPD或肺气肿单肺移植患者,术后不应使用PEEP,或者应限定在较低的压力(<5 cmH2O),有证据表明,术后早期甚至在手术室拔管可使这部分患者获益,能够最大限度地减少过度通气,缩短总体住院时间[33]。
差异性肺通气(differential lung ventilation, DLV)可通过独立调控双侧肺通气参数,适应单肺移植术后自体肺与移植肺在气道阻力及顺应性方面的差异。其常用技术包括双腔支气管插管(double-lumen tube, DLT)及双呼吸机辅助通气。前者易发生导管移位、引流不畅及气道阻力增高,常需深度镇静或肌松;后者操作复杂,临床成功率有待进一步验证。有支持性研究显示,DLV可迅速改善氧合,尤其在自体肺/移植肺动态顺应性比≥2.69时更具应用价值;但也有研究提示DLV可能延长机械通时间和ICU住院时间,并未显著改善短期病死率[34]。除肺减容手术外,单向支气管内瓣膜(endobronchial valve, EBV)通过选择性肺叶隔绝与气体吸收实现靶区减容,亦可用于极度肺过度充气的介入治疗。综上,目前差异性双肺通气仍缺乏高质量的研究依据,但极少数患者可能通过支气管内单向活瓣及肺减容手术获益。
推荐意见8:术后脱机困难的患者,需高度关注膈肌功能状况。推荐采用床旁超声评估膈肌厚度及活动度,以判断是否存在膈肌功能障碍,并据此调整撤机策略。(推荐强度B,证据等级2a)
推荐说明:肺移植术后脱机困难是多因素的,需要从肺内和肺外因素考虑,其中,膈肌功能障碍作为常见的术后并发症,需引起重视[35-37]。有研究指出约60%~80%的机械通气患者合并不同程度的膈肌功能障碍,其发生率是四肢肌力下降的两倍[38-40]。此类患者可能出现一过性或永久性呼吸衰竭,呼吸形态异常,自主咳痰能力持续无法恢复等[38-39]。膈肌功能不良作为ICU获得性肌无力的临床表现之一,存在术后导致机械通气时间延长的风险,而呼吸机的延迟撤离又会反向加重膈肌功能障碍,形成恶性循环[41-42]。除常规X线透视、CT等检查,膈肌超声作为一种安全、无辐射、非侵入性和广泛可用的技术,已被临床接受[40, 43]。膈肌超声提供两种主流的描述膈肌功能的方法——膈肌厚度(Tdi)/增厚分数(TFdi)和膈肌活动度(EXdi)。通常用于诊断膈肌功能障碍的两个指标包括Tdi值<2 mm和膈肌增厚分数(TFdi)值<20%[39]。膈肌活动度中定义吸气期间的膈肌运动,<1cm提示撤机失败,而膈肌移动度与呼吸频率之比(>1.3次/min/mm)比浅快呼吸指数能够更好地预测撤机[38, 43]。
4 肺移植围术期早期气道管理的要点是什么?推荐意见9:建议在术后尽早常规行支气管镜检查,以评估气道出血、水肿及吻合口的完整性,发现早期异常征象,及时清除气道分泌物、血凝块等,并留取肺泡灌洗液。(推荐强度B,证据等级2a)
推荐说明:肺移植术后24 h内应尽早行支气管镜检查,以评估气道吻合口完整性及是否存在水肿、缺血、狭窄或裂开等异常[44-45]。此外,应重点评估气道黏膜状态,早期发现出血或排异征象,并清除气道血凝块及分泌物,同期留取肺泡灌洗液送检常规和微生物学检查,以指导后续后续抗生素使用。如气道内分泌大量稀薄水样痰,需警惕缺血-再灌注损伤,通过严格液体管理可在次日迅速改善。若症状持续,应排除PGD或急性排斥反应等可能性,并考虑进一步处理。考虑到术后支气管情况的变化,建议建立专门的图像库方便调取对比,明确是否需要早期介入治疗等。
5 如何强化肺移植术后血流动力学监测与管理?推荐意见10:推荐术后加强Swan-Ganz导管、脉搏指示连续心输出量监测(PICCO)及超声心动图等监测,根据肺动脉压力(PAP)、中心静脉压(CVP)、平均动脉压(MAP)、心脏指数(CI)、尿量等多参数进行血流动力学评估,必要时应用TEE。术后早期实施限制性液体管理策略,以降低PGD及其他原因导致的肺水肿的发生风险。(推荐强度B,证据等级2b)
推荐说明:肺移植围手术期液体超负荷会增加PGD及心功能衰竭风险,因此,目前推荐目标导向性液体策略46,在维持稳定的血流动力学和充分的组织灌注下尽可能减少液体入量[2]。当前重症患者的血流动力学监测与组织灌注评估手段较多,包括血压、尿量、乳酸、中心静脉压(central venous pressure, CVP)、Swan-Ganz导管、脉搏指示连续心输出量监测(pulse indicator continous cadiac output, PICCO)、床旁超声等。推荐多模态血流动力学监测,每日监测如下:①早期每日进行床边纤维支气管镜检查,评估支气管水肿充血程度;②早期每日床边胸片评估双肺渗出情况;③床边超声评估胸腔内肺部B线、心脏充盈程度、下腔静脉和颈内静脉宽度和变异度;④每日观察患者结膜水肿、肺部听诊、肠鸣音、引流液性状、低垂部位和下肢水肿,并通过尿量颜色、尿比重、红细胞压积等评估患者容量状态;⑤有条件的中心建议早期应用Swan-Ganz导管及PICCO动态监测容量和心脏功能,具体涵盖肺动脉楔压(pulmonary artery wedge pressure, PAWP)、脉压变异度(pulse pressure variation, PPV)、每搏量变异度(stroke volume variation, SVV)等,此外,作为组织灌注的核心决定因素,对高危患者需积极评估与优化心输出量(cardiac output, CO)[46-47]。此外,TEE在肺移植围术期也具有重要价值,可用于评估血管吻合质量、指导液体复苏及血流动力学管理,已获美国超声心动图学会推荐,但其在连续实时监测方面仍存在一定局限[48-49]。推荐肺移植术后早期容量目标如下:①平均动脉压(mean arterial pressure, MAP)65~75 mmHg;②心脏指数(cardiac index, CI)2.2~2.5 L/min/m2;③CVP < 7 mmHg(9.5 cm2);④PAWP < 10 mmHg;⑤尿量 > 0.5 mL/(kg·h)。
推荐意见11:术后出现的血流动力学不稳定,应依据发生时期优先鉴别病因:早期重点评估再灌注损伤、容量状态及心功能;中后期需警惕感染性休克。强调通过有创血流动力学监测指导个体化治疗。(推荐强度B,证据等级2a)
推荐说明:肺移植术后患者休克的鉴别相对复杂,不同时期休克类型各有侧重。术后早期休克可能与再灌注损伤导致的炎症因子级联反应,导致全身毛细血管渗漏,引起有效循环容量不足相关[50]。此时休克可能伴随着PGD出现,随着炎症介质的清除,休克可在48~72 h内纠正。其他可能因素还包括限制性补液、镇静药物导致相对容量不足,部分与心律失常、应激性心肌病、心肌梗死等心源性休克相关。少数患者可能出现急性感染,引起脓毒症和感染性休克。当患者休克存在多种因素无法鉴别时,可通过有创血流动力学监测来进行鉴别[2, 51]。
术前中重度肺动脉高压的患者可能因术中肺动静脉阻断导致压力急剧增高,甚至直接导致术中心搏骤停。此外,肺移植手术因打开心包吻合血管不可避免损害心肌,术后患者心肌酶谱一过性增高,尽管绝大部分患者都能迅速回落,仍需警惕急性冠脉事件可能性,尤其是对于术前即存在冠心病、结构性心脏病的患者。此外,需注意应激性心肌病可能,其表现为可逆性心尖部球样变,虽罕见但需鉴别。心电图动态监测和床边心脏超声检测可提示心源性休克原因,射血分数、心肌局部收缩异常、心脏瓣膜结构性异常、肺动静脉压力等都可以提供临床诊疗思路。
感染是肺移植术后30 d内第二大死因[52]。术后早期感染多源于供体来源病原体或受体气道定植菌入血,可迅速进展为脓毒症及感染性休克。随着ICU侵入性操作、免疫抑制剂及广谱抗生素的应用,耐药菌感染风险显著增加。目前感染性休克的早期补液策略已发生变更,早期限制性补液对于肺移植患者具有临床意义。最佳补液类型尚不清楚,尽管部分学者认为使用白蛋白会导致肺毛细血管内液体堆积,增加肺水肿风险,但根据当前有限的证据和临床经验,白蛋白依然被推荐使用,尤其在患者利尿剂反应不佳的时候[53]。
6 围术期心血管并发症处理要点有哪些?推荐意见12:肺移植术后房性心律失常首选β受体阻滞剂或钙通道阻滞剂控制心室率,对药物难治性房颤可考虑射频消融。(推荐强度B,证据等级2a)
推荐说明:肺移植术后心律失常发生率为25%~35%,窦性心动过速多与容量不足、低氧、疼痛、发热、应激相关,积极寻找并纠正始动因素后能缓解,一般不需要特殊处理。房性心律失常更为常见,包括心房颤动(atrial fibrillation, AF)、心房扑动及室上性心动过速等,其发生常与手术操作牵拉或损伤传导通路、容量异常、电解质紊乱、急性心功能不全、感染及急性冠脉事件等因素相关[52, 54]。术后早期房性心律失常与不良临床结局明确相关,包括气管切开需求增加以及围术期和长期死亡风险上升。此外,高龄、男性、合并心血管疾病、COPD、既往心房颤动史、冠心病血运重建术后及双肺移植受者则为术后房颤发生的高危人群。对血流动力学稳定的房颤/房扑患者,推荐使用β受体阻滞剂或非二氢吡啶类钙通道阻滞剂控制心室率[54]。鉴于胺碘酮的肺毒性风险(如可诱发急性呼吸窘迫综合征、间质性肺炎乃至肺纤维化)及其通过细胞色素P450系统对他克莫司、环孢霉素等免疫抑制剂代谢的干扰,在肺移植术后心律失常处理中应尽量避免使用胺碘酮。当患者房颤持续或药物难以控制时,可考虑射频消融治疗,但当前仍缺乏远期并发症的相关分析[55]。
推荐意见13:对于合并冠心病的肺移植患者,建议制定个体化管理方案,包括术前评估冠状动脉病变或血运重建,术后常规监测心电图、心肌酶谱,在控制出血风险基础上尽早启用抗血小板治疗。(推荐强度B,证据等级2a)
推荐说明:国内老年肺移植患者数量较多,其中合并冠心病的肺移植患者需要密切关注。此类患者术前应充分评估冠脉血流情况,多学科协商确定冠脉处理方案,包括术前或术中行PCI介入或冠脉搭桥术。对于合并冠心病但冠状动脉解剖结构良好且左心室功能正常的肺移植受者,接受血运重建治疗后行肺移植术,亦可获得良好预后[56-59]。
但需注意,合并冠心病的肺移植患者术后非致命性心血管事件的发生率增加,包括心律失常、脑血管意外等[56, 60],这些患者在术后管理中仍需要谨慎维护。应常规监测心电图、心肌酶谱等,且需要多学科团队提前确定抗血小板治疗方案,更积极维持电解质平衡,在早期康复过程中,建议以呼吸训练为主,运动康复可适当放缓,增加医护人员的观察时间,避免急性心力衰竭[61]。故而我们推荐合并冠心病的肺移植患者围术期,在和外科确定出血风险后更早地启用抗血小板药物[62]。
推荐意见14:肺移植术后应警惕肺栓塞可能,其临床症状不典型,对于反复出现的无法解释的低氧血症,无论D-二聚体结果如何,均建议积极完善CTPA等影像学检查。(推荐强度B,证据等级2a)
推荐说明:国内外多项研究报道,肺移植术后肺栓塞(PTE)发生率在1.78%~4.0%左右,其中38%发生于术后1个月内,以间质性肺病亚类患者更为常见[63-64]。由于移植肺缺乏有效的支气管侧支循环,PTE可能是术后呼吸衰竭的一个重要但常被忽视的病因。单肺移植PTE发生率较高,可能与血栓更易进入血流灌注占优的移植肺有关。此外,自体肺常因基础疾病已存在严重功能受损,发生PTE后临床症状多不典型,故漏诊风险较高。部分PTE可表现为与肺部感染相似的呼吸衰竭征象,易被忽视,甚至仅在尸检中确诊[64]。需特别强调的是,术后早期发生的肺栓塞应高度警惕供体来源栓塞的可能。澳大利亚一项单中心研究对122例肺移植术进行分析,其中74例于供肺植入前实施探查性逆行冲洗,发现肉眼可见的意外肺动脉栓塞发生率达38%(其中血栓性栓塞占28%,脂肪栓塞占9%)。尽管术中已行冲洗处理,栓塞组患者术后仍表现出更长的机械通气时间及更低的1年生存率[65]。
推荐意见15:对于术前存在原发性肺动脉高压患者,需高度警惕围术期心力衰竭的风险,建议通过系列超声心动图和有创血流动力学监测早期识别;处理以优化容量管理及适当正性肌力支持为核心。(推荐强度B,证据等级2b)
推荐说明:术前合并原发性肺动脉高压或左心功能不全的受者,其围术期存在特殊的病理生理特点,应高度警惕心力衰竭的风险。患者右心室明显扩张,左心室因慢性压迫向左凸出,导致左心室废用性萎缩及左心室舒张功能受损。单纯肺移植使肺血管阻力恢复正常,维持正常的心输出量,但此病理生理被纠正后,左心室无法适应正常心输出量,可能诱发急性左心衰竭,尤其在拔管时一过性容量过负荷的时候,这种临床改变可以让无症状患者在数小时内迅速发展为严重肺水肿。TEE评估对于建立针对疾病的正确鉴别诊断是必要的[2-3]。
此类患者血流动力学及氧合情况在术后早期通常不稳定,尤其是在单肺移植后。极微小的刺激也可引起肺动脉高压和低氧血症,因此,镇静和机械通气支持通常需持续24~48 h。随后,根据耐受情况逐渐停用镇静或肌松药物,进入脱机流程。撤机前需要做好必要预防措施避免拔管失败,具体措施包括:合理限制液体入量、拔管时保持高坐位、适当使用左心室正性肌力药物(如多巴酚丁胺)。对于正性肌力药物反应不佳或合并严重低氧血症的难治性左心衰竭,应考虑适当延长机械通气及ECMO支持,并使用高PEEP以减少心脏前负荷。但如果过于严格地限制体液,则会出现完全相反的情况,这可能是应用右心室流出障碍导致的[66]。
7 围术期感染防控重点是什么?推荐意见16:肺移植受者术后感染风险较高,强调早期更积极的病原学监测,基于供受体定植及当地流行病学实施个体化抗感染策略,经验性覆盖革兰阴性菌与阳性球菌。(推荐强度B,证据等级2a)
推荐说明:肺移植受者因手术复杂、终末期肺病基础及移植后免疫抑制状态,术后感染风险较高。国内多中心研究显示术后感染发生率约68.3%,主要源于供体相关感染与院内感染[67]。移植后前6个月强免疫抑制期内机会性感染风险显著增加[68-69]。供体来源感染中,下呼吸道定植菌检出率高达48%~89%,其中约5%为多重耐药菌。国际数据显示,约0.18%~0.23%的供体发生病原体传播,以细菌(30%)和病毒(31%)为主,多发生于术后30 d内[70-71]。除供体来源外,医院获得性感染与受体自身菌群亦不容忽视。感染危险因素常包括吻合口组织坏死、肺去神经化致清除功能下降及天然气道菌群定植。
肺移植围术期感染部位以下呼吸道细菌感染与手术部位为主,其中手术部位感染发生率约5%~19%,多见于术后3~4周,以脓胸(42%)、手术切口感染(29%)及纵隔感染(16%)为主,革兰阴性菌与阳性菌比例相近[72-73]。
围术期经验性抗感染方案需结合受体基础疾病、供受体病原体定植情况、药敏结果及本地耐药流行病学制定[74]。结构性肺病(如支气管扩张)患者建议常规覆盖铜绿假单胞菌;合并肺结核或真菌感染高危因素者需扩展抗真菌覆盖。多项研究显示术后病原体以革兰阴性菌(如克雷伯菌、不动杆菌、假单胞菌)为主,其次是革兰氏阳性球菌和真菌[75-76]。一项基于全世界99个肺移植中心的横断面问卷调查结果显示,89%的中心常规覆盖革兰阴性菌,哌拉西林/他唑巴坦与第四代头孢菌素为常用选择;84%的中心联用抗MRSA药物(万古霉素为主)[77]。多重耐药菌流行地区应强化初始方案,可联合使用碳青霉烯类与氨基糖苷类或黏菌素。抗生素使用疗程存在差异,多数中心建议至少7~14 d,即使供体和受体培养结果为阴性仍多继续用药[77]。推荐基于供受体定植状态及当地流行病学资料个体化调整用药,并依据终末期器官功能调整抗生素剂量,同时谨慎把握围术期不同阶段抗菌药物的启用与停用时机[78-79]。
推荐意见17:肺移植受者侵袭性真菌感染风险显著,围术期建议普遍预防性抗真菌治疗,重点关注吻合口及气道感染情况,并根据个体风险调整疗程。(推荐强度B,证据等级2a)
推荐说明:肺移植受者侵袭性曲霉病发病率为4%~23.3%,显著高于其他实体器官移植[80]。国内单中心数据显示术后真菌感染率达13.9%,以丝状真菌和白色念珠菌为主[81]。其临床表现除常见的结节状空洞外,亦可见移植特有类型,如吻合口感染及溃疡性或假膜性气管支气管炎[80]。术后建议常规进行抗真菌预防,但目前尚无统一方案。多采用全身联合吸入性抗真菌药(如吸入性两性霉素等),其中吸入制剂可有效降低气道及吻合口局部感染风险。预防多持续至术后6个月内,主要针对曲真菌属[81-84]。对于高危患者或常规预防效果不佳时,可考虑联合棘白菌素类药物治疗。
推荐意见18:肺移植围术期建议常规预防巨细胞病毒感染。(推荐强度B,证据等级2a)
推荐说明:肺移植受者巨细胞病毒(cytomegalovirus, CMV)感染风险显著增高,尤其在术后前6个月。血清阳性的受者(D+/R+)或未感染的受者(D+/R-)均可能发生原发感染或再激活,因此常规推荐预防性抗病毒治疗[74, 85]。CMV感染临床表现差异大,包括无症状病毒血症、CMV综合征和CMV肺炎,后者影像学不典型,与急性排斥反应症状部分重叠,且与5年生存率下降相关[86-88]。建议所有肺移植受者接受至少3个月预防,D+/R-群体应延长至6-12个月[85, 89]。可于术后1~2周启用静脉更昔洛韦,后过渡至口服用药[74]。治疗性用药需结合病毒载量动态调整,通常持续至少2周直至病毒学转阴[87]。大多数CMV综合征病例为轻度至中度感染,可通过口服缬更昔洛韦进行治疗,如果无法口服药物或病情进展迅速或严重,首选静脉注射更昔洛韦。对于更昔洛韦、缬更昔洛韦、膦甲酸钠或西多福韦等常规抗病毒药物耐药或难治性的CMV感染,新型抗病毒药物如马立巴韦(maribavir)等已在临床研究中展现出潜在疗效。莱特莫韦(letermovir,商品名Prevymis®)作为一种DNA末端酶复合物抑制剂,虽已获批准用于造血干细胞移植受者的CMV预防,但其在肺移植等实体器官移植中的有效性和安全性证据仍有限。
8 如何处理肺移植围术期神经系统并发症?推荐意见19:肺移植术后出现神经系统症状(如意识障碍、癫痫发作)需立即排查脑血管意外、可逆性后部脑病综合征(PRES)及颅内感染,同时评估代谢紊乱和免疫抑制剂神经毒性,对PRES患者应优先调整免疫抑制方案并控制脑水肿和癫痫发作。(推荐强度B,证据等级2a)
推荐说明:肺移植术后早期神经系统并发症常见且严重影响预后,据国外研究报道,早期神经系统并发症发生率为10%左右[90]。缺血性卒中和脑出血是肺移植术后中枢神经系统中常见并发症,其中以缺血性脑卒中最多见。但这类疾病主要和患者术前状态相关,包括心律失常、凝血功能障碍、细菌性心内膜炎等,这些疾病可能预先存在并在移植后进展[91]。此外,移植后各种休克可能会加重缺血性卒中的发生。可逆性后部脑病综合征(posterior reversible encephalopathy syndrome, PRES)是一种(亚)急性发作的神经系统疾病,可发生在肺移植术后任何时期,与他克莫司/环孢素浓度并无相关性。PRES主要表现为视觉障碍、癫痫持续状态、脑水肿、脑积水和局灶性神经功能缺损[92]。头颅磁共振检查(magnetic resonance imaging, MRI)中有典型的枕叶高信号,但脑脊液无特异度表现。该疾病主要以对症治疗为主,包括识别和治疗潜在的诱发因素以及脑水肿和癫痫发作。经积极治疗,PRES大多数是可逆的。颅内感染相对少见,其中各种病毒性脑炎需要关注,包括疱疹病毒6型导致的急性边缘性脑炎,巨细胞病毒相关性脑炎等。另外,隐球菌脑膜炎,组织胞浆菌、曲真菌、耶氏肺孢子虫也可能导致颅内感染。当存在不明原因发热,神经系统表现时,建议尽快完善脑脊液检查,包括宏基因测序[91]。代谢性脑病则涵盖脓毒症相关脑病、肝性脑病和非肝因素特发性高氨血症、长期维生素B1缺乏引起的韦尼克脑病、肾功能不全导致的尿毒症脑病、电解质紊乱导致的相关脑水肿等。
推荐意见20:肺移植术后出现不明原因意识障碍时,应积极检测血氨水平并完善脲原体筛查,确诊特发性高氨血症后需联合CRRT降血氨(尤其意识障碍者)及针对性抗感染治疗。(推荐强度B,证据等级2a)
推荐说明:特发性高氨血症是一种特殊类型的代谢性脑病,目前认为肺移植受者和解脲脲原体机会性感染导致尿素循环障碍相关。高氨血症引起的精神状态并无特异度,包括改嗜睡、情绪和人格障碍、共济失调、呕吐、癫痫发作、深昏迷等。对于术后30 d内新发精神状态改变的肺移植受者,即使已存在明确诱因,仍建议常规监测血氨水平,以辅助临床决策[93]。一旦怀疑特发性高氨血症,应立即完善支原体和解脲支原体相关检查,包括血、呼吸道分泌物标本。早期降血氨治疗能够缓解脑水肿表现,包括使用乳果糖、门冬氨酸鸟氨酸和甘露醇等,意识水平明显下降患者,建议早期使用CRRT清除血氨[93]。对于可疑支原体感染需要使用喹诺酮类或大环内酯类治疗,常规治疗疗程为2周,但需监测至血氨完全正常后1周后再考虑停药。
9 如何开展肺移植术后个体化镇静镇痛策略及谵妄防治?推荐意见21:肺移植术后应实施以目标为导向的镇静镇痛策略,镇静优选丙泊酚或右美托咪定滴定给药,避免常规使用苯二氮䓬类药物;镇痛以阿片类药物为基础,联合多模式镇痛策略及非药物干预,重点关注高危患者及慢性疼痛的长期管理。(推荐强度B,证据等级2a)
推荐说明:肺移植术后镇静管理应以浅镇静为目标,维持Richmond躁动-镇静评分(richmond aitation sedation scale, RASS)在-1~0分最佳,以期实现患者早期清醒及配合治疗。建议在生命体征平稳后尽早停用镇静药物,并于再次用药前全面评估神志及肌力状态。目前尚无临床研究表明何种术后镇静药物预后最好。鉴于苯二氮䓬类药物可能因蓄积作用延长机械通气时间,已不推荐常规使用[94-95]。2017年一项多中心调查显示,术后镇静首选丙泊酚(57%)与右美托咪啶(18%)[96]。推荐二者滴定给药以实现理想镇静深度;其中右美托咪啶因呼吸抑制轻微,兼具抗焦虑与镇痛效应,且可安全用于拔管后阶段,但需关注其窦性心动过缓相关不良反应。对术前因特殊治疗(如俯卧位通气、控制性机械通气)已接受深镇静及肌松药物者,应每日重新评估深镇静必要性,并在指征消失后尽快减停药物。需高度关注此类患者术后镇静药物蓄积风险,建议对意识持续未恢复者进行血药浓度监测,有条件的中心可借助量化脑电图客观评估镇静深度并早期识别神经系统并发症。如考虑药物蓄积,可酌情使用氟马西尼等特异度拮抗剂。
患者疼痛管理应贯穿整个围术期。推荐对清醒患者采用视觉模拟评分法(visual analog scoring, VAS),镇静患者使用行为疼痛量表或危重症疼痛观察工具(critical care pain observation tool, CPOT)进行系统评估[94],目标将镇痛评分控制在0~2分。术后常规使用阿片类药物进行基础镇痛,瑞芬太尼因起效迅速、代谢快、呼吸抑制较轻,适用于气管插管期间维持;舒芬太尼、地佐辛等也可作为选择。拔管后接受无创通气者,应逐渐减停阿片类药物,并过渡至多模式镇痛策略。患者自控镇痛(patient controlled analgesia, PCA)泵可用于个体化镇痛调整,常用药物包括吗啡、舒芬太尼和氢吗啡酮,使用前需充分进行患者宣教。辅助镇痛可选用阿片类局部贴剂、曲马多、氟比洛芬等;疑似神经性疼痛者可联合加巴喷丁或普瑞巴林[97]。应特别关注术前合并抑郁或焦虑状态的患者,其术后疼痛程度可能更高,需动态评估,必要时加用抗焦虑或抗抑郁药物[98]。研究表明,约47.2%的患者术后3个月仍存在慢性疼痛,建议将疼痛管理纳入长期随访以改善患者生活质量[99]。
推荐意见22:肺移植术后可采用ESCAPE谵妄集束化方案进行管理。内容包括:(E)早期活动和改善ICU环境;(S)睡眠管理;(C)浅镇静;(A)控制疼痛;(P)精神状态评估;(E)积极沟通。(推荐强度B,证据等级2a)
推荐说明:谵妄是各种因素引起的一过性意识混乱状态,表现为意识障碍和认知功能改变,以精神症状为主要表现。谵妄患者意识水平高低不等,意识内容杂乱无章,是全身疾病和脑功能共同作用的结果。术后应激状态、嘈杂的ICU环境、急性疼痛、睡眠障碍等均可能诱发术后患者谵妄。有回顾性研究报道,肺移植术后早期谵妄发生率达36%~44%,其危险因素可能包括肥胖、术前苯二氮䓬类药物使用、术中低血压(MAP < 60 mmHg)持续时间等[100-101]。其他相关因素还涉及术中并发症、药物毒性(如钙调磷酸酶抑制剂所致神经毒性)、感染、代谢紊乱、神经系统并发症、酒精或药物戒断,以及维生素(如硫胺素、维生素B12、叶酸)缺乏和内分泌异常等。
谵妄分为兴奋型、抑制型和混合型。兴奋型谵妄以躁动、烦躁不安、试图拔除各种管路为特征;抑制型谵妄以感情淡漠、言语减少、嗜睡为特征;混合型则具备两者的典型特征。其中兴奋型谵妄需要区分糖皮质激素使用后的兴奋状态,前者定向力缺失而后者保留定向力。ICU医生可以通过谵妄评估量表(confusion assessment method for intensive care unit, CAM-ICU)评估方法进行评定。肺移植术后谵妄患者可通过ESCAPE谵妄集束化方案进行管理[102-103],具体包括:(E)早期活动和改善ICU环境,包括提供眼罩、耳塞、音乐等;(S)睡眠管理:维持昼夜节律,维持睡眠节律和时间,可使用阿普唑仑和酒石酸唑吡坦;(C)浅镇静水平;(A)控制疼痛;(P)精神状态评估;(E)医务人员,患者家属积极同患者沟通,进行情感交流。更早脱离ICU环境有助于谵妄控制。在肺移植术后谵妄的预防策略中,应较常规外科患者更加注重优化呼吸支持与改善通气舒适度,见表 3。
| ICU谵妄防治Bundle | 肺移植术后谵妄防治Bundle |
| A:疼痛预防和管理 | A (Ache):疼痛预防和管理 |
| B:每日唤醒和SBT实验 | B (be quiet and sleep):安静和充分休息 |
| C:镇静镇痛 | C (comfort):提高呼吸舒适度 |
| D:评估谵妄 | D (drug less):减少药物干预 |
| E:早期活动 | E (Exercise):早期活动 |
| F:家庭参与 | F (Family):家庭参与 |
推荐意见23:术后拔管即需评估吞咽障碍和反流误吸风险;围术期应每日评估应激性溃疡、胃轻瘫等急性胃肠损伤症状。(推荐强度B,证据等级2a)
推荐说明:吞咽障碍是肺移植术后常见并发症,尤其多见于长时间气管插管或喉返神经损伤致声带麻痹的患者。研究显示,约70.5%的肺移植术后患者存在不同程度的吞咽功能障碍,其中63.8%伴发误吸[104]。常规床边检查难以明确无症状性误吸,建议在恢复经口进食前采用改良钡餐或纤维内镜等充分评估吞咽功能[105]。在此之前,可留置鼻肠管以保证药物及营养摄入。术后胃轻瘫亦较为常见,多与手术操作、免疫抑制剂使用或神经肌肉功能损伤相关,临床表现为恶心、呕吐、早饱和腹胀等。建议调整饮食(少量多餐、低脂低纤维)、使用胃肠动力药物,并在必要时予以肠外营养支持。难治性病例亦可考虑胃电刺激或幽门注射肉毒杆菌毒素[106]。
针对术后胃肠道功能的系统评估,推荐采用急性胃肠损伤(acute gastrointestinal injury,AGI)分级[107]:Ⅰ级为存在风险或胃肠道功能部分受损;Ⅱ级为胃肠功能障碍,无法满足机体正常营养需求,表现为胃轻瘫伴大量潴留、腹泻或喂养不耐受;Ⅲ级指经干预仍无法改善的胃肠功能衰竭,伴肠内营养持续不耐受和多器官功能衰竭(multiple organ dysfunction syndrome,MODS)进展;Ⅳ级为合并远隔器官功能障碍的严重衰竭状态,病情急剧恶化,致死风险高,需急诊手术处理。建议根据AGI分级制定个体化营养支持与治疗策略。对于胃肠道功能评估Ⅰ级的患者,建议在肠胃损伤后24~48 h尽早给予肠内营养(enteral nutrition,EN);Ⅱ级以上应用胃肠动力药;开始或维持肠内营养。如果发生大量胃潴留或反流,常规考虑尝试给予少量的肠内营养。不耐受肠内营养的患者应给予补充肠外营养(parenteral nutrition,PN)。Ⅳ级患者则需禁食,并需要进一步外科干预[108-109]。
推荐意见24:肺移植术后应常规监测肝功能指标(包括转氨酶、胆红素、血氨及碱性磷酸酶等),并筛查病毒学及影像学异常;肝功能损害需积极明确病因,针对右心衰竭、药物毒性、感染及营养等因素进行干预,必要时考虑人工肝支持治疗。(推荐强度B,证据等级2a)
推荐说明:肺移植术后肝功能损害可见于容量复苏后右心衰竭导致肝脏淤血;药物性肝脏损害,如伏立康唑、对乙酰氨基酚、胺碘酮;其次是术后长期肠外营养相关性肝病和脓毒症相关性肝损伤。此外需要警惕免疫抑制情况下诱发的急性乙型病毒性肝炎,巨细胞病毒和EB病毒也会引起急性肝炎症状,但相对少见。术后要密切监测肝酶指标,包括谷丙转氨酶、谷草转氨酶、总胆红素、直接胆红素、间接胆红素、血氨、碱性磷酸酶、γ-谷氨酰转肽酶,同时建议术后定期复查乙型病毒性肝炎抗体和DNA。这些指标结合腹部超声和CT影像学检查,能够初步判断患者是否存在胆源性或肝源性疾病。肝功能异常通常以治疗原发病和药物治疗为主,极少患者需要进行血浆置换、血浆灌流等人工肝治疗[93]。
11 如何进行肺移植围术期急性肾损伤管理?推荐意见25:肺移植术后应高度警惕急性肾损伤(AKI),应严格遵循KDIGO指南,优化肾脏灌注,避免肾毒性药物及对比剂使用,优先选择对肾血流影响较小的血管活性药物。(推荐强度B,证据等级2a)
推荐意见26:肺移植术后CRRT应用时机应根据容量、内环境、利尿反应性综合评估。(推荐强度D,证据等级5)
推荐说明:肺移植术后急性肾损伤(acute kidney injury, AKI)是影响患者术后恢复和长期生存的重要因素。研究报道,约33%~69%的受者在术后出现AKI,其中5%至13%的患者需要连续性肾脏替代治疗(continuous renal replacement therapy, CRRT)[110-113]。AKI的高危因素包括:①有效循环容量不足;②过度利尿;③心功能障碍;④肾毒性药物(免疫抑制剂、抗生素);⑤围手术期脓毒症;⑥其他(动脉粥样硬化、急性间质性肾炎)。肺移植术后血流动力学不稳定及低氧血症刺激肾上腺素能神经并改变NO代谢,影响肾脏血流分布。此外,高碳酸血症会诱发外周血管扩张,降低全身血管阻力,导致肾素-血管紧张素-醛固酮系统(renin-angiotensin-aldosterone system,RAAS)的激活并直接收缩肾脏血管,引起肾脏灌注减少,诱发AKI。度过急性期后,诱发AKI的因素逐渐转变,脓毒症及感染性休克中炎症介质损伤肾小管,导致急性肾小管坏死,免疫抑制剂和抗生素的肾毒性可能诱导急性肾损伤转变为慢性肾功能不全[114-116]。
AKI的诊断按照KDIGO指南进行分期,目前尚无有效的药物治疗,治疗限于解除诱因和CRRT[2-3]。对于诊断为AKI患者,循环不稳定时使用较高剂量血管活性药物维持较高的平均动脉压(如MAP > 75 mmHg)维持适当的肾脏灌注;在适度补充容量后再使用利尿剂,避免激进的利尿策略;优先使用他克莫司而不是环孢素;避免静脉使用氨基糖苷类、两性霉素B等肾毒性强的抗生素,并积极根据内生肌酐清除率和CRRT处方调整抗生素用药剂量;积极纠正高碳酸血症;规范进行造影剂前后水化流程等。
肾脏替代治疗时机尚不明确,目前多项大型临床研究并不支持更早的进行CRRT治疗,另外由于免疫抑制等因素,倾向于保守的CRRT治疗策略。当患者出现保守治疗无效的高钾血症、严重代谢性酸中毒,利尿效果不佳的高容量状态,可考虑行CRRT治疗,对于右心衰竭、肺动脉高压患者,更应尽早评估。鉴于肺移植患者需要早期活动需要,尽量留置颈内透析置管,且做好护理。尽管大部分患者能恢复正常肾功能,但仍有少数患者转变为慢性肾功能不全,需要终生肾脏替代治疗。
12 肺移植围术期营养支持与早期康复促进要点有哪些?推荐意见27:肺移植术后应充分评估营养风险,早期推荐总热量摄入为25~35 kcal/kg,1.3~1.5 g/kg的蛋白质摄入,优先选择经口进食或肠内营养支持。(推荐强度B,证据等级2a)
推荐说明:肺移植术后早期,手术创伤与应激状态显著增加机体营养需求。营养支持旨在满足代谢消耗、补充能量储备,并促进移植物存活。此外,若并发感染、消化系统并发症、PGD或排斥反应,将进一步改变营养代谢状况,需动态评估营养风险并个体化调整营养支持策略[109]。建议每日评估患者腹部体征、EN耐受性及PN处方合理性,密切观察相关不良反应。可通过监测前白蛋白、转铁蛋白等指标初步评估代谢状态;床旁超声有助于评估胃潴留;具备条件的医疗中心可采用代谢车监测氮平衡,为营养处方的制定与调整提供依据。
目前尚缺乏针对肺移植受者特定营养需求及其预后影响的专门研究。基于其他实体器官移植及重大手术患者的循证依据,建议肺移植术后早期每日总热量摄入目标为25-35 kcal/kg[2, 109]。对于术后早期拔管且无吞咽障碍或误吸风险的患者,应优先选择经口进食;如果无法口服,则应将早期EN作为管理重点,建议于术后48 h内启动;若存在EN禁忌,应在3~7 d内实施PN。当间接量热法无法客观评估能量需求,能量供给目标可设定为每日25~30 kcal/kg。实际热量需求应根据患者移植前营养状况、并发症(如感染、排斥反应)等进行个体化调整[109]。
在移植后的开始阶段,蛋白质分解代谢明显增加,营养治疗的重点应该是尽量减少损失,保持目前的体重。因此,患者每天应保证1.3~1.5 g/kg的蛋白质摄入。然而,存在严重营养不良、胸管引流漏、伤口愈合不良、感染或发生排斥反应的患者每天蛋白质需求可增加至2.5 g/kg[2, 109]。氮平衡监测可用于评估蛋白质代谢状态,并据此调整蛋白质供给。同时应保障充足的微量营养素及电解质摄入,维持钠、钾、镁等电解质稳态,必要时补充钙剂及维生素A、C、D。
推荐意见28:围术期管理团队应强化肺移植受者术前访视,充分评估患者康复潜力。(推荐强度B,证据等级2b)
推荐说明:肺移植术前患者常因运动耐量下降及长期卧床导致肌肉萎缩。肺预康复作为一项成熟有效的干预措施,可显著改善慢性呼吸系统疾病患者的运动能力和生活质量,目前应用广泛[117-119]。尽管现有研究多集中于COPD,间质性肺病证据相对较少,但多项研究均表明,即便对于病情严重的移植等待者,术前康复仍可安全实施,并有助于提升功能锻炼水平与生存质量[120-122]。有研究显示,6 min步行距离每增加100 m,术后住院时间可减少2.6 d[123]。因此,建议肺移植术前等待患者,通过专业的康复评估制定个体化预康复方案。
推荐意见29:肺移植术后应尽早启动康复训练,重点包括呼吸功能训练以及吞咽功能评估与康复,定期超声监测膈肌活动度指导康复进程,以预防呼吸肌疲劳及肺部并发症。(推荐强度B,证据等级2a)
推荐说明:肺移植术后康复训练应尽早进行,尤其是术前长期卧床的患者。长期机械通气容易导致膈肌废用,一旦脱离呼吸机,需尽快指导建立有效的咳痰反射和呼吸方式,避免呼吸肌疲劳。脱机患者则需要进行高强度排痰操作和体位引流,包括使用震动排痰仪、高频震荡通气、频繁翻身拍背等[124]。痰液引流能够最大程度避免术后低氧血症和高碳酸血症发生,有利于早期康复顺利进行,包括自主引流和高频震动排痰,实施中关注患者疼痛、氧和情况。患者术后膈肌活动受影响,咳嗽反射及腹式呼吸的建立存在困难,适当负重训练和正确的引导至关重要,并通过每周B超评估膈肌功能活动度评价康复疗效[125]。
肺移植术后患者易发生呛咳及隐匿性误吸,是导致反复肺部感染的重要危险因素。拔除气管插管后,应尽早进行吞咽功能评估与康复干预。推荐使用洼田饮水试验、反复唾液吞咽试验或容积-黏度吞咽测试等进行初步筛查;若怀疑存在误吸或需明确诊断,可采用吞咽造影检查或软管喉内镜吞咽功能评估。可行染料试验(如果绿、亚甲蓝等)并通过气道分泌物抽吸辅助判断。需注意,支气管镜下虽可观察误吸,但需警惕假阳性结果[126]。
推荐意见30:肺移植术后应系统化防治ICU获得性肌无力,通过MRC评分、握力测量及肌肉超声等早期识别,预防以早期康复、多学科协作及代谢管理为核心,对已发生ICU获得性肌无力者实施阶梯式康复,重点关注肌松剂使用者的个体化方案。(推荐强度B,证据等级2a)
推荐说明:肺移植术后ICU获得性肌无力(intensive care unit-acquired weakness, ICU-AW)的防控需系统化实施。早期识别应结合医学研究委员会(MRC)肌力评分及握力测定;对无法配合者,可借助肌肉超声(MUS)监测股四头肌形态与回声变化辅助诊断。预防应以早期康复为核心,待血流动力学稳定后即开始呼吸肌及渐进式肢体训练[125, 127],并严格控制血糖(目标6~10 mmol/L)、优化营养支持[热量25~30 kcal/(kg·d)]及合理镇静,多学科协作是有效实施的关键。对已发生ICU-AW的患者,康复应遵循阶梯原则:从被动关节活动逐步过渡至主动训练(肌力≥4级),包括坐位平衡、辅助站立及行走等。需密切监测耐受度,避免过度疲劳,Borg指数(见表 4)可作为量化依据[128]。术前长期使用肌松剂者需个体化方案,重点加强上肢和远端肌群训练,并鼓励家庭参与以优化康复效果。
| 分值 | 描述(5分及以上建议立即暂停训练) |
| 0分 | 一点也不觉得呼吸困难或疲劳 |
| 0.5分 | 非常非常轻微的呼吸困难或疲劳,几乎难以察觉 |
| 1分 | 非常轻微的呼吸困难或疲劳 |
| 2分 | 轻度的呼吸困难或疲劳 |
| 3分 | 中度的呼吸困难或疲劳 |
| 4分 | 略严重的呼吸困难或疲劳 |
| 5分 | 严重的呼吸困难或疲劳 |
| 6~8分 | 非常严重的呼吸困难或疲劳 |
| 9分 | 非常非常严重的呼吸困难或疲劳 |
| 10分 | 极度的呼吸困难或疲劳,达到极限 |
推荐意见31:肺移植术后睡眠障碍可采用多导睡眠监测(PSG)联合体动记录仪及主观量表(如PSQI等)综合评估,重点关注药物(如他克莫司)影响及心理因素(焦虑/抑郁),通过药物浓度监测、剂量调整及心理行为干预实现个体化管理。(推荐强度A,证据等级1a)
推荐说明:目前,约有30%~81%的肺移植患者术后存在睡眠质量差的问题,女性和年轻患者更易受影响。常见问题包括总睡眠时间减少、睡眠效率下降及入睡延迟[129-133]。使用多导睡眠监测(polysomnography, PSG)可客观评估睡眠指标,发现部分患者夜间觉醒时间延长,总睡眠时间少于6 h,睡眠效率低于85%。体动记录仪和主观问卷,如匹茨堡睡眠质量指数(pittsburgh sleep quality index, PSQI)量表等,可以提供更多居家环境下的睡眠数据[129-131, 134-135]。钙调磷酸酶抑制剂(如他克莫司)可能干扰睡眠周期,显著增加失眠发生风险,需对患者进行血药浓度和睡眠监测,并及时调整治疗方案[133]。抑郁和焦虑显著影响术后睡眠质量,尤其是在失眠严重的患者中。通过心理支持和行为疗法可显著改善患者的睡眠和整体生活质量[135-136]。肺移植术后睡眠质量差是一种普遍现象,涉及多方面影响因素,包括药物作用、生理变化及心理状态等。通过结合多种主客观评估方法,可以全面了解患者的睡眠情况并采取个性化干预措施。
13 围术期患者免疫状态监测和抗排异药物使用特点有哪些?推荐意见32:建议根据ISHLT病理分级制定个体化抗排异策略,对A2级及以上急性细胞性排斥应予积极治疗,对无症状A1级排斥可在肺功能稳定时予以观察;抗体介导的排斥需综合临床、抗体检测及影像病理结果诊断,可采用抗体清除联合靶向免疫治疗。(推荐强度B,证据等级2a)
推荐意见33:术后建议采用以糖皮质激素联合钙调磷酸酶抑制剂(CNIs)为基础的免疫抑制方案,诱导阶段可短期应用T细胞抗体制剂;应避免无CNIs方案,并根据个体反应动态调整治疗。(推荐强度B,证据等级2a)
推荐说明:急性细胞性排斥反应在移植后第一年内的发生率约20%~50%,目前认为其主要机制为移植肺中的T细胞浸润[137]。在大多数情况下,通过强化糖皮质激素治疗可缓解急性细胞性排斥[138]。对于复发或激素抵抗的急性排斥反应,可采用抗胸腺细胞球蛋白、全淋巴照射或体外光分离疗法进行治疗。急性细胞性排斥反应的诊断需依据经支气管活检标本,并参照国际心肺移植学会(ISHLT)病理学评分标准进行判定[139]。对于A2级(轻度排斥)及以上的病例,即使患者无症状,通常也予以治疗;而对无症状的A1级(极轻微排斥)是否需干预仍存争议。若肺功能保持稳定,可考虑采取密切观察,因研究显示A1级排斥并未明显增加慢性移植肺功能障碍或死亡风险[140]。
抗体介导的排斥反应由受者体内抗供者HLA或非HLA抗原的抗体引发,既可单独发生,也可与急性细胞性排斥并存。其诊断需综合临床症状、新发供者特异度抗体的检出以及影像学和病理学上移肺损伤表现的变化,以提高确诊把握。与肾组织相比,补体(C4d)染色在肺组织中对抗体介导排斥的诊断特异度较低。治疗手段包括通过血浆置换和静脉注射免疫球蛋白以清除抗体,并可采用免疫细胞靶向治疗,如利妥昔单抗、蛋白酶体抑制剂等[141]。对于新近检测出供者特异度抗体但无影像或病理学排斥证据的无症状受者是否应予以治疗,目前尚无定论[142]。
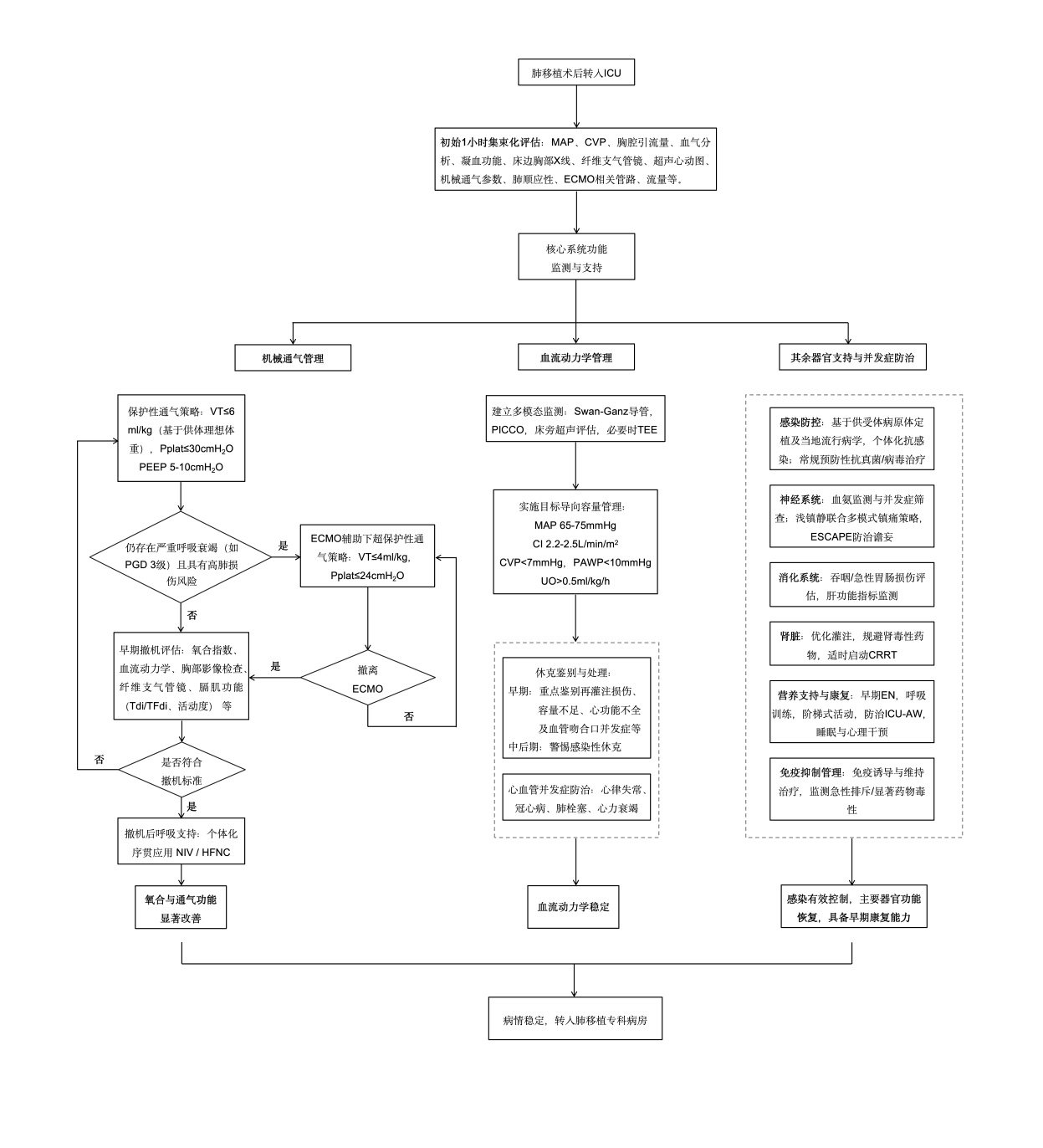
肺移植免疫抑制治疗包括免疫诱导和维持治疗两阶段。免疫诱导治疗的中心间差异显著,目前尚无统一共识,建议围术期采用短期、高效的诱导方案,以预防早期急性排斥反应,延迟维持性免疫药物的应用或减少其用量。常用诱导药物为T细胞抗体制剂,包括单克隆抗体(如巴利昔单抗、阿仑单抗)及多克隆抗体(如抗胸腺细胞球蛋白)。维持治疗常采用多药联合方案,通过作用于淋巴细胞活化不同阶段协同抑制免疫应答,核心药物包括糖皮质激素、钙调磷酸酶抑制剂(calcineurin inhibitors, CNIs)、抗代谢药和哺乳动物雷帕霉素靶蛋白抑制剂(mammalian target of rapamycin inhibitors, mTORi)。标准方案为泼尼松+他克莫司+吗替麦考酚酯(mycophenolate mofetil, MMF)三联治疗[143-144],部分采用四药方案(泼尼松+CNIs+抗代谢药+mTORi)。肺移植围术期重症监护系统化管理流程方案见图 1。应注意的是,无CNIs方案常与较高的急性排异风险相关,因此并不推荐放弃CNIs治疗而仅用mTORi[145]。总体原则建议采用个体化联合用药策略,在确保有效预防排斥的前提下,尽可能减少药物剂量以降低不良反应,并依据治疗反应与免疫状态动态调整方案。
|
| 图 1 肺移植围术期重症监护系统化管理流程图 |
|
|
执笔作者:周瑜(浙江大学医学院附属第二医院)丁朔(浙江大学医学院附属第二医院)王大鹏(南京医科大学附属无锡人民医院)
参与编写者:梁琦强(同济大学附属东方医院)万胡强(浙江大学医学院附属第二医院)赵晋(浙江大学医学院附属第二医院)李晓霞(浙江大学医学院附属第二医院)
专家组成员(按姓名拼音排序):陈静瑜(南京医科大学附属无锡人民医院)代明营(青岛大学附属医院)杜鑫淼(四川大学华西医院)冯敏(郑州大学第一附属医院)郭璐(四川省医学科学院·四川省人民医院)何小军(浙江大学医学院附属第二医院)胡春晓(南京医科大学附属无锡人民医院)黄健(浙江大学医学院附属第二医院)黄曼(浙江大学医学院附属第二医院)姜淑云(南京医科大学附属无锡人民医院)巨春蓉(广州医科大学附属第一医院)柯立(中国科学技术大学附属第一医院)李洋(吉林大学第一医院)李玉萍(上海市肺科医院)梁朝阳(中日友好医院)林慧庆(武汉大学人民医院)刘金平(武汉大学中南医院)乔坤(深圳市第三人民医院)卫栋(南京医科大学附属无锡人民医院)魏文学(河南省人民医院)吴波(南京医科大学附属无锡人民医院)吴云龙(杭州市临平区第一人民医院)许红阳(南京医科大学附属无锡人民医院)杨莉(浙江大学医学院附属第四医院)药晨(中国人民解放军总医院)叶冰(福建医科大学附属协和医院)曾妃(浙江大学医学院附属第二医院)
利益冲突 所有作者声明无利益冲突
| [1] | 黄洁夫. 中国器官捐献和移植发展报告[M]. 北京人民卫生出版社, 2025: 234. |
| [2] | Di Nardo M, Tikkanen J, Husain S, et al. Postoperative management of lung transplant recipients in the intensive care unit[J]. Anesthesiology, 2022, 136(3): 482-499. DOI:10.1097/aln.0000000000004054 |
| [3] | Girgis R, Hadley R, Murphy E. Pulmonary, circulatory and renal considerations in the early postoperative management of the lung transplant recipient[J]. Gcsp, 2023, 2023(3): e202318. DOI:10.21542/gcsp.2023.18 |
| [4] | Shintani Y, Funaki S, Kanou T, et al. Integrated cardiothoracic team approach for complex lung transplantation procedures in Japan: current status and future direction[J]. J Thorac Dis, 2023, 15(9): 5195-5203. DOI:10.21037/jtd-22-1720 |
| [5] | 胡春晓, 李小杉, 钱共匋, 等. 基于多团队协作下的中国肺移植质控体系的构建[J]. 中华器官移植杂志, 2018, 39(12): 707-710. DOI:10.3760/cma.j.issn.0254-1785.2018.12.001 |
| [6] | Machuca TN, Collaud S, Mercier O, et al. Outcomes of intraoperative extracorporeal membrane oxygenation versus cardiopulmonary bypass for lung transplantation[J]. J Thorac Cardiovasc Surg, 2015, 149(4): 1152-1157. DOI:10.1016/j.jtcvs.2014.11.039 |
| [7] | Clark SC, Levine AJ, Hasan A, et al. Vascular complications of lung transplantation[J]. Ann Thorac Surg, 1996, 61(4): 1079-1082. DOI:10.1016/0003-4975(96)00003-3 |
| [8] | Mughal MM, Gildea TR, Murthy S, et al. Short-term deployment of self-expanding metallic stents facilitates healing of bronchial dehiscence[J]. Am J Respir Crit Care Med, 2005, 172(6): 768-771. DOI:10.1164/rccm.200410-1388oc |
| [9] | Avasarala SK, Dutau H, Mehta AC. Forbearance with endobronchial stenting: cognisance before conviction[J]. Eur Respir Rev, 2023, 32(167): 220189. DOI:10.1183/16000617.0189-2022 |
| [10] | Verbeek GL, Myles PS, Westall GP, et al. Intra-operative protective mechanical ventilation in lung transplantation: a randomised, controlled trial[J]. Anaesthesia, 2017, 72(8): 993-1004. DOI:10.1111/anae.13964 |
| [11] | Fuehner T, Kuehn C, Welte T, et al. ICU care before and after lung transplantation[J]. Chest, 2016, 150(2): 442-450. DOI:10.1016/j.chest.2016.02.656 |
| [12] | Beer A, Reed RM, Bölükbas S, et al. Mechanical ventilation after lung transplantation. an international survey of practices and preferences[J]. Annals ATS, 2014, 11(4): 546-553. DOI:10.1513/annalsats.201312-419oc |
| [13] | Morgan S, Aneman A, Nair P. Mechanical ventilation post-bilateral lung transplantation: a scoping review[J]. Acta Anaesthesiol Scand, 2023, 67(5): 576-587. DOI:10.1111/aas.14219 |
| [14] | Eberlein M, Reed RM, Bolukbas S, et al. Lung size mismatch and primary graft dysfunction after bilateral lung transplantation[J]. J Heart Lung Transplant, 2015, 34(2): 233-240. DOI:10.1016/j.healun.2014.09.030 |
| [15] | Niroomand A, Qvarnström S, Stenlo M, et al. The role of mechanical ventilation in primary graft dysfunction in the postoperative lung transplant recipient: a single center study and literature review[J]. Acta Anaesthesiol Scand, 2022, 66(4): 483-496. DOI:10.1111/aas.14025 |
| [16] | Tague LK, Bedair B, Witt C, et al. Lung protective ventilation based on donor size is associated with a lower risk of severe primary graft dysfunction after lung transplantation[J]. J Heart Lung Transplant, 2021, 40(10): 1212-1222. DOI:10.1016/j.healun.2021.06.016 |
| [17] | Xuan CH, Gu JX, Xu ZP, et al. A novel nomogram for predicting prolonged mechanical ventilation in lung transplantation patients using extracorporeal membrane oxygenation[J]. Sci Rep, 2024, 14: 11692. DOI:10.1038/s41598-024-62601-2 |
| [18] | Atchade E, Boughaba A, Dinh AT, et al. Prolonged mechanical ventilation after lung transplantation: risks factors and consequences on recipient outcome[J]. Front Med, 2023, 10: 1160621. DOI:10.3389/fmed.2023.1160621 |
| [19] | Gao PG, Li CW, Wu JQ, et al. Establishment of a risk prediction model for prolonged mechanical ventilation after lung transplantation: a retrospective cohort study[J]. BMC Pulm Med, 2023, 23(1): 11. DOI:10.1186/s12890-023-02307-9 |
| [20] | Hadem J, Gottlieb J, Seifert D, et al. Prolonged mechanical ventilation after lung transplantation: a single-center study[J]. Am J Transplant, 2016, 16(5): 1579-1587. DOI:10.1111/ajt.13632 |
| [21] | Benazzo A, Schwarz S, Frommlet F, et al. Donor ventilation parameters as predictors for length of mechanical ventilation after lung transplantation: Results of a prospective multicenter study[J]. J Heart Lung Transplant, 2021, 40(1): 33-41. DOI:10.1016/j.healun.2020.10.008 |
| [22] | Schwarz S, Benazzo A, Dunkler D, et al. Ventilation parameters and early graft function in double lung transplantation[J]. J Heart Lung Transplant, 2021, 40(1): 4-11. DOI:10.1016/j.healun.2020.10.003 |
| [23] | Feltracco P, Milevoj M, Alberti V, et al. Early tracheostomy following lung transplantation[J]. Transplant Proc, 2011, 43(4): 1151-1155. DOI:10.1016/j.transproceed.2011.01.154 |
| [24] | Miyoshi R, Chen-Yoshikawa TF, Hamaji M, et al. Effect of early tracheostomy on clinical outcomes in critically ill lung transplant recipients[J]. Gen Thorac Cardiovasc Surg, 2018, 66(9): 529-536. DOI:10.1007/s11748-018-0949-3 |
| [25] | Chiumello D, Chevallard G, Gregoretti C. Non-invasive ventilation in postoperative patients: a systematic review[J]. Intensive Care Med, 2011, 37(6): 918-929. DOI:10.1007/s00134-011-2210-8 |
| [26] | Ouellette DR, Patel S, Girard TD, et al. Liberation from mechanical ventilation in critically ill adults: an official American college of chest physicians/American thoracic society clinical practice guideline[J]. Chest, 2017, 151(1): 166-180. DOI:10.1016/j.chest.2016.10.036 |
| [27] | Feltracco P, Serra E, Barbieri S, et al. Noninvasive high-frequency percussive ventilation in the prone position after lung transplantation[J]. Transplant Proc, 2012, 44(7): 2016-2021. DOI:10.1016/j.transproceed.2012.05.062 |
| [28] | Feltracco P, Serra E, Barbieri S, et al. Non-invasive ventilation in prone position for refractory hypoxemia after bilateral lung transplantation[J]. Clin Transplant, 2009, 23(5): 748-750. DOI:10.1111/j.1399-0012.2009.01050.x |
| [29] | Rocco M, Conti G, Antonelli M, et al. Non-invasive pressure support ventilation in patients with acute respiratory failure after bilateral lung transplantation[J]. Intensive Care Med, 2001, 27(10): 1622-1626. DOI:10.1007/s001340101063 |
| [30] | 王大鹏, 聂晓伟, 潘红, 等. 经鼻高流量湿化氧疗治疗肺移植术后移植物失功患者的临床研究[J]. 现代生物医学进展, 2017, 17(34): 6709-6712. DOI:10.13241/j.cnki.pmb.2017.34.023 |
| [31] | Roca O, de Acilu MG, Caralt B, et al. Humidified high flow nasal Cannula supportive therapy improves outcomes in lung transplant recipients readmitted to the intensive care unit because of acute respiratory failure[J]. Transplantation, 2015, 99(5): 1092-1098. DOI:10.1097/tp.0000000000000460 |
| [32] | Siddiqui FM, Diamond JM. Lung transplantation for chronic obstructive pulmonary disease: past, present, and future directions[J]. Curr Opin Pulm Med, 2018, 24(2): 199-204. DOI:10.1097/mcp.0000000000000452 |
| [33] | Shehata IM, Elhassan A, Urits I, et al. Postoperative management of hyperinflated native lung in single-lung transplant recipients with chronic obstructive pulmonary disease: a review article[J]. Pulm Ther, 2021, 7(1): 37-46. DOI:10.1007/s41030-020-00141-6 |
| [34] | Pilcher DV, Auzinger GM, Mitra B, et al. Predictors of independent lung ventilation: an analysis of 170 single-lung transplantations[J]. J Thorac Cardiovasc Surg, 2007, 133(4): 1071-1077. DOI:10.1016/j.jtcvs.2006.10.028 |
| [35] | Nocera D, Giovanazzi S, Pozzi T, et al. Does the intensity of therapy correspond to the severity of acute respiratory distress syndrome (ARDS)?[J]. J Clin Med, 2024, 13(23): 7084. DOI:10.3390/jcm13237084 |
| [36] | Yan Y, Xie YP, Chen XB, et al. Mechanical power is associated with weaning outcome in critically ill mechanically ventilated patients[J]. Sci Rep, 2022, 12: 19634. DOI:10.1038/s41598-022-21609-2 |
| [37] | Ghiani A, Kneidinger N, Neurohr C, et al. Mechanical power density predicts prolonged ventilation following double lung transplantation[J]. Transpl Int, 2023, 36: 11506. DOI:10.3389/ti.2023.11506 |
| [38] | Ricoy J, Rodríguez-Núñez N, Álvarez-Dobaño JM, et al. Diaphragmatic dysfunction[J]. Pulmonology, 2019, 25(4): 223-235. DOI:10.1016/j.pulmoe.2018.10.008 |
| [39] | Hu JG, Guo RJ, Li HL, et al. Perioperative diaphragm dysfunction[J]. J Clin Med, 2024, 13(2): 519. DOI:10.3390/jcm13020519 |
| [40] | Supinski GS, Morris PE, Dhar S, et al. Diaphragm dysfunction in critical illness[J]. Chest, 2018, 153(4): 1040-1051. DOI:10.1016/j.chest.2017.08.1157 |
| [41] | Petrof BJ, Jaber S, Matecki S. Ventilator-induced diaphragmatic dysfunction[J]. Curr Opin Crit Care, 2010, 16(1): 19-25. DOI:10.1097/mcc.0b013e328334b166 |
| [42] | Yuan XS, Xue FS, Yu YC, et al. The molecular mechanism of sepsis-induced diaphragm dysfunction[J]. J Thorac Dis, 2023, 15(12): 6831-6847. DOI:10.21037/jtd-23-1680 |
| [43] | Zambon M, Greco M, Bocchino S, et al. Assessment of diaphragmatic dysfunction in the critically ill patient with ultrasound: a systematic review[J]. Intensive Care Med, 2017, 43(1): 29-38. DOI:10.1007/s00134-016-4524-z |
| [44] | Crespo MM, McCarthy DP, Hopkins PM, et al. ISHLT Consensus Statement on adult and pediatric airway complications after lung transplantation: Definitions, grading system, and therapeutics[J]. J Heart Lung Transplant, 2018, 37(5): 548-563. DOI:10.1016/j.healun.2018.01.1309 |
| [45] | Mahajan AK, Folch E, Khandhar SJ, et al. The diagnosis and management of airway complications following lung transplantation[J]. Chest, 2017, 152(3): 627-638. DOI:10.1016/j.chest.2017.02.021 |
| [46] | Duan QR, Zhang YJ, Yang D. Perioperative fluid management for lung transplantation is challenging[J]. Heliyon, 2023, 9(4): e14704. DOI:10.1016/j.heliyon.2023.e14704 |
| [47] | Saugel B, Vincent JL. Cardiac output monitoring: how to choose the optimal method for the individual patient[J]. Curr Opin Crit Care, 2018, 24(3): 165-172. DOI:10.1097/mcc.0000000000000492 |
| [48] | Kim KK, Krause M, Brandes IF, et al. Transesophageal echocardiography for perioperative management in thoracic surgery[J]. Curr Opin Anaesthesiol, 2021, 34(1): 7-12. DOI:10.1097/aco.0000000000000947 |
| [49] | Hahn RT, Abraham T, Adams MS, et al. Guidelines for performing a comprehensive transesophageal echocardiographic examination: recommendations from the American society of echocardiography and the society of cardiovascular anesthesiologists[J]. J Am Soc Echocardiogr, 2013, 26(9): 921-964. DOI:10.1016/j.echo.2013.07.009 |
| [50] | Shaver CM, Ware LB. Primary graft dysfunction: pathophysiology to guide new preventive therapies[J]. Expert Rev Respir Med, 2017, 11(2): 119-128. DOI:10.1080/17476348.2017.1280398 |
| [51] | Pinsky MR, Cecconi M, Chew MS, et al. Effective hemodynamic monitoring[J]. Crit Care, 2022, 26(1): 294. DOI:10.1186/s13054-022-04173-z |
| [52] | Kao CC, Parulekar AD. Postoperative management of lung transplant recipients[J]. J Thorac Dis, 2019, 11(S14): S1782-S1788. DOI:10.21037/jtd.2019.05.60 |
| [53] | Singer M, Deutschman CS, Seymour CW, et al. The third international consensus definitions for sepsis and septic shock (sepsis-3)[J]. Jama, 2016, 315(8): 801. DOI:10.1001/jama.2016.0287 |
| [54] | Marazzato J, Eikermann M, Di Biase L. Management of atrial arrhythmias after lung transplant[J]. JACC Clin Electrophysiol, 2023, 9(8): 1824-1835. DOI:10.1016/j.jacep.2023.01.021 |
| [55] | Hussein AA, Panchabhai TS, Budev MM, et al. Atrial fibrillation and pulmonary venous electrical conduction recovery after full surgical resection and anastomosis of the pulmonary veins[J]. JACC Clin Electrophysiol, 2017, 3(6): 559-567. DOI:10.1016/j.jacep.2016.09.009 |
| [56] | Patel VS, Palmer SM, Messier RH, et al. Clinical outcome after coronary artery revascularization and lung transplantation[J]. Ann Thorac Surg, 2003, 75(2): 372-377. DOI:10.1016/s0003-4975(02)04639-8 |
| [57] | Franz M, Siemeni T, Aburahma K, et al. Lung transplant and severe coronary artery disease: results from a single-centre experience[J]. Eur J Cardio Thorac Surg, 2022, 62(2): ezac348. DOI:10.1093/ejcts/ezac348 |
| [58] | Tran T, Kashem MA, Firoz A, et al. Lung transplant survival with past and concomitant cardiac revascularization[J]. J Heart Lung Transplant, 2023, 42(10): 1334-1340. DOI:10.1016/j.healun.2023.05.007 |
| [59] | Serrao G, Vinayak M, Nicolas J, et al. The evaluation and management of coronary artery disease in the lung transplant patient[J]. J Clin Med, 2023, 12(24): 7644. DOI:10.3390/jcm12247644 |
| [60] | Chaikriangkrai K, Jyothula S, Jhun HY, et al. Impact of pre-operative coronary artery disease on cardiovascular events following lung transplantation[J]. J Heart Lung Transplant, 2016, 35(1): 115-121. DOI:10.1016/j.healun.2015.08.009 |
| [61] | Sinha N, Balayla G, Braghiroli J. Coronary artery disease in lung transplant patients[J]. Clin Transplant, 2020, 34(11): e14078. DOI:10.1111/ctr.14078 |
| [62] | Sherman W, Rabkin DG, Ross D, et al. Lung transplantation and coronary artery disease[J]. Ann Thorac Surg, 2011, 92(1): 303-308. DOI:10.1016/j.athoracsur.2011.04.021 |
| [63] | 范立, 吴波, 卫栋, 等. 肺移植围术期静脉血栓栓塞症的防治与管理[J]. 实用器官移植电子杂志, 2021, 9(5): 411-414. DOI:10.3969/j.issn.2095-5332.2021.05.017 |
| [64] | Kristensen AW, Mortensen J, Berg RMG. Pulmonary thromboembolism as a complication of lung transplantation[J]. Clin Transplant, 2017, 31(4): e12922. DOI:10.1111/ctr.12922 |
| [65] | Oto T, Rabinov M, Griffiths AP, et al. Unexpected donor pulmonary embolism affects early outcomes after lung transplantation: a major mechanism of primary graft failure?[J]. J Thorac Cardiovasc Surg, 2005, 130(5): 1446. DOI:10.1016/j.jtcvs.2005.07.025 |
| [66] | 胡春晓, 王志萍, 许波, 等. 肺移植术中肺动脉高压的麻醉管理[J]. 中华器官移植杂志, 2019, 40(3): 189-192. DOI:10.3760/cma.j.issn.0254-1785.2019.03.017 |
| [67] | Hu CX, Chen WH, He JX, et al. Lung transplantation in China between 2015 and 2018[J]. Chin Med J, 2019, 132(23): 2783-2789. DOI:10.1097/cm9.0000000000000543 |
| [68] | Lease ED, Budev MM. Infectious complications in lung transplant recipients[J]. Thorac Surg Clin, 2022, 32(2): 211-220. DOI:10.1016/j.thorsurg.2021.12.002 |
| [69] | Ahmad O, Shafii AE, Mannino DM, et al. Impact of donor lung pathogenic bacteria on patient outcomes in the immediate post-transplant period[J]. Transpl Infect Dis, 2018, 20(6): e12986. DOI:10.1111/tid.12986 |
| [70] | Liu D, Zhang J, Wu B, et al. Impact of donor lung colonized bacteria detected by next-generation sequencing on early post-transplant outcomes in lung transplant recipients[J]. BMC Infect Dis, 2020, 20(1): 689. DOI:10.1186/s12879-020-05393-w |
| [71] | Kaul DR, Vece G, Blumberg E, et al. Ten years of donor-derived disease: a report of the disease transmission advisory committee[J]. Am J Transplant, 2021, 21(2): 689-702. DOI:10.1111/ajt.16178 |
| [72] | Humphries RM, Abbott AN, Hindler JA. Understanding and addressing CLSI breakpoint revisions: a primer for clinical laboratories[J]. J Clin Microbiol, 2019, 57(6): e00203-e00219. DOI:10.1128/jcm.00203-19 |
| [73] | Shields RK, Clancy CJ, Minces LR, et al. Epidemiology and outcomes of deep surgical site infections following lung transplantation[J]. Am J Transplant, 2013, 13(8): 2137-2145. DOI:10.1111/ajt.12292 |
| [74] | Joean O, Welte T, Gottlieb J. Chest infections after lung transplantation[J]. Chest, 2022, 161(4): 937-948. DOI:10.1016/j.chest.2021.10.014 |
| [75] | Zhang XQ, Lei Y, Tan XL, et al. Optimization of early antimicrobial strategies for lung transplant recipients based on metagenomic next-generation sequencing[J]. Front Microbiol, 2022, 13: 839698. DOI:10.3389/fmicb.2022.839698 |
| [76] | Lian QY, Chen A, Zhang JH, et al. High-throughput next-generation sequencing for identifying pathogens during early-stage post-lung transplantation[J]. BMC Pulm Med, 2021, 21(1): 348. DOI:10.1186/s12890-021-01723-z |
| [77] | Coiffard B, Prud'Homme E, Hraiech S, et al. Worldwide clinical practices in perioperative antibiotic therapy for lung transplantation[J]. BMC Pulm Med, 2020, 20(1): 109. DOI:10.1186/s12890-020-1151-9 |
| [78] | Graziano E, Peghin M, Grossi PA. Perioperative antibiotic stewardship in the organ transplant setting[J]. Transpl Infect Dis, 2022, 24(5): e13895. DOI:10.1111/tid.13895 |
| [79] | Tessier J. A work in progress: antimicrobial stewardship in solid organ transplant patient populations[J]. Curr Opin Infect Dis, 2022, 35(4): 363-369. DOI:10.1097/qco.0000000000000848 |
| [80] | Avery R. Antifungal prophylaxis in lung transplantation[J]. Semin Respir Crit Care Med, 2011, 32(6): 717-726. DOI:10.1055/s-0031-1295719 |
| [81] | Qiao WZ, Zou J, Ping FF, et al. Fungal infection in lung transplant recipients in perioperative period from one lung transplant center[J]. J Thorac Dis, 2019, 11(4): 1554-1561. DOI:10.21037/jtd.2019.03.18 |
| [82] | Pennington KM, Yost KJ, Escalante P, et al. Antifungal prophylaxis in lung transplant: a survey of United States' transplant centers[J]. Clin Transplant, 2019, 33(7): e13630. DOI:10.1111/ctr.13630 |
| [83] | Neoh CF, Snell GI, Kotsimbos T, et al. Antifungal prophylaxis in lung transplantation: a world-wide survey[J]. Am J Transplant, 2011, 11(2): 361-366. DOI:10.1111/j.1600-6143.2010.03375.x |
| [84] | 王文静, 李小杉, 钱婷, 等. 肺移植术后侵袭性真菌感染的危险因素及对术后早期死亡风险的影响分析[J]. 东南大学学报(医学版), 2023, 42(1): 132-139. DOI:10.3969/j.issn.1671-6264.2023.01.019 |
| [85] | Razonable RR, Humar A. Cytomegalovirus in solid organ transplant recipients: Guidelines of the American Society of Transplantation Infectious Diseases Community of Practice[J]. Clin Transplant, 2019, 33(9): e13512. DOI:10.1111/ctr.13512 |
| [86] | Patrucco F, Curtoni A, Sidoti F, et al. Herpes virus infection in lung transplantation: diagnosis, treatment and prevention strategies[J]. Viruses, 2023, 15(12): 2326. DOI:10.3390/v15122326 |
| [87] | Kotton CN, Kumar D, Caliendo AM, et al. International consensus guidelines on the management of cytomegalovirus in solid organ transplantation[J]. Transplantation, 2010, 89(7): 779-795. DOI:10.1097/tp.0b013e3181cee42f |
| [88] | Snyder LD, Finlen-Copeland CA, Turbyfill WJ, et al. Cytomegalovirus pneumonitis is a risk for bronchiolitis obliterans syndrome in lung transplantation[J]. Am J Respir Crit Care Med, 2010, 181(12): 1391-1396. DOI:10.1164/rccm.200911-1786oc |
| [89] | Almaghrabi RS, Omrani AS, Memish ZA. Cytomegalovirus infection in lung transplant recipients[J]. Expert Rev Respir Med, 2017: 1-7. DOI:10.1080/17476348.2017.1317596 |
| [90] | Shigemura N, Sclabassi RJ, Bhama JK, et al. Early major neurologic complications after lung transplantation: incidence, risk factors, and outcome[J]. Transplantation, 2013, 95(6): 866-871. DOI:10.1097/tp.0b013e318280b359 |
| [91] | Pedroso JL, Almeida Dutra L, Braga-Neto P, et al. Neurological complications of solid organ transplantation[J]. Arq Neuro-Psiquiatr, 2017, 75(10): 736-747. DOI:10.1590/0004-282x20170132 |
| [92] | Fischer M, Schmutzhard E. Posterior reversible encephalopathy syndrome[J]. J Neurol, 2017, 264(8): 1608-1616. DOI:10.1007/s00415-016-8377-8 |
| [93] | Leger RF, Silverman MS, Hauck ES, et al. Hyperammonemia post lung transplantation: a review[J]. Clin Med Insights Circ Respir Pulm Med, 2020, 14: 117954842096623. DOI:10.1177/1179548420966234 |
| [94] | Mehta S, Spies C, Shehabi Y. Ten tips for ICU sedation[J]. Intensive Care Med, 2018, 44(7): 1141-1143. DOI:10.1007/s00134-017-4992-9 |
| [95] | 中华医学会急诊医学分会危重症学组, 中国急诊成人镇痛、镇静与谵妄管理专家共识组. 中国急诊成人镇痛、镇静与谵妄管理专家共识[J]. 中华急诊医学杂志, 2023, 32(12): 1594-1609. DOI:10.3760/cma.j.issn.1671-0282.2023.12.004 |
| [96] | King CS, Valentine V, Cattamanchi A, et al. Early postoperative management after lung transplantation: Results of an international survey[J]. Clin Transplant, 2017, 31(7): e12985. DOI:10.1111/ctr.12985 |
| [97] | Potestio C, Jordan D, Kachulis B. Acute postoperative management after lung transplantation[J]. Best Pract Res Clin Anaesthesiol, 2017, 31(2): 273-284. DOI:10.1016/j.bpa.2017.07.004 |
| [98] | Farquhar JM, Smith PJ, Snyder L, et al. Patterns and predictors of pain following lung transplantation[J]. Gen Hosp Psychiatry, 2018, 50: 125-130. DOI:10.1016/j.genhosppsych.2017.11.007 |
| [99] | Loxe SC, de Mello LS, Camara L, et al. Chronic pain after lung transplantation and its impact on quality of life: a 4-year follow-up[J]. Transplant Proc, 2020, 52(5): 1388-1393. DOI:10.1016/j.transproceed.2020.02.032 |
| [100] | Sher Y, Mooney J, Dhillon G, et al. Delirium after lung transplantation: Association with recipient characteristics, hospital resource utilization, and mortality[J]. Clin Transplant, 2017, 31(5): e12966. DOI:10.1111/ctr.12966 |
| [101] | Anderson BJ, Chesley CF, Theodore M, et al. Incidence, risk factors, and clinical implications of post-operative delirium in lung transplant recipients[J]. J Heart Lung Transplant, 2018, 37(6): 755-762. DOI:10.1016/j.healun.2018.01.1295 |
| [102] | 汤铂, 王小亭, 陈文劲, 等. 重症患者谵妄管理专家共识[J]. 中华内科杂志, 2019, 58(2): 108-118. DOI:10.3760/cma.j.issn.0578-1426.2019.02.007 |
| [103] | Barr J, Fraser GL, Puntillo K, et al. Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit[J]. Crit Care Med, 2013, 41(1): 263-306. DOI:10.1097/ccm.0b013e3182783b72 |
| [104] | Atkins BZ, Trachtenberg MS, Prince-Petersen R, et al. Assessing oropharyngeal dysphagia after lung transplantation: altered swallowing mechanisms and increased morbidity[J]. J Heart Lung Transplant, 2007, 26(11): 1144-1148. DOI:10.1016/j.healun.2007.07.038 |
| [105] | Baumann B, Byers S, Wasserman-Wincko T, et al. Postoperative swallowing assessment after lung transplantation[J]. Ann Thorac Surg, 2017, 104(1): 308-312. DOI:10.1016/j.athoracsur.2017.01.080 |
| [106] | Marczin N, de Waal EEC, Hopkins PMA, et al. International consensus recommendations for anesthetic and intensive care management of lung transplantation. An EACTAIC, SCA, ISHLT, ESOT, ESTS, and AST approved document[J]. J Heart Lung Transplant, 2021, 40(11): 1327-1348. DOI:10.1016/j.healun.2021.07.012 |
| [107] | Reintam Blaser A, Malbrain MLNG, Starkopf J, et al. Gastrointestinal function in intensive care patients: terminology, definitions and management. Recommendations of the ESICM Working Group on Abdominal Problems[J]. Intensive Care Med, 2012, 38(3): 384-394. DOI:10.1007/s00134-011-2459-y |
| [108] | Marik PE, Hooper MH. Normocaloric versus hypocaloric feeding on the outcomes of ICU patients: a systematic review and meta-analysis[J]. Intensive Care Med, 2016, 42(3): 316-323. DOI:10.1007/s00134-015-4131-4 |
| [109] | Taylor BE, McClave SA, Martindale RG, et al. Guidelines for the provision and assessment of nutrition support therapy in the adult critically ill patient: society of critical care medicine (SCCM) and American society for parenteral and enteral nutrition (A.S.P.E.N.)[J]. Crit Care Med, 2016, 44(2): 390-438. DOI:10.1097/ccm.0000000000001525 |
| [110] | Wajda-Pokrontka M, Nadziakiewicz P, Krauchuk A, et al. Incidence and perioperative risk factors of acute kidney injury among lung transplant recipients[J]. Transplant Proc, 2022, 54(4): 1120-1123. DOI:10.1016/j.transproceed.2022.02.014 |
| [111] | Botros M, Jackson K, Singh P, et al. Insights into early postoperative acute kidney injury following lung transplantation[J]. Clin Transplant, 2022, 36(4): e14568. DOI:10.1111/ctr.14568 |
| [112] | Xue J, Wang L, Chen CM, et al. Acute kidney injury influences mortality in lung transplantation[J]. Ren Fail, 2014, 36(4): 541-545. DOI:10.3109/0886022x.2013.876350 |
| [113] | Jing L, Chen WH, Zhao L, et al. Acute kidney injury following adult lung transplantation[J]. Chin Med J, 2022, 135(2): 172-180. DOI:10.1097/cm9.0000000000001636 |
| [114] | 江利冰, 蒋守银, 张茂. 围术期与ICU内急性肾损伤管理指南[J]. 中华急诊医学杂志, 2016, 25(7): 862-863. DOI:10.3760/cma.j.issn.1671-0282.2016.07.004 |
| [115] | Lertjitbanjong P, Thongprayoon C, Cheungpasitporn W, et al. Acute kidney injury after lung transplantation: a systematic review and meta-analysis[J]. J Clin Med, 2019, 8(10): 1713. DOI:10.3390/jcm8101713 |
| [116] | Pickkers P, Darmon M, Hoste E, et al. Acute kidney injury in the critically ill: an updated review on pathophysiology and management[J]. Intensive Care Med, 2021, 47(8): 835-850. DOI:10.1007/s00134-021-06454-7 |
| [117] | Spruit MA, Singh SJ, Garvey C, et al. An official American thoracic society/European respiratory society statement: key concepts and advances in pulmonary rehabilitation[J]. Am J Respir Crit Care Med, 2013, 188(8): e13-e64. DOI:10.1164/rccm.201309-1634st |
| [118] | Osadnik CR, Singh S. Pulmonary rehabilitation for obstructive lung disease[J]. Respirology, 2019, 24(9): 871-878. DOI:10.1111/resp.13569 |
| [119] | 曾妃, 梁江淑渊, 兰美娟. 肺移植患者超前过渡期管理方案的构建及应用研究[J]. 中华急诊医学杂志, 2023, 32(5): 691-696. DOI:10.3760/cma.j.issn.1671-0282.2023.05.024 |
| [120] | McCarthy B, Casey D, Devane D, et al. Pulmonary rehabilitation for chronic obstructive pulmonary disease[J]. Cochrane Database Syst Rev, 2015, 2015(4): CD003793. DOI:10.1002/14651858.cd003793.pub3 |
| [121] | Florian J, Rubin A, Mattiello R, et al. Impact of pulmonary rehabilitation on quality of life and functional capacity in patients on waiting lists for lung transplantation[J]. J Bras Pneumol, 2013, 39(3): 349-356. DOI:10.1590/s1806-37132013000300012 |
| [122] | Gloeckl R, Halle M, Kenn K. Interval versus continuous training in lung transplant candidates: a randomized trial[J]. J Heart Lung Transplant, 2012, 31(9): 934-941. DOI:10.1016/j.healun.2012.06.004 |
| [123] | Li M, Mathur S, Chowdhury NA, et al. Pulmonary rehabilitation in lung transplant candidates[J]. J Heart Lung Transplant, 2013, 32(6): 626-632. DOI:10.1016/j.healun.2013.04.002 |
| [124] | Carlin BW, Lega M, Veynovich B. Management of the patient undergoing lung transplantation: an intensive care perspective[J]. Crit Care Nurs Q, 2009, 32(1): 49-57. DOI:10.1097/01.cnq.0000343135.19695.eb |
| [125] | Langer D. Rehabilitation in patients before and after lung transplantation[J]. Respiration, 2015, 89(5): 353-362. DOI:10.1159/000430451 |
| [126] | 蔡英华, 姚勇. 肺移植临床护理实践[M]. 南京东南大学出版社, : 238. |
| [127] | Burtin C, Clerckx B, Robbeets C, et al. Early exercise in critically ill patients enhances short-term functional recovery[J]. Crit Care Med, 2009, 37(9): 2499-2505. DOI:10.1097/ccm.0b013e3181a38937 |
| [128] | Boswell-Ruys CL, Lewis CRH, Wijeysuriya NS, et al. Impact of respiratory muscle training on respiratory muscle strength, respiratory function and quality of life in individuals with tetraplegia: a randomised clinical trial[J]. Thorax, 2020, 75(3): 279-288. DOI:10.1136/thoraxjnl-2019-213917 |
| [129] | Reilly-Spong M, Park T, Gross CR. Poor sleep in organ transplant recipients: self-reports and actigraphy[J]. Clin Transplant, 2013, 27(6): 901-913. DOI:10.1111/ctr.12255 |
| [130] | Fatigati A, Alrawashdeh M, Zaldonis J, et al. Patterns and predictors of sleep quality within the first year after lung transplantation[J]. Prog Transpl, 2016, 26(1): 62-69. DOI:10.1177/1526924816632123 |
| [131] | Sawhney V, Seethamraju H, Bourguet C, et al. Non-respiratory complaints are main reasons for disturbed sleep post lung transplant[J]. Sleep Med, 2020, 70: 106-110. DOI:10.1016/j.sleep.2019.11.1243 |
| [132] | Burkhalter H, Denhaerynck K, Huynh-Do U, et al. Change of sleep quality from pre- to 3 years post-solid organ transplantation: The Swiss Transplant Cohort Study[J]. PLoS One, 2017, 12(10): e0185036. DOI:10.1371/journal.pone.0185036 |
| [133] | Rohde KA, Schlei ZW, Katers KM, et al. Insomnia and relationship with immunosuppressant therapy after lung transplantation[J]. Prog Transpl, 2017, 27(2): 167-174. DOI:10.1177/1526924817699960 |
| [134] | Testelmans D, Schoovaerts K, Belge C, et al. Sleep-disordered breathing after lung transplantation: an observational cohort study[J]. Am J Transplant, 2021, 21(1): 281-290. DOI:10.1111/ajt.16130 |
| [135] | Cordoza M, Koons B, Perlis ML, et al. Self-reported poor quality of sleep in solid organ transplant: a systematic review[J]. Transplant Rev, 2021, 35(4): 100650. DOI:10.1016/j.trre.2021.100650 |
| [136] | Gutiérrez VL, Hirotsu C, Tufik S, et al. Does sleep play a role in the relationship among depression, anxiety, and mortality in lung transplanted patients?[J]. Am J Transplant, 2016, 16(8): 2494. DOI:10.1111/ajt.13825 |
| [137] | Renaud-Picard B, Koutsokera A, Cabanero M, et al. Acute rejection in the modern lung transplant era[J]. Semin Respir Crit Care Med, 2021, 42(3): 411-427. DOI:10.1055/s-0041-1729542 |
| [138] | Todd JL, Neely ML, Kopetskie H, et al. Risk factors for acute rejection in the first year after lung transplant. a multicenter study[J]. Am J Respir Crit Care Med, 2020, 202(4): 576-585. DOI:10.1164/rccm.201910-1915oc |
| [139] | Stewart S, Fishbein MC, Snell GI, et al. Revision of the 1996 working formulation for the standardization of nomenclature in the diagnosis of lung rejection[J]. J Heart Lung Transplant, 2007, 26(12): 1229-1242. DOI:10.1016/j.healun.2007.10.017 |
| [140] | Levy L, Huszti E, Tikkanen J, et al. The impact of first untreated subclinical minimal acute rejection on risk for chronic lung allograft dysfunction or death after lung transplantation[J]. Am J Transplant, 2020, 20(1): 241-249. DOI:10.1111/ajt.15561 |
| [141] | Halverson LP, Hachem RR. Antibody-mediated rejection[J]. Clin Chest Med, 2023, 44(1): 95-103. DOI:10.1016/j.ccm.2022.10.008 |
| [142] | Keller M, Yang S, Ponor L, et al. Preemptive treatment of de novo donor-specific antibodies in lung transplant patients reduces subsequent risk of chronic lung allograft dysfunction or death[J]. Am J Transplant, 2023, 23(4): 559-564. DOI:10.1016/j.ajt.2022.12.019 |
| [143] | 中华医学会器官移植学分会. 中国肺移植免疫抑制治疗及排斥反应诊疗规范(2019版)[J]. 中华移植杂志(电子版), 2019, 13(2): 94-98. DOI:10.3877/cma.j.issn.1674-3903.2019.02.004 |
| [144] | Meyer KC, Raghu G, Verleden GM, et al. An international ISHLT/ATS/ERS clinical practice guideline: diagnosis and management of bronchiolitis obliterans syndrome[J]. Eur Respir J, 2014, 44(6): 1479-1503. DOI:10.1183/09031936.00107514 |
| [145] | Benden C, Haughton M, Leonard S, et al. Therapy options for chronic lung allograft dysfunction–bronchiolitis obliterans syndrome following first-line immunosuppressive strategies: a systematic review[J]. J Heart Lung Transplant, 2017, 36(9): 921-933. DOI:10.1016/j.healun.2017.05.030 |
 2026, Vol. 35
2026, Vol. 35