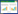脓毒性休克的特征为在充分容量复苏后仍持续存在低血压,需使用血管加压药以维持平均动脉压(mean arterial pressure,MAP)≥65 mmHg,同时伴有血清乳酸水平>2 mmol/L(18 mg/dL)。由此导致的循环、细胞及代谢功能障碍显著增加了患者的病死率[1]。据2017年统计数据,全球约有4 800万例脓毒症病例,约1 100万例死亡与脓毒症相关,约占全球总死亡人数的19.7% [2]。脓毒症已成为全球范围内的重要公共卫生负担。与其他严重应激状态类似,脓毒症患者在疾病早期即表现出明显的高代谢特征。在强烈炎症反应及能量代谢紊乱的共同作用下,患者常出现骨骼肌萎缩、蛋白质分解增强及脂质分解增加[3-4]。营养支持不仅为机体细胞代谢提供能量和必需底物,更重要的是,EN可通过维持肠黏膜屏障完整性、调节机体免疫功能、减轻疾病严重程度,从而改善患者预后并缩短住院时间[4-6]。既往研究表明,EN所产生的生理刺激对于维持胃肠道功能至关重要,尤其在肠道屏障功能、免疫调节及营养物质吸收等方面具有重要作用。此外,肠内营养素可刺激胃肠蠕动并调节胃肠激素分泌,对于维持胃肠动力的完整性同样具有重要意义[4, 6]。目前,多项国际指南均推荐在重症患者中尽早实施EN。欧洲临床营养与代谢学会[7]以及美国肠外肠内营养学会/重症监护医学学会[8]指南均建议在成人重症患者发病后24~48 h内尽早启动EN。然而,最新的ASPEN指南并未明确规定EN启动的具体时间节点[9]。最新发布的第四版《生存脓毒症运动指南》则建议在患者入住ICU后72 h内开始EN治疗[10]。日本脓毒症及脓毒性休克管理临床实践指南则建议在脓毒症急性期(24~48 h内)实施EN[11]。尽管各指南均强调早期EN的重要性,但由于现有研究证据质量有限,脓毒症患者EN的最佳启动时机仍缺乏明确结论。
1 资料与方法 1.1 研究对象本研究为单中心、前瞻性、随机对照试验。研究对象为2024年8月22日至2025年3月31日期间入住中国某三甲医院ICU的脓毒症患者。纳入标准:①年龄大于18岁;②符合Sepsis 3.0标准;③接受EN治疗;④预计在ICU住院时间大于10 d。排除标准:①怀孕或哺乳期;②有神经肌肉疾病病史;③下肢骨折;④良性肿瘤或自身免疫性疾病;⑤曾住院ICU的患者。诊断标准:脓毒症诊断依据《第三国际共识定义脓毒症和脓毒性休克》1中的标准,定义为患者存在感染且序贯器官衰竭评估(sequential organ failure assessment,SOFA)评分≥2。
治疗方案和分组:所有患者均依照国际脓毒症治疗指南进行管理,包括对原发疾病的处理、液体复苏、抗感染治疗、血流动力学管理、机械通气、皮质类固醇使用、CRRT、镇痛和镇静以及血糖管理。患者在确诊脓毒症后,根据是否在48 h内开始EN,被随机分配至EEN组(≤48 h)或DEN组(> 48 h)。随机分组采用分配隐藏方法,在患者入组及随机分配完成前,患者和所有研究人员(包括临床医生和分配人员)均对分组结果保持盲目。随机分配完成后,由于干预措施的性质限制,本研究未实施双盲,临床医生和研究人员知晓患者分组情况。
1.2 数据收集收集患者基线数据,包括年龄、性别、体重指数(BMI)、查尔森合并症指数(Charlson Comorbidity Index,CCI)以及感染部位。在脓毒症诊断后的24 h内,记录最严重的急性生理学与慢性健康评估(APACHE)Ⅱ评分和SOFA评分。实验室检查包括白细胞计数(WBC)、血红蛋白(Hb)、C反应蛋白(CRP)、降钙素原(PCT)、白蛋白(ALB)、前白蛋白(PA)和血清肌酐(SCr)。关于营养支持,记录营养途径、初始NUTRIC评分,并在EN的第3、7、14天评估实际每日能量(kcal/d)和蛋白质(g/d)摄入量,以及目标摄入量的百分比。为了评估营养干预对肌肉质量的影响,我们在EN的第1天和第14天使用超声测量股四头肌厚度(quadriceps thickness,QT)和膈肌厚度(diaphragm thickness,DT),并在同一天评估白细胞介素-6(IL-6)水平。此外,整个研究期间,我们密切监测并记录了胃肠道不耐受的相关症状,包括肠鸣音缺失或异常、呕吐、腹胀、胃残余量大于250 mL、胃肠道出血及腹泻[12]。
本研究的主要终点为30 d全因病死率。次要终点包括ICU病死率、抗生素使用时间、机械通气时间、血管加压药使用时间、CRRT时间、ICU住院时间(length of stay,LOS)以及总住院时间(total LOS)。
DT测量方法:采用高频(7~13 MHz)线阵探头,放置在第8和第9肋间隙之间,大致位于腋前线和腋中线之间,指示点指向患者头部。使用2D模式,识别超声图像中的膈肌。膈肌位于胸膜(浅回声层)和腹膜(更深的回声层)之间,表现为低回声的肌肉层。由两名经过统一培训的临床医生独立测量膈肌厚度,并取两次测量的平均值作为最终结果[13-14]。
QT测量方法:采用高频线阵探头,避免对肌肉施加过大压力。将探头置于髌骨与髂前上棘连线的2/3处,尽量与股骨表面长轴垂直。股四头肌包括股内侧肌、股中间肌、股外侧肌和股直肌。肌肉厚度定义为两层筋膜之间的距离[15]。
1.3 统计学方法使用SPSS 26.0版本进行统计分析。数据的正态性通过Shapiro-Wilk检验评估,方差齐性通过Levene检验进行检验。连续变量以均值±标准差(x±s)或中位数(四分位间距)表示,分类变量则通过频率和百分比描述。对正态分布的连续变量,采用Student' s t检验进行组间比较;对非正态分布的连续变量,采用Mann-Whitney U检验。分类变量的组间比较使用χ2检验(Chi-square test)。对于具有重复测量的组内比较,采用方差分析(ANOVA)。使用R 4.0.0或更高版本生成Kaplan-Meier生存曲线,以比较两组的28 d生存率。以P < 0.05为差异有统计学意义。
2 结果从2024年8月22日至2025年3月31日,共有262名被诊断为脓毒症的患者。在这些患者中,173名因ICU住院时间不足10 d、3名因神经肌肉疾病、1名因下肢骨折、10名因活动性恶性肿瘤或自身免疫性疾病、6名因曾经住院过ICU而被排除。最终,68名患者接受了EN治疗,其中34名患者被随机分配至EEN组,34名患者被分配至DEN组(见图 1)。
|
| 图 1 纳入流程图 Fig 1 Study inclusion flow chart |
|
|
表 1总结了EEN组和DEN组患者的一般特征。值得注意的是,与EEN组相比,DEN组中接受鼻胃-空肠喂养管的患者比例较高(5.9% vs. 26%,P = 0.021),但其他特征差异无统计学意义。
| 指标 | EEN(n = 34) | DEN(n = 34) | P值 |
| 男性(%) | 19(56) | 20(59) | 0.806 |
| 年龄(岁) | 67.82 ± 13.04 | 71.09 ± 12.51 | 0.296 |
| BMI(kg/m2) | 22.23 ± 4.20 | 21.88 ± 3.65 | 0.715 |
| CCI | 4(3, 5) | 4.5(3.75, 5) | 0.753 |
| APACHE Ⅱ | 18(12, 26) | 16(12, 22) | 0.360 |
| SOFA | 5(4, 7) | 6(5, 8) | 0.125 |
| NUTRIC | 4(3,6) | 5(4,5) | 0.676 |
| 营养途径(%) | 0.021 | ||
| 鼻胃-空肠营养管 | 9(26) | 2(5.9) | |
| 鼻-胃管 | 25(74) | 32(94) | |
| 感染部位(%) | |||
| 肺部感染 | 31(91) | 31(91) | 1.000 |
| 腹部感染 | 1(3) | 3(9) | 0.303 |
| 泌尿道感染 | 9(26.) | 7(21) | 0.567 |
| 导管相关血流感染 | 2(6) | 3(9) | 0.642 |
| 皮肤、软组织感染 | 1(3) | 2(6) | 0.555 |
| 颅内感染 | 0 | 1(3) | 0.314 |
| 不确定 | 2(6) | 4(12) | 0.393 |
| WBC(×109/L) | 12.40(9.31, 18.14) | 12.06(8.98, 15.97) | 0.659 |
| Hb(g/L) | 119.62 ± 27.70 | 115.91 ± 31.43 | 0.608 |
| ALB(g/L) | 30.21 ± 6.26 | 30.28 ± 5.54 | 0.961 |
| PA(mg/dL) | 10.35(5.65, 15.65) | 10.15(6.45, 14.30) | 0.888 |
| SCr(μmol/L) | 68.00(43.75, 186.50) | 86.50(54.00, 125.75) | 0.239 |
| PCT(ng/mL) | 10.43 ± 23.05 | 19.06 ± 30.71 | 0.194 |
| CRP(mg/L) | 130.13(42.30, 231.73) | 115.95(51.83, 175.10) | 0.484 |
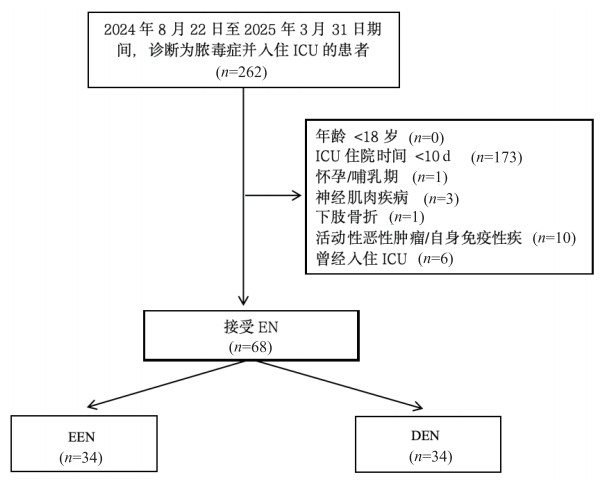
Kaplan-Meier生存曲线(图 2)比较了EEN组和DEN组之间的生存概率。随着时间的推移,两组的生存概率较为接近,且未观察到显著差异。P值为0.498(HR = 2,95%CI: 0.26 ~ 15.36),表明EEN组和DEN组之间的生存率差异无统计学意义。
|
| 图 2 两组患者在30 d时的Kaplan-Meier生存曲线 Fig 2 Kaplan-Meier survival curves of the two groups of patients at 30 days |
|
|
| 指标 | EEN(n = 34) | DEN(n = 34) | P值 |
| Day3-能量(kcal) | 923(650, 1 225) | 650(650, 1 000) | 0.389 |
| Day3-能量(%) | 60(45, 75) | 54(46, 76) | 0.806 |
| Day3-蛋白质(g) | 39(29, 59) | 40(29, 59) | 0.635 |
| Day3-蛋白质(%) | 48(32, 84) | 53(35, 70) | 0.830 |
| Day7-能量(kcal) | 1 300(900, 1 300) | 1 000(650, 1 300) | 0.186 |
| Day7-能量(%) | 76(60, 93) | 70(46, 92) | 0.361 |
| Day7-蛋白质(g) | 58(34, 60) | 58(34, 60) | 0.834 |
| Day7-蛋白质(%) | 61(44, 82) | 65(43, 86) | 0.787 |
| Day14-能量(kcal) | 1 300(946, 1 350) | 1 300(1 000, 1 500) | 0.937 |
| Day14-能量(%) | 90(67, 100) | 90(0.66, 100) | 0.822 |
| Day14-蛋白质(g) | 59(47, 76) | 59(40, 86) | 0.875 |
| Day14-蛋白质(%) | 71(53, 87) | 75(57, 94) | 0.509 |
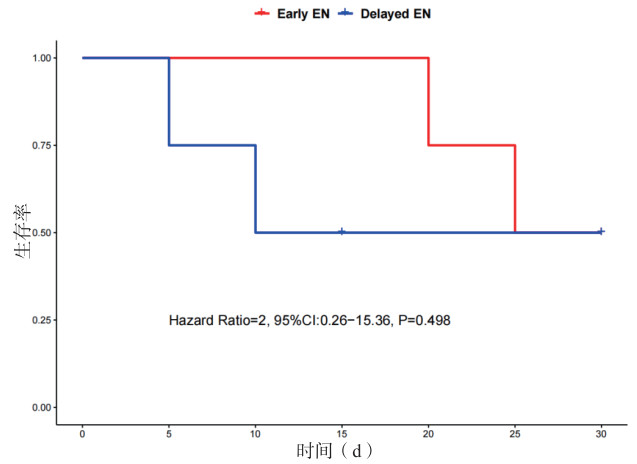
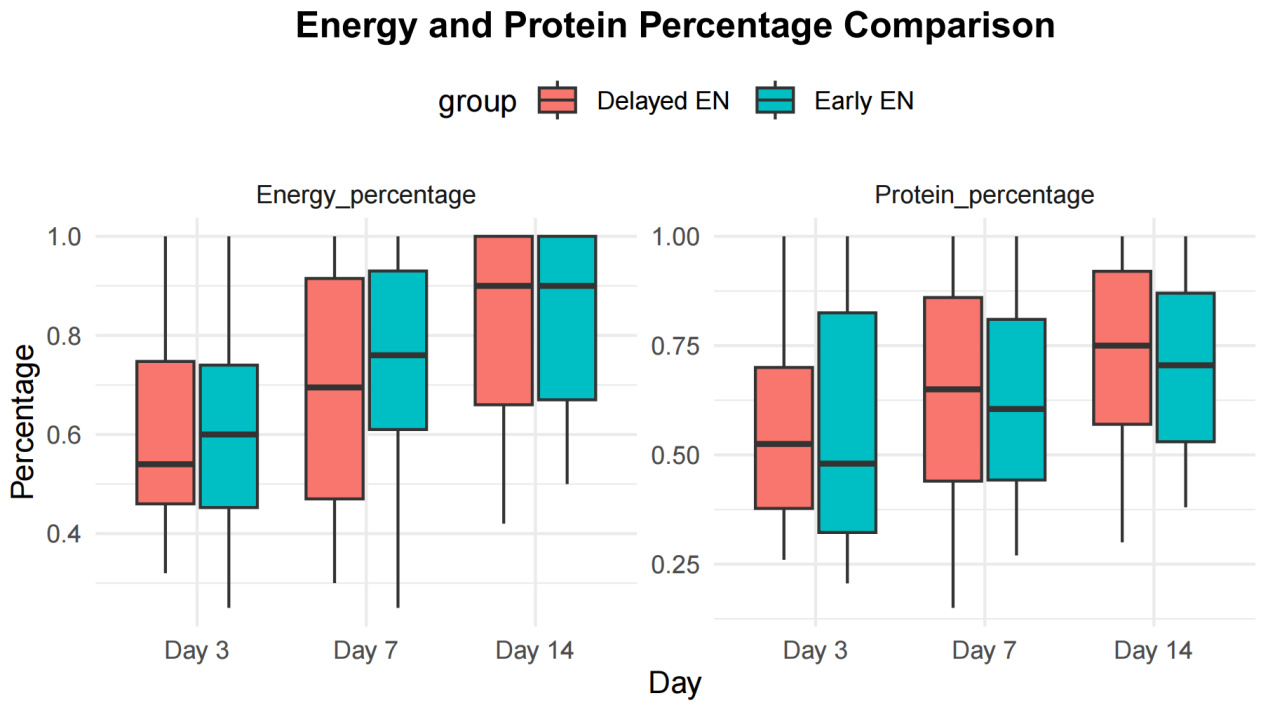
表 3比较了EEN组和DEN组在第3天、第7天和第14天的能量和蛋白质摄入量。第3天,EEN组的摄入量为60%(45%~75%),DEN组为54%(46%~76%);第7天,EEN组为76%(60%~93%),DEN组为70%(46%~92%);第14天,两组均达到90%(EEN组为67%~100%,DEN组为66%~100%)。对于蛋白质,第3天,EEN组为48%(32%~84%),DEN组为53%(35%~70%);第7天,EEN组为61%(44%~82%),DEN组为65%(43%~86%);第14天,EEN组为71%(53%~87%),DEN组为75%(57%~94%)。结果显示,在任何时间点,两组之间的差异均无统计学意义(P > 0.05)。箱线图(图 3)展示了EEN组和DEN组在第3天、第7天和第14天的能量和蛋白质摄入百分比的比较。
| 症状(%) | EEN(n =34) | DEN(n =34) | P值 |
| 腹胀 | 9(26.57) | 2(6) | 0.045 |
| 肠鸣音消失或异常 | 11(32) | 7(21) | 0.410 |
| 腹泻 | 4(12) | 3(9) | 1.000 |
| 胃残余量 > 250 mL | 5(15) | 1(3) | 0.197 |
| 胃肠道出血 | 5(15) | 2(6) | 0.427 |
| 呕吐 | 5(15) | 3(9) | 0.709 |
|
| 图 3 EEN组和DEN组在第3天、第7天和第14天的能量和蛋白质对比 Fig 3 Comparison of energy and protein between the EEN group and the DEN group on day 3, day 7 and day 14 |
|
|
表 3比较了EEN组和DEN组在胃肠道不耐受方面的差异。EEN组腹胀的发生率高于DEN组(27% vs. 65.8%,P = 0.045)。然而,两组在肠鸣音缺失或异常、腹泻、胃残留、胃肠道出血和呕吐方面差异无统计学意义(P > 0.05)。
QT和DT在两组间于第1天及第14天比较差异无统计学意义(均 P > 0.05)。同样地,第1天和第14天两组IL-6水平差异亦无统计学意义(均 P > 0.05)。
对于QT和DT,重复测量方差分析显示,两组之间的差异无统计学意义(P = 0.330,P = 0.829),而两个时间点之间的差异具有统计学意义(P = 0.008,P = 0.009)。组与时间之间的交互作用也无统计学意义(P = 0.510,P = 0.085)(表 4~6)。
| 指标 | EEN(n =25) | DEN(n =27) | P值 |
| QT(Day 1, cm) | 1.67±0.75 | 1.73±0.60 | 0.716 |
| QT(Day 14, cm) | 1.25±0.33 | 1.40±0.37 | 0.129 |
| DT(Day 1, cm) | 1.22±0.33 | 1.16±.0.39 | 0.473 |
| DT(Day 14, cm) | 1.01±0.20 | 1.08±0.27 | 0.294 |
| IL-6(Day 1, pg/mL) | 1529.17(832.68, 2225.66) | 1618.94(698.89, 2538.98) | 0.371 |
| IL-6(Day 14, pg/mL) | 15.51(12.33, 18.70) | 15.07(9.03, 21.1) | 0.897 |
| 因素 | df | F Value | P值 | Partial Eta Squared(η2) |
| 时间 | 1, 50 | 7.668 | 0.008 | 0.133 |
| 组别 | 1, 50 | 0.966 | 0.330 | 0.019 |
| 时间和组别交互 | 1, 50 | 0.439 | 0.510 | 0.009 |
| 因素 | df | F Value | P值 | Partial Eta Squared(η2) |
| 时间 | 1, 50 | 7.501 | 0.009 | 0.130 |
| 组别 | 1, 50 | 0.047 | 0.829 | 0.001 |
| 时间和组别交互 | 1, 50 | 3.082 | 0.085 | 0.058 |
一项系统综述和Meta分析发现,尽管在48 h内接受EEN的患者住院病死率较低(OR = 0.69,95% CI: 0.39~1.23 vs. OR=0.89,95% CI: 0.69~1.13),但这种差异无统计学意义[16]。基于MIMIC-Ⅳ数据库的回顾性分析表明,在脓毒症患者中,EEN(在72 h内启动)并未显著降低28 d或60 d病死率,但可能缩短ICU住院时间[17]。这一发现与本研究结果一致。本研究最终表明,无论是脓毒症诊断后48 h内开始的EEN,还是48 h后开始的DEN,都与30 d病死率无显著关系。然而,与DEN组相比,EEN组患者的住院时间明显较短,这表明EN的启动时机对30 d病死率的影响可能有限。这一发现也与其他研究一致[16-19]。McKeever等[20]指出,关于肠内营养开始时间的定义,“早期”应指急性重症疾病中的分解代谢阶段,而“晚期”应指恢复阶段,无论这一阶段发生在患者入住ICU的哪一天。
在本研究中,EEN组的胃肠道不耐受较为常见,腹胀发生率显著高于DEN组。这一结果可能与EN对肠道的刺激作用有关,因为在营养供给期间,患者的胃肠功能尚未完全恢复,可能导致胃肠不适。尽管如此,在腹泻、呕吐或胃残留物等其他胃肠道症状方面,未观察到两组之间的显著差异,表明早期和延迟EN对这些症状的影响相似。此外,DEN组患者鼻胃-空肠管置入的频率更高。这些发现与一项系统综述和荟萃分析的结果一致,该分析报告称,EEN组腹泻的发生频率有所增加(OR=2.23,95%CI: 1.115~4.34)[16]。这些数据表明,在重症患者接受EN时,胃肠道功能障碍是一个显著问题。
在本研究中,EEN组和DEN组的热量摄入总体符合ESPEN的建议。然而,蛋白质摄入量较低,尽管如此,两组在第3天、第7天和第14天的热量和蛋白质摄入比例相对稳定,并达到了ESPEN推荐的目标。这一结果与EuroPN研究的发现一致,后者报告称,ICU患者达到了ESPEN推荐的热量目标的83%(59%~107%)和蛋白质目标的65%(41%~91%),而早期适度的热量和蛋白质摄入与临床结果的改善相关,尤其是与成功脱离呼吸机及较低的死亡风险相关[21]。这一结果强调了在重症患者中,适当的营养支持,尤其是蛋白质的摄入,对于临床预后具有重要影响。
尽管两组在股四头肌和膈肌厚度方面没差异有统计学意义,但在第1天和第14天观察到明显的肌肉流失趋势,这可能与ICU获得性虚弱相关[22-23]。同样,IL-6也呈现出类似的变化模式。这表明,EEN并未显著改善肌肉质量或全身炎症反应,进一步表明这种干预对这些结果可能没有实质性影响。然而,一项干预性研究发现,在第7天,EEN组的IL-6水平显著低于DEN组(P < 0.001)[20]。另外,一项回顾性研究显示,在患有肌肉减少症的患者中,接受EEN治疗的患者与未接受EEN治疗的患者相比,住院病死率显著更低(9% vs. 34%,P = 0.005),提示EEN在这一患者群体中可能具有潜在的重要性[21]。同样的,另外一项回顾性研究也显示,在存在营养不良风险的危重症患者中,EEN可延缓ICU获得性虚弱的发生[24]。然而,我们的研究未能得出这一结论,因此,未来仍需前瞻性随机对照研究,以进一步明确EEN在ICU获得性虚弱预防和管理中的真实作用[25-26]。
在本研究中,尽管EEN未显著影响30 d病死率,但与DEN相比,EEN组的住院时间明显缩短。
然而,本研究存在一定的局限性。首先,这是一项单中心临床研究,样本量较小,这限制了其结果的外部推广性。其次,随访时间较短,且未评估长期预后指标。因此,未来需要开展前瞻性、多中心、大样本的随机对照试验来评估EEN对脓毒症患者预后的影响,从而制定最佳的营养治疗策略。
利益冲突 所有作者声明无利益冲突
作者贡献声明 张凤:研究设计、数据收集及整理、统计学分析和论文撰写;张利鹏:研究设计、论文修改
伦理 该研究方案已获得内蒙古医科大学附属医院伦理委员会批准(批准号:KY2024029 - 修订版01),并在中国临床试验注册中心注册(注册号:ChiCTR2500100864)。所有参与者在研究开始前已签署知情同意书
| [1] | Singer M, Deutschman CS, Seymour CW, et al. The third international consensus definitions for sepsis and septic shock (sepsis-3)[J]. Jama, 2016, 315(8): 801. DOI:10.1001/jama.2016.0287 |
| [2] | Rudd KE, Johnson SC, Agesa KM, et al. Global, regional, and national sepsis incidence and mortality, 1990–2017: analysis for the Global Burden of Disease Study[J]. Lancet, 2020, 395(10219): 200-211. DOI:10.1016/s0140-6736(19)32989-7 |
| [3] | Wischmeyer PE. Nutrition therapy in sepsis[J]. Crit Care Clin, 2018, 34(1): 107-125. DOI:10.1016/j.ccc.2017.08.008 |
| [4] | Xu FC, Lu G, Wang J. Enhancing sepsis therapy: the evolving role of enteral nutrition[J]. Front Nutr, 2024, 11: 1421632. DOI:10.3389/fnut.2024.1421632 |
| [5] | McClave SA, Taylor BE, Martindale RG, et al. Guidelines for the provision and assessment of nutrition support therapy in the adult critically ill patient: society of critical care medicine (SCCM) and American society for parenteral and enteral nutrition (A.S.P.E.N.)[J]. J Parenter Enteral Nutr, 2016, 40(2): 159-211. DOI:10.1177/0148607115621863 |
| [6] | Schörghuber M, Fruhwald S. Effects of enteral nutrition on gastrointestinal function in patients who are critically ill[J]. Lancet Gastroenterol Hepatol, 2018, 3(4): 281-287. DOI:10.1016/s2468-1253(18)30036-0 |
| [7] | Singer P, Blaser AR, Berger MM, et al. ESPEN guideline on clinical nutrition in the intensive care unit[J]. Clin Nutr, 2019, 38(1): 48-79. DOI:10.1016/j.clnu.2018.08.037 |
| [8] | Martindale RG, McClave SA, Vanek VW, et al. Guidelines for the provision and assessment of nutrition support therapy in the adult critically ill patient: Society of Critical Care Medicine and American Society for Parenteral and Enteral Nutrition: Executive Summary[J]. Crit Care Med, 2009, 37(5): 1757-1761. DOI:10.1097/ccm.0b013e3181a40116 |
| [9] | Compher C, Bingham AL, McCall M, et al. Guidelines for the provision of nutrition support therapy in the adult critically ill patient: The American Society for Parenteral and Enteral Nutrition[J]. J Parenter Enteral Nutr, 2022, 46(1): 12-41. DOI:10.1002/jpen.2267 |
| [10] | Evans L, Rhodes A, Alhazzani W, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021[J]. Crit Care Med, 2021, 49(11): e1063-e1143. DOI:10.1097/ccm.0000000000005337 |
| [11] | Egi M, Ogura H, Yatabe T, et al. The Japanese clinical practice guidelines for management of sepsis and septic shock 2020 (J-SSCG 2020)[J]. Acute Med Surg, 2021, 8: e659. DOI:10.1002/ams2.659 |
| [12] | Reintam Blaser A, Malbrain MLNG, Starkopf J, et al. Gastrointestinal function in intensive care patients: terminology, definitions and management. Recommendations of the ESICM Working Group on Abdominal Problems[J]. Intensive Care Med, 2012, 38(3): 384-394. DOI:10.1007/s00134-011-2459-y |
| [13] | Vieira Santana P, Zumpano Cardenas L, Pereira de Albuquerque AL, et al. Diaphragmatic ultrasound: a review of its methodological aspects and clinical uses[J]. J Bras Pneumol, 2020, 46(6): e20200064. DOI:10.36416/1806-3756/e20200064 |
| [14] | Cheong I, Marcelo Tamagnone F. Comparative evaluation of diaphragmatic excursion in ICU patients: ultrasonography assessment via the conventional M-mode versus the anatomical M-mode[J]. World J Emerg Med, 2025, 16(5): 488. DOI:10.5847/wjem.j.1920-8642.2025.090 |
| [15] | Tillquist M, Kutsogiannis DJ, Wischmeyer PE, et al. Bedside ultrasound is a practical and reliable measurement tool for assessing quadriceps muscle layer thickness[J]. J Parenter Enteral Nutr, 2014, 38(7): 886-890. DOI:10.1177/0148607113501327 |
| [16] | Grillo-Ardila CF, Tibavizco-Palacios D, Triana LC, et al. Early enteral nutrition (within 48 h) for patients with sepsis or septic shock: a systematic review and meta-analysis[J]. Nutrients, 2024, 16(11): 1560. DOI:10.3390/nu16111560 |
| [17] | Xu FC, Xu JX, Ma JJ, et al. Early versus delayed enteral nutrition in ICU patients with sepsis: a propensity score-matched analysis based on the MIMIC-Ⅳ database[J]. Front Nutr, 2024, 11: 1370472. DOI:10.3389/fnut.2024.1370472 |
| [18] | Ohbe H, Jo T, Matsui H, et al. Early enteral nutrition in patients with severe traumatic brain injury: a propensity score–matched analysis using a nationwide inpatient database in Japan[J]. Am J Clin Nutr, 2020, 111(2): 378-384. DOI:10.1093/ajcn/nqz290 |
| [19] | Ortiz-Reyes L, Patel JJ, Jiang XR, et al. Early versus delayed enteral nutrition in mechanically ventilated patients with circulatory shock: a nested cohort analysis of an international multicenter, pragmatic clinical trial[J]. Crit Care, 2022, 26(1): 173. DOI:10.1186/s13054-022-04047-4 |
| [20] | McKeever L, Peterson SJ, Lateef O, et al. The influence of timing in critical care nutrition[J]. Annu Rev Nutr, 2021, 41: 203-222. DOI:10.1146/annurev-nutr-111120-114108 |
| [21] | Matejovic M, Huet O, Dams K, et al. Medical nutrition therapy and clinical outcomes in critically ill adults: a European multinational, prospective observational cohort study (EuroPN)[J]. Crit Care, 2022, 26(1): 143. DOI:10.1186/s13054-022-03997-z |
| [22] | Vanhorebeek I, Latronico N, Van den Berghe G. ICU-acquired weakness[J]. Intensive Care Med, 2020, 46(4): 637-653. DOI:10.1007/s00134-020-05944-4 |
| [23] | Chen J, Huang M. Intensive care unit-acquired weakness: Recent insights[J]. J Intensive Med, 2024, 4(1): 73-80. DOI:10.1016/j.jointm.2023.07.002 |
| [24] | Zheng QL, Liu CY, Le LY, et al. ICU-acquired weakness in critically ill patients at risk of malnutrition: risk factors, biomarkers, and early enteral nutrition impact[J]. World J Emerg Med, 2025, 16(1): 51. DOI:10.5847/wjem.j.1920-8642.2025.020 |
| [25] | 李俊玉, 王国栋, 商娜, 等. 急诊老年患者衰弱预测模型的建立与验证[J]. 中华急诊医学杂志, 2025, 34(2): 226-232. DOI:10.3760/cma.j.issn.1671-0282.2025.02.015 |
| [26] | 刘慧珍, 王国栋, 商永, 等. 三种衰弱筛查量表对急诊科老年患者预后预测效能的比较[J]. 中华急诊医学杂志, 2025, 34(1): 55-61. DOI:10.3760/cma.j.issn.1671-0282.2025.01.009 |
 2026, Vol. 35
2026, Vol. 35