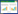脓毒症是机体感染所引发的过度炎症反应,依据病情严重程度可分为脓毒症和脓毒症休克,其中脓毒症休克的病情尤为凶险,其发病率高达30%~50%[1]。脓毒症休克的病理机制复杂,涉及炎症反应失衡、免疫功能紊乱及凝血功能障碍等多个环节[2-3]。在脓毒症休克的发展过程中,心功能障碍的发生较为常见,不仅直接损害心脏的泵血功能、加重全身组织的灌注不足;还会显著增加患者的死亡风险,延长住院时间,增加医疗成本[4]。脓毒症休克合并心功能障碍的发病率和病死率较高,给临床治疗带来了巨大困难。因此,探究脓毒症休克合并心功能障碍的影响因素,有助于临床医生早期识别高危患者,进而制定个性化的治疗方案,提高治疗效果。此外,建立有效的预测模型可为临床决策提供科学、可靠的依据,有助于合理分配医疗资源,优化治疗流程。本研究探索脓毒症休克合并心功能障碍的独立影响因素并建立预测模型,为其临床早期诊断和治疗提供理论依据和实践指导。
1 资料与方法 1.1 研究对象前瞻性收集2021年3月至2024年10月于本院就诊的脓毒症休克患者,纳入和排除标准:纳入标准:①经诊断确诊为脓毒症休克患者;②患者临床资料完整;③患者及家属签署知情同意书且配合治疗。排除标准:①年龄 < 18岁或 > 80岁;②既往存在心功能不全、心肌病、冠状动脉粥样硬化性心脏病;③患有急性或慢性肾脏疾病;④患有恶性肿瘤或严重自身免疫疾病。
样本量计算式[5]:
其中设定Z=1.96,δ=0.1p,p取0.30~0.50[1],经计算,N的取值范围为384~896。本研究最终纳入390例脓毒症休克患者,按照7:3将患者随机(随机数字法)分为模型组(n=273)和验证组(n=117)[6],模型组用于构建脓毒症休克合并心功能障碍预测模型与内部验证,验证组用于确认列用于模型外部验证与诊断效能对比分析。本研究已获得本院伦理委员会批准(审批号:2021-01-KY004),且患者均签署知情同意书。
1.2 诊断标准脓毒症休克诊断标准:依据谭睿等[7]的诊断标准:①明确或疑似感染;②序贯器官衰竭评分(sequential organ failure assessment,SOFA)≥2分;③需服用血管活性药物以维持平均动脉压(mean arterial pressure,MAP) > 65 mmHg;④乳酸(lactate,Lac)≥2 mmol/L。心功能障碍诊断标准:参考李佳卓等[8]的诊断标准:入院24 h内的超声心电图结果提示左(右)心室收缩或舒张功能障碍且左心室射血分数 < 0.50或患者左心室射血分数≥0.50但在超声心动图数据有左(右)心室功能减退或整体左(右)心室收缩功能障碍。依据是否发生心功能障碍,将模型组分为心功能障碍组(n=74)与非心功能障碍组(n=199)。
1.3 指标观察(1)一般资料:入院时记录患者的性别、年龄、体质指数(body mass index,BMI)、糖尿病史及高血压史;(2)实验室检测指标:记录患者收缩压、舒张压、MAP、心率;入院12 h内采集患者静脉血,采用全自动生化仪(Siemens,德国)检测:白细胞计数(whiteblood cell count,WBC)、降钙素原(procalcitonin,PCT)、C反应蛋白(C-reactive protein,CRP)、Lac、白介素-6(interleukin-6,IL-6)、肌酸激酶(creatine kinase,CK)、肌酸激酶MB同工酶(creatine kinase-MB,CK-MB)、脑钠肽(brian natriureticpeptide,BNP)及N末端前体脑钠肽(N-terminal pro-brain natriuretic peptide,NT-proBNP)。(3)超声心动图指标:纳入患者均于入院重症监护室(intensive care unit,ICU)24 h内进行超声心动图检查,使用超声设备(Philips,美国),S5-1探头进行心脏检查,测量舒张早期二尖瓣峰值血流速度(E峰)、舒张晚期二尖瓣峰值血流速度(A峰)及舒张早期二尖瓣峰值血流速度/二尖瓣环舒张早期心肌运动速度(E/e')。(4)病情程度评估:急性生理学与慢性健康状况评分Ⅱ(acutephysiologyand chronic health evaluationⅡ,APACHEⅡ)及SOFA。(5)预后指标:ICU病死率、住院病死率、气管插管率、急性肾损伤(acute kidney injury,AKI)发生率、新发房颤发生率(住院期间任何被记录到的房颤)、连续性肾脏替代治疗(continuous renal replacement therapy,CRRT)率、住ICU时间及住院时间。
1.4 统计学方法采用SPSS 26.0和R语言软件进行数据分析,计数资料用频数(百分比)表示,两组间比较采用χ2;符合正态分布计量资料用均数±标准差(x±s)表示,两组间比较采用独立样本t检验;不符合正态分布计量资料用[M(Q1, Q3)]表示,两组间比较采用非参数检验秩和检验(Mann-Whitney U检验)。采用LASSO回归、Logistic回归及森林图分析脓毒症休克患者合并心功能障碍的影响因素,通过受试者工作特征(receiver operating characteristic,ROC)曲线和校准曲线评估预测模型的分辨力及校准度。以P < 0.05为差异有统计学意义。
2 结果 2.1 模型组与验证组临床资料比较共纳入390例脓毒症休克患者,筛选流程见图 1。模型组和验证组间临床资料比较,性别、年龄、BMI、糖尿病史、高血压史、收缩压、舒张压、MAP、心率、WBC、PCT、CRP、Lac、IL-6、CK、CK-MB)、BNP、NT-proBNP、E峰、A峰、E/e’、APACHEⅡ及SOFA均差异无统计学意义(P > 0.05),见表 1。
|
| 图 1 研究对象筛选流程图 Fig 1 Flowchart of participants inclusion |
|
|
| 变量 | 模型组(n=273) | 验证组(n=117) | χ2/Z/t | P值 |
| 性别(男)a | 119(43.6) | 53(45.3) | 0.097 | 0.755 |
| 年龄(岁)b | 64(61, 67) | 64(61, 67.5) | 0.563 | 0.574 |
| BMI(kg/m2)b | 22.56(20.75, 24.21) | 22.23(20.38, 24.23) | 0.230 | 0.818 |
| 糖尿病a | 129(47.3) | 55(47.0) | 0.002 | 0.965 |
| 高血压a | 130(47.6) | 47(40.2) | 1.833 | 0.176 |
| 收缩压(mmHg)c | 90.74±20.98 | 89.15±20.77 | 0.688 | 0.492 |
| 舒张压(mmHg)c | 65.91±8.84 | 65.57±8.33 | 0.353 | 0.724 |
| MAP(mmHg)c | 87.23±12.83 | 85.59±14.51 | 1.112 | 0.267 |
| 心率(次/min)b | 106(95, 119) | 106(95, 124) | 0.406 | 0.684 |
| WBC(×109L)c | 16.10±5.38 | 15.85±4.95 | 0.430 | 0.667 |
| PCT(ng/mL)b | 10.96(9.43, 12.14) | 11.11(9.91, 12.42) | 1.416 | 0.157 |
| CRP(mg/L)b | 252.51(232.23, 278.67) | 249.99(232.84, 264.14) | 0.843 | 0.399 |
| Lac(mmol/L)c | 4.68±0.66 | 4.70±0.60 | 0.158 | 0.875 |
| IL-6(pg/mL)c | 172.37±21.00 | 173.70±20.04 | 0.579 | 0.563 |
| CK(U/L)b | 226.09(208.84, 263.20) | 221.73(204.99, 264.37) | 0.662 | 0.508 |
| CK-MB(U/L)c | 27.33±6.71 | 26.55±4.24 | 1.174 | 0.241 |
| BNP(ng/mL)b | 0.63(0.57, 0.69) | 0.64(0.56, 0.70) | 0.086 | 0.931 |
| NT-proBNP(ng/mL)b | 0.66(0.42, 0.98) | 0.68(0.48, 0.95) | 1.035 | 0.301 |
| E峰(m/s)c | 0.81±0.22 | 0.80±0.21 | 0.358 | 0.720 |
| A峰(m/s)b | 0.61(0.46, 0.81) | 0.62(0.49, 0.76) | 0.241 | 0.809 |
| E/e’ c | 11.64±1.99 | 11.74±1.98 | 0.490 | 0.625 |
| APACHEⅡ(分)b | 19(15, 23) | 18(16, 22) | 0.133 | 0.894 |
| SOFA(分)b | 12(10, 14) | 13(10, 14.5) | 0.980 | 0.327 |
| 注:a为(频数,百分比),b为M(Q1, Q3),c为(x±s) | ||||
心功能障碍组与非心功能障碍组患者的性别、年龄、BMI、糖尿病、高血压、收缩压、舒张压、MAP、心率、WBC、PCT、CRP、CK、E峰、A峰、气管插管率、AKI发生率、CRRT率、住ICU时间及住院时间差异无统计学意义(P > 0.05);两组间患者的Lac、IL-6、CK-MB、BNP、NT-proBNP、E/e’、APACHEⅡ、SOFA、ICU病死率、住院病死率及新发房颤发生率差异有统计学意义(P < 0.05),见表 2。
| 变量 | 心功能障碍组(n=74) | 非心功能障碍组(n=199) | χ2/Z/t | P值 |
| 性别(男)a | 32(43.2) | 87(43.7) | 0.005 | 0.944 |
| 年龄(岁)b | 64(60, 67) | 65(61, 67) | 1.039 | 0.299 |
| BMI(kg/m2)c | 22.49±2.36 | 22.43±2.54 | 0.164 | 0.870 |
| 糖尿病a | 38(51.4) | 91(45.7) | 0.684 | 0.408 |
| 高血压a | 40(54.1) | 90(45.2) | 1.685 | 0.194 |
| 收缩压(mmHg)c | 92.42±17.50 | 90.11±22.15 | 0.807 | 0.420 |
| 舒张压(mmHg)c | 66.22±7.64 | 65.80±9.26 | 0.346 | 0.730 |
| MAP(mmHg)c | 85.53±13.53 | 87.86±12.54 | 1.340 | 0.182 |
| 心率(次/min)c | 107.89±20.87 | 105.51±18.98 | 0.898 | 0.370 |
| WBC(×109 L)c | 16.13±5.26 | 16.09±5.44 | 0.052 | 0.959 |
| PCT(ng/mL)b | 11.26(9.41, 12.39) | 10.84(9.44, 11.94) | 1.107 | 0.268 |
| CRP(mg/L)c | 254.85±34.40 | 253.03±32.03 | 0.410 | 0.682 |
| Lac(mmol/L)c | 5.05±0.65 | 4.55±0.61 | 5.905 | < 0.001 |
| IL-6(pg/mL)c | 181.61±19.89 | 168.94±20.40 | 4.595 | < 0.001 |
| CK(U/L)b | 231.43(212.51, 261.87) | 225.15(206.49, 264.92) | 0.701 | 0.483 |
| CK-MB(U/L)c | 30.00±6.21 | 26.34±6.63 | 4.123 | < 0.001 |
| BNP(ng/ml)c | 0.65±0.09 | 0.62±0.09 | 2.698 | 0.007 |
| NT-proBNP(ng/mL)b | 0.77(0.57, 1.17) | 0.61, (0.34, 0.87) | 3.806 | < 0.001 |
| E峰(m/s)c | 0.82±0.22 | 0.81±0.22 | 0.249 | 0.803 |
| A峰(m/s)b | 0.59(0.44, 0.85) | 0.62(0.47, 0.80) | 0.025 | 0.980 |
| E/e’ c | 12.52±1.79 | 11.31±1.97 | 4.615 | < 0.001 |
| APACHEⅡ(分)b | 20(16, 23) | 19(14, 22) | 1.974 | 0.048 |
| SOFA(分)b | 13(10.75, 15) | 12(10, 14) | 2.102 | 0.036 |
| ICU病死率(%)a | 35(47.3) | 34(17.1) | 26.069 | < 0.001 |
| 住院病死率(%)a | 36(48.6) | 39(19.6) | 22.847 | < 0.001 |
| 气管插管率(%)a | 52(70.3) | 142(71.4) | 0.031 | 0.860 |
| AKI发生率(%)a | 30(40.5) | 60(30.2) | 2.635 | 0.105 |
| 新发房颤发生率(%)d | 15(20.3) | 20(10.1) | 5.041 | 0.040 |
| CRRT率(%)d | 25(33.8) | 53(26.6) | 1.351 | 0.291 |
| 住ICU时间(d)b | 9(5, 12) | 8(5, 12) | 0.560 | 0.576 |
| 住院时间(d)c | 18.57±6.14 | 18.02±6.56 | 0.623 | 0.534 |
| 注:a为(频数,百分比),b为M(Q1, Q3),c为(x±s),d为Fisher精确概率法 | ||||
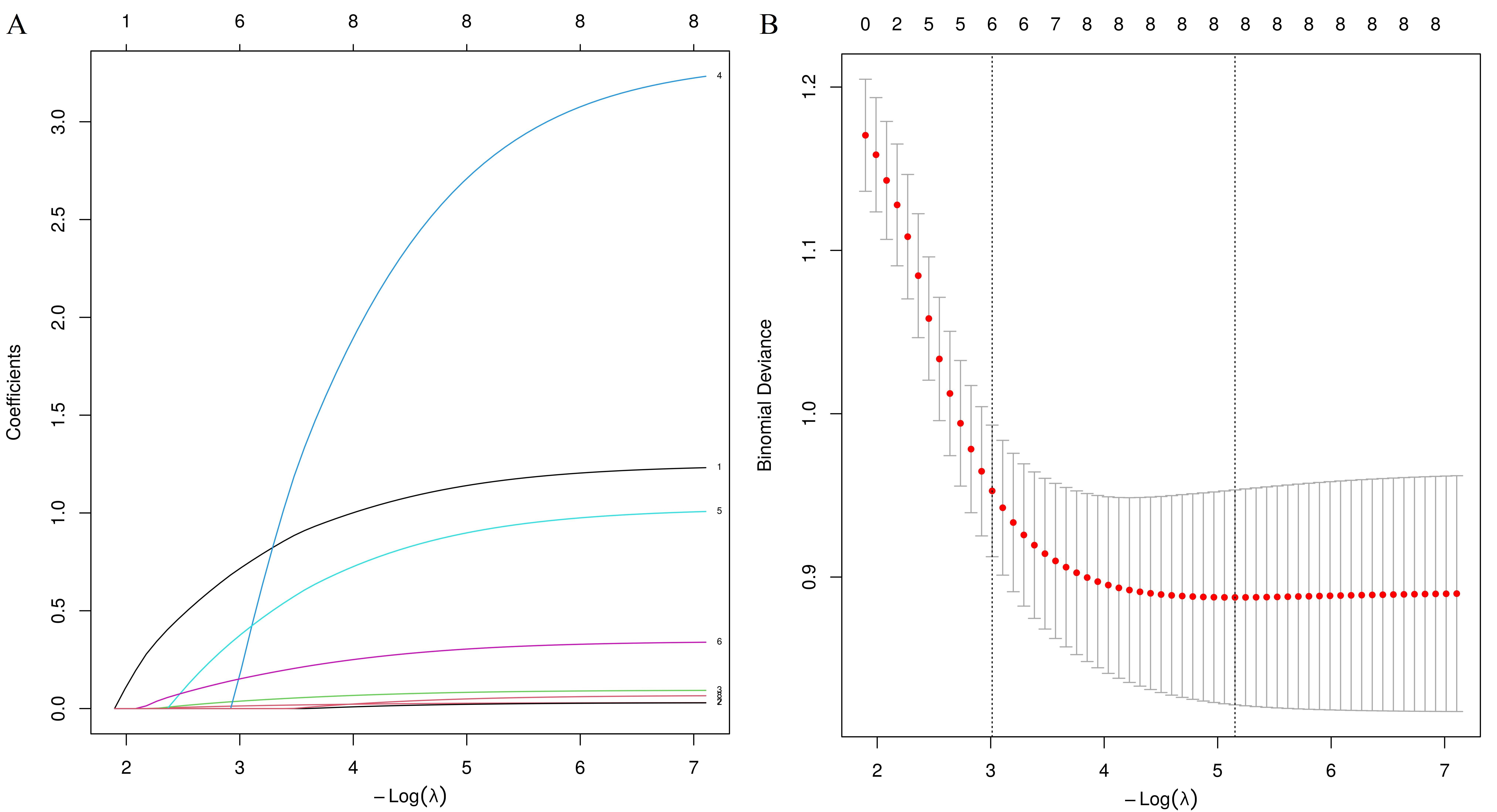
将表 2筛选出的变量纳入LASSO回归分析,结果显示,最优λ值为0.006,筛选出Lac、IL-6、CK-MB、BNP、NTproBNP、E/e’、APACHEⅡ及SOFA为特征变量,见图 2。
|
| 注:A:LASSO回归系数路径图,B:LASSO回归交叉验证曲线图 图 2 LASSO回归分析结果 Fig 2 LASSO regression analysis results |
|
|
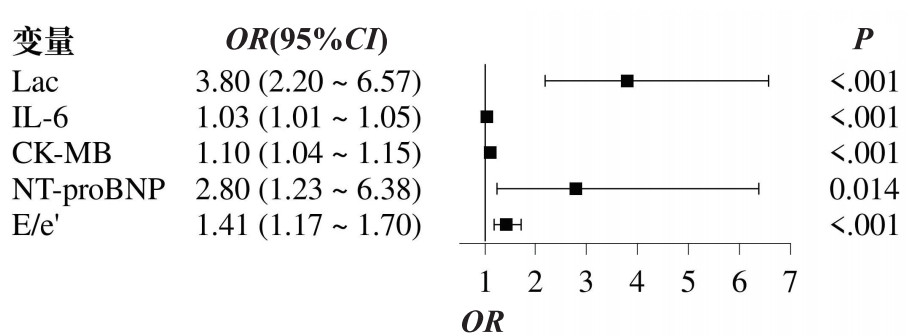
以患者是否发生心功能障碍(是=1,否=0)为因变量,以表 2中差异有统计学意义(P < 0.05)的变量(Lac、IL-6、CK-MB、BNP、NT-proBNP、E/e’、APACHEⅡ及SOFA)为自变量,纳入多因素Logistic回归分析,方法条件向前,结果显示,Lac、IL-6、CK-MB、NT-proBNP及E/e’是独立影响因素(P < 0.05),见表 3。森林图结果显示,Lac、IL-6、CK-MB、NT-proBNP及E/e’是发生心功能障碍的危险因素(P < 0.05,OR > 1),见图 3。基于上述因素建立预测模型为Logit(P) =-20.190+1.134×Lac+0.030×IL-6+0.092×CK-MB+1.030×NT-proBNP+0.346×E/e’。
| 变量 | β | 瓦尔德 | P值 | OR | 95%CI |
| Lac | 1.334 | 22.762 | < 0.001 | 3.798 | 2.195~6.570 |
| IL-6 | 0.030 | 13.172 | < 0.001 | 1.031 | 1.014~1.048 |
| CK-MB | 0.092 | 12.437 | < 0.001 | 1.097 | 1.042~1.155 |
| NT-proBNP | 1.030 | 6.022 | 0.014 | 2.802 | 1.230~6.379 |
| E/e’ | 0.346 | 13.358 | < 0.001 | 1.414 | 1.174~1.703 |
|
| 图 3 独立影响因素Logistic回归的森林图 Fig 3 Forest plot of Logistic regression of independent influencing factors |
|
|
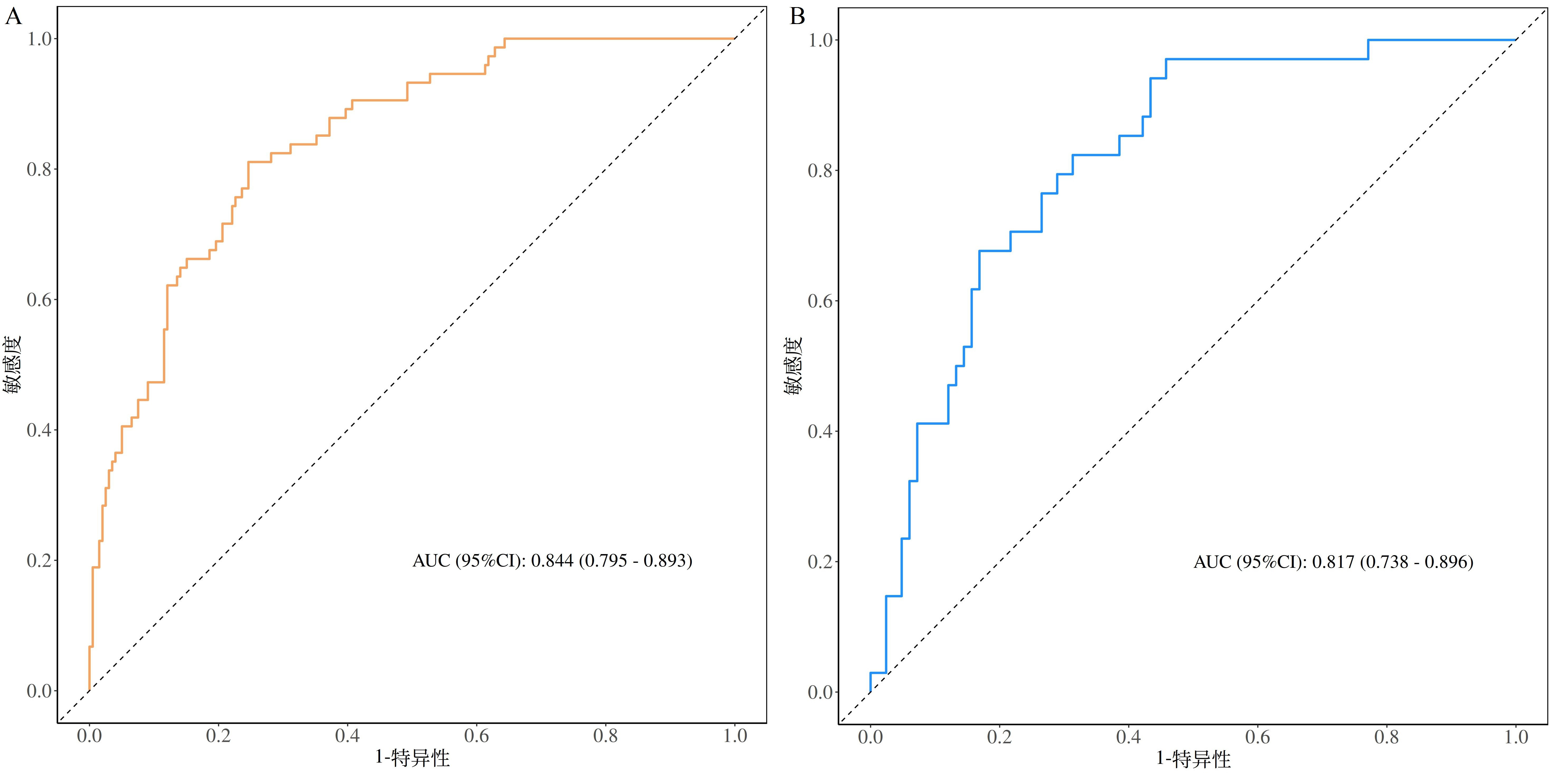
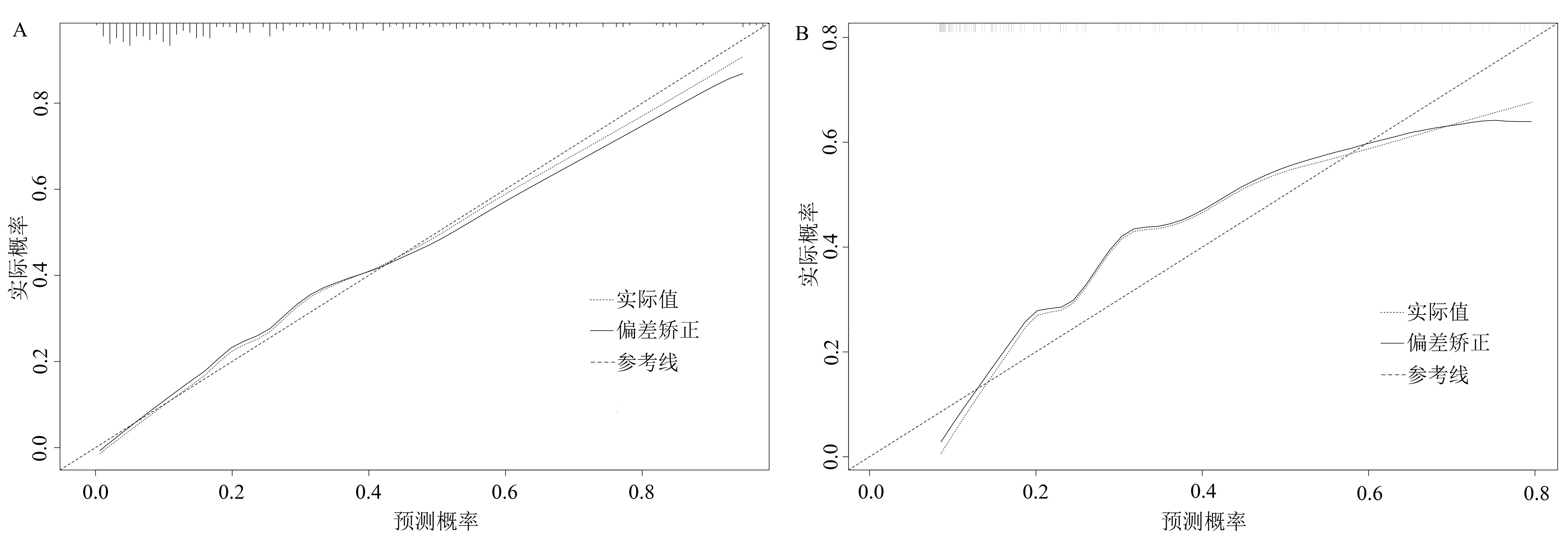
ROC曲线结果显示,该预测模型在模型组和验证组中的曲线下面积(area under the curve,AUC)分别为0.844及0.817,见图 4。Hosmer-Lemeshow检验结果显示,模型组和验证组的χ2和P值分别为9.660、0.290及5.988、0.649,差异均无统计学意义(P > 0.05),见图 5。
|
| 注:A:模型组,B:验证组 图 4 预测模型的ROC曲线图 Fig 4 ROC curve of the prediction model |
|
|
|
| 注:A:模型组,B:验证组 图 5 预测模型的校准曲线 Fig 5 Calibration curve of the prediction model |
|
|
脓毒症发生时,患者机体内部会引发一系列复杂且相互关联的病理生理过程,包括免疫细胞的过度激活、炎症介质的级联反应、细胞程序性死亡及线粒体功能的显著紊乱等,最终诱发心功能障碍[9-10]。脓毒症休克患者合并心功能障碍类型包括左心室收缩功能障碍、左心室舒张功能障碍和右心室功能障碍。其中,左心室功能障碍较常见,但右心功能障碍是28 d病死率的独立危险因素[11-12]。Lac是细胞代谢和能量产生的重要生物标志物,Lac水平升高是脓毒症相关心功能障碍的高危因素[13-14]。IL-6水平过度升高可能导致炎症失控,引发心肌纤维化、心室重构及心功能下降,从而增加心血管不良事件的风险。发生脓毒症休克时,脂多糖等病原体相关分子模式与固有免疫细胞膜Toll样受体等模式识别受体结合,启动细胞内信号转导通路,引起TNF-α、IL-1β、IL-6等炎症介质大量合成与释放,最终导致心功能障碍[15]。Yu等[16]建立大鼠脓毒症休克合并心功能障碍模型,结果发现血浆和心脏组织中的IL-1β、IL-6及TNF-α水平明显升高。CK-MB及NT-proBNP是诊断心功能损伤的重要标准,E/e’是评估心脏舒张功能受损的有效指标[17-18]。Jeong等[19]发现,年龄、糖尿病史、NT-pro-BNP是脓毒症合并心功能障碍的独立影响因素。赵鹏等[20]研究表明,APACHEⅡ评分、24 h乳酸清除率、NT-ProBNP、MAP、心率均与脓毒症患者合并心功能障碍的预后密切相关。本研究结果显示,Lac、IL-6、CK-MB、NT-proBNP及E/e’是脓毒症休克合并心功能障碍的独立影响因素(P < 0.05),与心功能障碍的生理、病理学理论相符,同时与上述研究结果一致;与张照龙等[21]研究相比,本研究在年龄、心率、MAP方面差异不显著,可能是不同心功能障碍类型在生理、病理以及对年龄、心率、MAP等指标的影响上存在差异,而本研究未对其进行亚型分类;此外,不同地区、不同医院的脓毒症休克患者可能在基础疾病、治疗情况等方面存在差异,进而影响年龄、心率、MAP等指标与心功能障碍之间的关系。
联合多种指标建立预测模型并对各项指标进行赋值量化,有助于临床医生在患者入院初期就对其发生心功能障碍的风险进行评估,制定个性化的治疗方案,提高救治效率[22]。杨建中等[23]发现,年龄、NT-proBNP、心型脂肪酸结合蛋白、新发心律失常是脓毒症舒张性心功能障碍的独立影响因素,联合预测因子诊断脓毒症舒张性心功能障碍优于单项指标,构建联合诊断模型具有临床应用价值及意义。庄燕等[24]研究发现,SOFA评分、BNP及CK-MB是脓毒症合并心功能障碍的独立因素,预测模型的AUC为0.801。本研究结果显示,预测模型在模型组和验证组中的AUC分别为0.844及0.817,AUC均大于0.75,表明预测模型在模型组和验证组均具有良好的区分度。Hosmer-Lemeshow检验结果显示,模型组和验证组的P值> 0.05,表明该模型与实际结果一致性良好。在临床实践中,对于高风险患者,密切监测Lac、IL-6、CK-MB、NT-proBNP及E/e’,有助于早期识别和诊断心功能障碍,及时调整治疗方案,最终可能改善患者预后。
利益冲突 所有作者声明无利益冲突
作者贡献声明 蔡青云:论文撰写;蔡青云,杨留生,张崇阳:数据收集及整理、统计学分析;蔡青云,石文芳:研究设计、论文修改;石文芳:研究指导
| [1] | DeMerle KM, Angus DC, Baillie JK, et al. Sepsis subclasses: a framework for development and interpretation[J]. Crit Care Med, 2021, 49(5): 748-759. DOI:10.1097/ccm.0000000000004842 |
| [2] | 王静霞, 张涛, 胡春琼, 等. 亚胺培南西司他丁钠联合小剂量氢化可的松治疗脓毒症休克患者的可行性[J]. 中华医院感染学杂志, 2024, 34(18): 2727-2731. DOI:10.11816/cn.ni.2024-240029 |
| [3] | Hollenberg SM, Singer M. Pathophysiology of sepsis-induced cardiomyopathy[J]. Nat Rev Cardiol, 2021, 18(6): 424-434. DOI:10.1038/s41569-020-00492-2 |
| [4] | Yap JQ, Nikouee A, Lau JE, et al. Mitochondria at the heart of sepsis: mechanisms, metabolism, and sex differences[J]. Int J Mol Sci, 2025, 26(9): 4211. DOI:10.3390/ijms26094211 |
| [5] | Riley RD, Ensor J, Snell KIE, et al. Calculating the sample size required for developing a clinical prediction model[J]. BMJ, 2020, 368(8238): m441. DOI:10.1136/bmj.m441 |
| [6] | 刘韵涵, 姜明明, 李冬梅, 等. 基于可解释机器学习方法老年脑卒中患者吞咽障碍预测模型的构建与验证[J]. 中华老年心脑血管病杂志, 2025, 27(6): 698-704. DOI:10.3969/j.issn.1009-0126.2025.06.003 |
| [7] | 谭睿, 杨鹏磊, 王晶, 等. 载脂蛋白A-I联合血清淀粉样蛋白A判断脓毒症及脓毒症休克患者的病情及预后价值[J]. 中华急诊医学杂志, 2024, 33(5): 643-650. DOI:10.3760/cma.j.issn.1671-0282.2024.05.009 |
| [8] | 李佳卓, 梁群, 姜芊竹, 等. 脓毒症心功能障碍患者中西医结合预后临床预测模型构建及验证[J]. 中华中医药学刊, 2024, 42(12): 57-61. DOI:10.13193/j.issn.1673-7717.2024.12.012 |
| [9] | 李亚南, 谢永鹏, 颜瑶, 等. 无创心肌做功评估脓毒症心肌病左室收缩功能[J]. 中华急诊医学杂志, 2025, 34(12): 1735-1743. DOI:10.3760/cma.j.cn114656-20250623-00468 |
| [10] | Velissaris D. Sepsis-induced myocardial dysfunction: a review of pathophysiology, diagnosis, and treatment[J]. Curr Infect Dis Rep, 2021, 23(6): 1-9. DOI:10.1007/s11886-020-01277-24 |
| [11] | Kim JS, Kim M, Kim YJ, et al. Troponin testing for assessing sepsis-induced myocardial dysfunction in patients with septic shock[J]. J Clin Med, 2019, 8(2): 239. DOI:10.3390/jcm8020239 |
| [12] | Kim JS, Kim YJ, Kim M, et al. Association between right ventricle dysfunction and poor outcome in patients with septic shock[J]. Heart, 2020, 106(21): 1665-1671. DOI:10.1136/heartjnl-2020-316889 |
| [13] | 李诗瑶, 王海, 杨妮, 等. 乳酸化在脓毒症器官损伤中的研究进展[J]. 中华急诊医学杂志, 2025, 34(12): 1782-1785. DOI:10.3760/cma.j.cn114656-20250515-00374 |
| [14] | 郝翠平, 胡庆河, 朱丽娜, 等. 血乳酸和降钙素原与病情严重程度评分对脓毒性休克患者短期预后的联合预测价值[J]. 中华危重病急救医学, 2021, 33(3): 281-285. DOI:10.3760/cma.j.cn121430-20201113-00715 |
| [15] | 李玉玲, 康健, 冯卓. 脓毒症心功能障碍的研究进展[J]. 中华危重症医学杂志(电子版), 2017, 10(3): 200-206. DOI:10.3877/cma.j.issn.1674-6880.2017.03.013 |
| [16] | Yu Y, Hu LL, Liu L, et al. Hsp22 ameliorates lipopolysaccharide-induced myocardial injury by inhibiting inflammation, oxidative stress, and apoptosis[J]. Bioengineered, 2021, 12(2): 12544-12554. DOI:10.1080/21655979.2021.2010315 |
| [17] | 许小泽, 林正豪, 刘雪燕. 危重型COVID-19患者血清cTnI、CK-MB、NT-proBNP与心功能的相关分析[J]. 暨南大学学报(自然科学与医学版), 2020, 41(6): 520-526. DOI:10.11778/j.jdxb.2020.06.007 |
| [18] | 林友国. E/e比值在慢性心力衰竭诊疗中的临床应用价值[J]. 中国中西医结合影像学杂志, 2017, 15(5): 562-563. DOI:10.3969/j.issn.1672-0512.2017.05.015 |
| [19] | Jeong HS, Lee TH, Bang CH, et al. Risk factors and outcomes of sepsis-induced myocardial dysfunction and stress-induced cardiomyopathy in sepsis or septic shock: a comparative retrospective study[J]. Medicine, 2018, 97(13): e0263. DOI:10.1097/md.0000000000010263 |
| [20] | 赵鹏, 寿松涛, 李晨, 等. 脓毒症患者合并心肌损伤的危险因素及其生存分析[J]. 中华医院感染学杂志, 2022, 32(7): 961-965. DOI:10.11816/cn.ni.2022-210792 |
| [21] | 张照龙, 王金忠, 王小智, 等. 脓毒症患者不同心功能障碍类型的临床特点及预后[J]. 中国老年学杂志, 2024, 44(6): 1281-1284. DOI:10.3969/j.issn.1005-9202.2024.06.001 |
| [22] | 陈发超, 徐银川, 张召才. 新型生化标志物在脓毒症心肌损伤中的诊断价值研究进展[J]. 中国全科医学, 2021, 24(5) 533-538, 545. DOI:10.12114/j.issn.1007-9572.2020.00.566 |
| [23] | 杨建中, 李转运, 殷富康, 等. 以心肌标志物为基础的脓毒症舒张性心功能障碍联合诊断模型的构建[J]. 中国全科医学, 2018, 21(20): 2426-2431. |
| [24] | 庄燕, 张海东, 戴林峰, 等. 脓毒症心肌功能障碍危险因素及临床预测模型的构建[J]. 中国中西医结合急救杂志, 2022, 29(3): 262-267. DOI:10.3969/j.issn.1008-9691.2022.03.002 |
 2026, Vol. 35
2026, Vol. 35