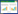脓毒症是机体对感染反应失调导致的危及生命的器官功能障碍,据统计,全世界估计每年4890万脓毒症和1100万脓毒症导致的死亡病例[1],高发病率和病死率是当前重大的医学科学问题和社会民生问题[2]。随着全球人口老龄化加剧,老年脓毒症疾病负担日益沉重,病死率随年龄增长显著上升,已成为全球公共卫生领域的重要挑战[3-5]。老年脓毒症患者常伴多种基础疾病、免疫功能低下且生理储备功能减退,临床表现常不典型,治疗反应差,预后不佳 [6-7],因此,早期快速识别高危患者并进行动态、精准的风险分层,对于指导临床决策、改善患者预后具有重要意义。
目前,研究多集中于短期预后评估[8-10],序贯器官衰竭评估(sequential organ failure assessment,SOFA)评分、快速序贯器官衰竭评分(quick sequential organ failure assessment,qSOFA)广泛应用于预测住院期间或28 d病死率[11-12],这些评分系统在急诊和重症监护室快速分诊和评估病情严重程度方面发挥了重要作用。然而,这些传统评分系统主要反映短期器官功能状态,对老年患者中长期(如90 d、180 d及1年)死亡风险的动态预测能力有限。老年脓毒症患者即使存活出院,仍面临因免疫功能障碍、基础疾病负担及并发症等导致的长期死亡风险升高[13-14],现有预后评估体系在中长期动态风险预测方面的不足,限制了临床医生对患者进行全面预后评估及制定个体化长期管理策略的能力。为弥补这一不足,实现从短期到中长期死亡风险的精准、动态评估,本研究基于多因素Cox回归分析,构建一个整合临床指标与治疗因素的对因素Cox回归模型。该模型旨在动态评估老年脓毒症患者在不同时间节点(包括院内、28 d、90 d、180 d及1年)的死亡风险,为早期识别高危患者、实施分层干预和优化医疗资源配置提供量化依据,从而为改善老年脓毒症患者的近期及远期预后提供新的工具和思路。
1 资料与方法 1.1 研究对象本研究为单中心、回顾性队列研究,连续纳入2021年1月1日至2024年11月30日宁波市医疗中心李惠利医院收治的符合标准的老年脓毒症患者。脓毒症诊断标准:采用国际通用的脓毒症3.0诊断标准(Sepsis 3.0)[15],即存在明确或可疑感染,且SOFA评分较基线升高≥2分。纳入标准:(1)年龄≥65周岁;(2)首次诊断脓毒症并符合上述Sepsis 3.0诊断标准;(3)急诊或入院24 h内完成基线指标采集。排除标准:(1)年龄 < 65周岁;(2)住院时间<24 h;(3)近1年有因脓毒症住院史;(4)数据不足如缺乏诊断脓毒症的记录;(5)合并晚期恶性肿瘤、终末期肾病、肝硬化Child-Pugh C级、严重痴呆或临终关怀状态;(6)妊娠期妇女。本研究方案经宁波市医疗中心李惠利医院伦理委员会批准(KY2025SL316-01),豁免患者知情同意。
1.2 研究方法 1.2.1 临床资料收集① 一般资料:年龄、性别、感染部位(呼吸系统、腹腔感染、胆道感染、泌尿道感染、血流感染、其他)、基础疾病(高血压、2型糖尿病、脑卒中、肿瘤);②入院后生命体征:体温、脉搏、呼吸、平均动脉压(mean arterial pressure, MAP);③入院24 h内实验室检查指标:血常规(白细胞、中性粒细胞计数、淋巴细胞计数、红细胞、血红蛋白、血细胞比容、血小板)、肝功能(总蛋白、白蛋白、前白蛋白、总胆红素、乳酸脱氢酶)、肾功能(尿素氮、肌酐、尿酸)、脂代谢(总胆固醇、甘油三酯、低密度脂蛋白)、电解质(总钙、钠、钾)、空腹葡萄糖、糖化血红蛋白、血浆纤维蛋白原、D二聚体、APTT、TT、CRP、HBP、IL-6、Lac、病原感染类型等;④入院24 h SOFA评分、入院时qSOFA评分。
1.2.2 治疗干预信息CRRT、呼吸机治疗、ICU入住情况。
1.2.3 结局指标① 主要终点:全因病死率,记录时间点为:院内、入院后28 d、90 d、180 d、1年。生存时间定义为从入院日期到死亡日期或末次随访日期。②次要终点:ICU入住率、ICU住院时间、总住院时间、总住院费用。
1.2.4 预测模型构建与验证① 预测因子筛选:将收集的潜在预测变量(包括基线资料、临床指标、治疗干预)纳入单因素Cox比例风险回归分析,筛选P < 0.05的变量。进一步采用多因素Cox比例风险回归模型(向后逐步回归法,剔除标准P > 0.05),最终确定独立预测因子,并计算风险比(hazard ratio, HR)及其95%置信区间(CI)。②多因素联合预测模型构建:基于多因素Cox回归分析确定的独立预测因子及其回归系数(β值),构建用于预测老年脓毒症患者不同时间点(院内、28 d、90 d、180 d、1年)死亡风险的多因素联合预测模型。该模型通过Cox回归方程体现各预测因子对风险的贡献。③模型性能评价:区分度(discrimination):采用ROC曲线计算各时间节点(院内、28 d、90 d、180 d、1年)曲线下面积(AUC)。比较联合模型与单一最佳预测因子(ICU治疗)的AUC,采用DeLong检验评估差异。
校准度(calibration):绘制各时间节点的校准曲线(calibration curve),通过Bootstrap法(1000次重复抽样)进行内部验证,评估模型预测概率与实际观察概率的一致性。采用Brier评分量化预测误差(0为完美,1为最差)。
临床实用性(clinical utility):绘制DCA曲线,评估在不同阈值概率(threshold probability)下,应用该预测模型相较于“全部干预”或“全不干预”策略的临床净获益(net benefit)。
1.3 统计学方法使用R软件(版本4.4.3)完成。双侧P < 0.05视为差异具有统计学意义。符合正态分布的计量资料以均数±标准差(x±s)表示,组间比较采用独立样本“t”检验。非正态分布的计量资料以M(P25~P75)表示,组间比较采用Mann-Whitney U检验。计数资料以频数和百分比[n (%)]表示,组间比较采用χ2检验或Fisher精确检验。生存分析:采用Kaplan-Meier法绘制生存曲线,Log-rank检验比较组间差异。模型相关分析:(Cox回归、时间依赖ROC、校准曲线、DCA),使用R包:survival (Cox模型),timeROC (时间依赖ROC),rms (列线图、校准曲线),dcurves (DCA)。以P < 0.05差异有统计学意义。
2 结果 2.1 基线资料与临床特征搜集老年脓毒症患者共纳入1 471例患者,其中男性患者占比62.61%(病死率26.71%),女性患者占比37.39%(病死率21.10%),男性病死率高于女性,差异有统计学意义(P =0.019)。高血压患者占比43.78%(病死率26.71%)、糖尿病占比24.81%(病死率26.85%)、脑卒中患者占比16.93%(病死率24.10%)、恶性肿瘤患者占比6.66%(病死率39.80%),主要临床结局:入住ICU 644例(43.78%),其中院内存活1 109例(75.4%),28 d存活1 101(74.8%),90 d存活949例(64.5%),180 d存活896例(60.9%),1年存活818例(55.6%),见表 1。
| 指标 | 总体结果(n=1471) | 存活组(n=1109) | 死亡组(n=362) | P值 |
| 一般人口学特征 | ||||
| 性别(男/女)(n, %) | 921(62.61)/550(37.39) | 675(60.87)/434(39.13) | 246(67.96)/116(32.04) | 0.019 |
| 年龄(岁),M(P25~P75) | 78(72~84) | 77(72~83) | 80(74~86) | < 0.001 |
| 感染相关特征 | ||||
| 感染部位(n, %) | - | - | - | < 0.001 |
| - 呼吸系统感染 | 786(53.43) | 621(55.99) | 165(45.58) | - |
| - 腹腔感染 | 243(16.52) | 178(16.05) | 65(17.96) | - |
| - 泌尿道感染 | 189(12.85) | 156(14.07) | 33(9.12) | - |
| - 血流感染 | 127(8.63) | 72(6.49) | 55(15.19) | - |
| - 胆道感染 | 68(4.62) | 53(4.78) | 15(4.14) | - |
| - 其他感染(皮肤软组织/颅内等) | 58(3.94) | 29(2.61) | 29(8.01) | - |
| 基础疾病(n, %) | ||||
| 高血压 | 644(43.78) | 472(42.53) | 212(58.56) | < 0.001 |
| 2型糖尿病 | 365(24.81) | 267(24.08) | 98(27.07) | 0.252 |
| 脑卒中 | 249(16.93) | 189(17.04) | 60(16.57) | 0.834 |
| 恶性肿瘤 | 98(6.66) | 59(5.32) | 39(10.77) | < 0.001 |
| 入院24 h生命体征 | ||||
| 体温(℃, x±s) | 38.2±1.5 | 38.1±1.4 | 38.5±1.6 | < 0.001 |
| 脉搏(次/min, x±s) | 98.6±18.3 | 97.2±17.8 | 102.5±18.9 | < 0.001 |
| 呼吸(次/min, x±s) | 22.5±5.7 | 21.8±5.3 | 24.6±6.2 | < 0.001 |
| 平均动脉压(mmHg, x±s) | 78.3±12.6 | 80.5±11.9 | 72.1±12.8 | < 0.001 |
| 入院24 h实验室指标 | ||||
| 白细胞计数(×109/L),M(P25~P75) | 12.8(8.5~18.6) | 12.1(8.2~17.3) | 15.6(9.8~22.5) | < 0.001 |
| 中性粒细胞比例(%, x±s) | 82.5±10.3 | 81.2±10.1 | 86.3±9.8 | < 0.001 |
| 单核细胞计数(×109/L, x±s) | 0.31 ± 0.31 | 0.30 ± 0.31 | 0.34 ± 0.31 | 0.020 |
| 淋巴细胞计数[×109/L, M(P25~P75)] | 0.9(0.6~1.3) | 1.0(0.7~1.4) | 0.7(0.5~1.0) | < 0.001 |
| 血红蛋白(g/L, x±s) | 115.8±20.3 | 118.2±19.7 | 108.5±20.5 | < 0.001 |
| 血小板计数[×109/L, M(P25~P75)] | 186(125~268) | 198(132~281) | 145(98~212) | < 0.001 |
| 白蛋白(g/L, x±s) | 30.2±5.7 | 31.5±5.3 | 26.8±5.4 | < 0.001 |
| 血尿素氮[mmol/L, M(P25~P75)] | 9.8(6.5~14.2) | 8.6(6.2~12.5) | 13.5(8.8~18.6) | < 0.001 |
| 肌酐[μmol/L, M(P25~P75)] | 112(85~168) | 105(82~152) | 138(95~215) | < 0.001 |
| 乳酸(mmol/L, x±s) | 2.3±1.4 | 2.0±1.1 | 3.2±1.7 | < 0.001 |
| C反应蛋白[mg/L, M(P25~P75)] | 86(45~135) | 80(42~128) | 105(58~156) | < 0.001 |
| 白细胞介素- 6 [pg/mL, M(P25~P75)] | 128(65~243) | 105(60~208) | 215(125~326) | < 0.01 |
| 器官功能评分 | ||||
| 入院24 h SOFA评分,[M(P25~P75)] | 6(4~8) | 5(3~7) | 9(7~12) | < 0.001 |
| 入院时qSOFA评分,[M(P25~P75)] | 2(1~3) | 1(1~2) | 3(2~3) | < 0.001 |
| 临床结局 | ||||
| 院内死亡 | 1109(75.4) | 362(24.6) | - | |
| 28 d死亡 | 1101(74.8) | 370(25.2) | ||
| 90 d死亡 | 949(64.5) | 522(35.5) | ||
| 180 d死亡 | 896(60.9) | 575(39.1) | ||
| 1年死亡 | 818(55.6) | 653(44.4) | ||
| ICU入住率 | 644(43.78) | 428(38.59) | 216(59.67) | < 0.001 |
| ICU住院时间[d, M(P25~P75)] | 7(4~12) | 8(5~13) | 5(3~8) | < 0.001 |
| 总住院时间[d, M(P25~P75)] | 14(9~22) | 16(10~24) | 8(5~15) | < 0.001 |
| 总住院费用[万元, M(P25~P75)] | 8.6(5.2~13.8) | 9.2(5.8~14.5) | 6.5(4.1~10.2) | < 0.001 |
首先,将所有收集的潜在预测变量(包括基线人口学资料、临床指标及治疗干预措施)纳入单因素Cox比例风险回归分析。设定筛选标准为P < 0.05,共筛选出21个与老年脓毒症患者死亡风险显著相关的变量进入后续多因素分析(表 2)。进一步采用多因素Cox比例风险回归模型,运用向后逐步回归法(剔除标准设定为P > 0.05)对上述变量进行筛选。最终确定qSOFA评分、淋巴细胞计数、呼吸机治疗、CRRT及ICU治疗5个变量为老年脓毒症患者死亡的独立预测因子(表 3)。基于多因素Cox回归分析确定的独立预测因子及其回归系数(β值),构建用于预测老年脓毒症患者不同时间点(院内、28 d、90 d、180 d、1年)死亡风险的多因素联合预测模型,Cox比例风险模型的方程:h(t, X)=h0(t)×exp(1.43·ICU+1.17×mechanical ventilation+0.60×qSOFA+0.72×CRRT-0.45×Lymphocyte Count),(变量解释与赋值:ICU:是否入住ICU(是=1,否=0);mechanical ventilation:是否接受呼吸机治疗(是=1,否=0);qSOFA:qSOFA评分(连续整数,如0, 1, 2, 3);CRRT:是否接受CRRT治疗(是=1,否=0);Lymphocyte Count:淋巴细胞计数(单位:×109/L,连续数值))。
| 变量 | β系数 | SE | χ2 | P值 | OR(95%CI) |
| 年龄(岁) | 0.409 | 0.101 | 16.564 | 0.000 | 1.505(1.236~1.833) |
| 血氧饱和度(%) | -0.026 | 0.005 | 23.858 | 0.000 | 0.974(0.964~0.984) |
| 意识水平 | 0.758 | 0.1 | 57.471 | 0.000 | 2.133(1.754~2.595) |
| qSOFA | 0.742 | 0.195 | 14.5 | 0.000 | 2.100(1.434~3.077) |
| SOFA | 0.097 | 0.017 | 31.542 | 0.000 | 1.102(1.065~1.140) |
| 呼吸机治疗 | 0.961 | 0.08 | 142.941 | 0.000 | 2.614(2.233~3.06) |
| CRRT | 0.85 | 0.086 | 96.787 | 0.000 | 2.34(1.975~2.771) |
| 病因 | 0.318 | 0.078 | 16.484 | 0.000 | 1.375(1.179~1.603) |
| ICU入住率 | 1.265 | 0.082 | 235.436 | 0.000 | 3.543(3.015~4.165) |
| ICU住院天数(d) | 0.002 | 0.001 | 6.078 | 0.014 | 1.002(1~1.004) |
| 高血压 | 0.362 | 0.078 | 21.229 | 0.000 | 1.436(1.231~1.674) |
| 白细胞介素-6(pg/mL) | 0.377 | 0.134 | 7.923 | 0.005 | 1.458(1.121~1.895) |
| 淋巴细胞计数(×109/L) | 1.088 | 0.342 | 10.102 | 0.001 | 2.969(1.518~5.809) |
| 单核细胞计数(×109/L) | 0.084 | 0.036 | 5.379 | 0.020 | 1.088(1.013~1.168) |
| 乳酸(mmol/L) | 0.085 | 0.014 | 35.303 | 0.000 | 1.089(1.059~1.120) |
| 空腹血糖(mmol/L) | 0.034 | 0.006 | 31.845 | 0.000 | 1.035(1.023~1.047) |
| 前白蛋白(g/L) | -0.003 | 0.001 | 15.418 | 0.000 | 0.997(0.996~0.999) |
| 血尿素氮(mmol/L) | 0.444 | 0.086 | 26.587 | 0.000 | 1.559(1.317~1.845) |
| 活化部分凝血活酶时间(s) | 0.014 | 0.003 | 19.445 | 0.000 | 1.014(1.008~1.020) |
| 纤维蛋白原(g/L) | -0.137 | 0.024 | 33.75 | 0.000 | 0.872(0.833~0.913) |
| TyG | 0.185 | 0.057 | 10.421 | 0.001 | 1.203(1.075~1.346) |
| 注:qSOFA[快速序贯器官衰竭评分(quick sequential organ failure assessment)];SOFA[序贯器官衰竭评分(sequential organ failure assessment)];CRRT[连续性肾脏替代治疗(continuous renal replacement therapy)];ICU[重症监护病房(intensive care unit)];TyG[甘油三酯-葡萄糖指数(tyceride-glucose index)] | |||||
| 变量 | β系数 | SE | χ2 | HR (95% CI) | P值 |
| ICU | 1.43 | 0.12 | 142.08 | 4.18 (3.32~5.26) | < 0.001 |
| 呼吸机治疗 | 1.17 | 0.11 | 113.36 | 3.21 (2.58~4.00) | < 0.001 |
| qSOFA | 0.60 | 0.08 | 56.25 | 1.82 (1.35~2.45) | < 0.001 |
| CRRT | 0.72 | 0.07 | 105.80 | 2.05 (1.60~2.63) | < 0.001 |
| 淋巴细胞计数(×109/L) | -0.45 | 0.06 | 56.25 | 0.64 (0.52~0.79) | < 0.001 |
| 注:ICU[重症监护病房(intensive care unit)];qSOFA[快速序贯器官衰竭评分(quick sequential organ failure assessment)];CRRT(连续性肾脏替代治疗[continuous renal replacement therapy)] | |||||
关键发现:1.入住ICU 是预测价值最强的独立危险因素(见表 3)。2.淋巴细胞计数(每增加1×109/L)是唯一的保护性因素(见表 3)。3.所有独立预测因子的95%置信区间均未包含1(即HR≠1),且P值均小于0.001,差异均具有统计学意义。
2.3 多因素联合模型与单因素指标预测性能比较多因素联合预测模型与单因素指标在不同时间点的ROC曲线(见图 1),如图 1A所示,本研究所构建的多因素联合预测模型(整合了qSOFA评分、淋巴细胞计数、呼吸机治疗、CRRT及ICU治疗5个指标)在院内、28 d、90 d、180 d及1年五个时间节点的AUC均显著高于单一最佳预测指标ICU治疗(所有时间点DeLong检验P < 0.01)。模型区分度随预测时间延长呈现缓慢衰减趋势(院内AUC: 0.826; 1年AUC: 0.717),表明该模型兼具优异的短期预测效能与稳定的中长期动态风险评估能力。图 1B进一步通过时间依赖性ROC曲线直观呈现了联合模型随时间的动态预测性能,其曲线均位于左上象限,再次验证了模型良好的区分度。
|
| 注:A:多因素联合预测模型与单因素指标在院内、28 d、90 d、180 d及1年时间点预测老年脓毒症患者死亡风险的ROC曲线进行比较。多因素模型在各时间点均显示出更高的AUC值(均P<0.01),表明其具有更优的区分能力。B:多因素联合预测模型在不同时间点(院内、28 d、90 d、180 d及1年)的时间依赖ROC曲线,直观展示了模型随着时间变化的动态预测性能。 图 1 多时间点单因素指标、多因素联合模型预测死亡风险ROC曲线 Fig 1 ROC curves of single-factor indicators and multivariate combined model for predicting mortality risk at multiple time points |
|
|
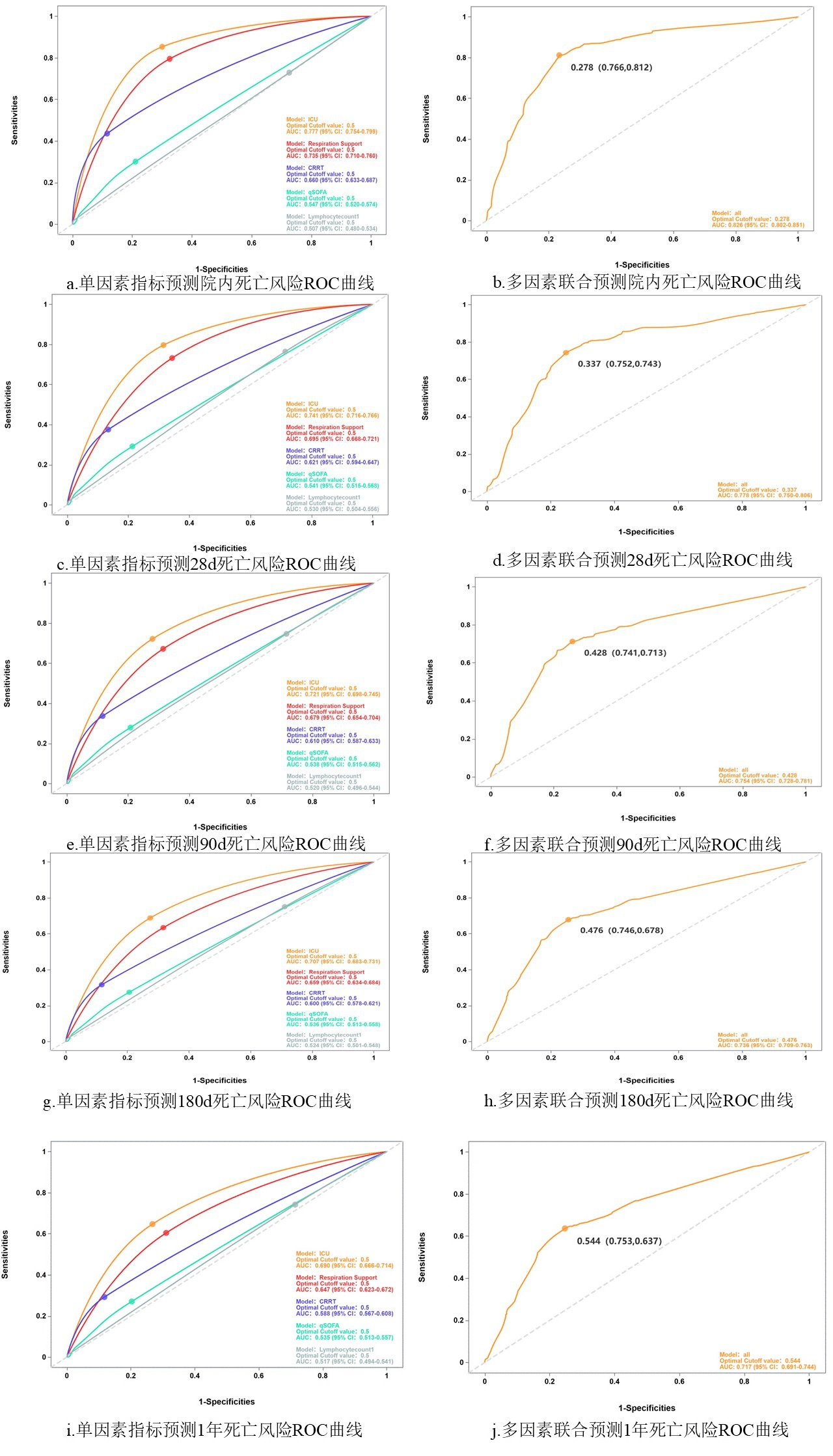
基于上述5个独立预测因子构建的多因素联合预测模型在各时间节点的预测效能如(表 4)所示。联合模型在所有时间节点AUC均显著高于最佳单一指标ICU治疗(P < 0.01),且随预测时间延长,AUC值呈现缓慢衰减趋势(从院内0.826降至1年0.717,降幅13.2%),表明模型适用于动态风险评估。三维曲面图形式展示了多因素联合预测模型在五个不同终点时间点的动态预测能力(见图 2)。图 2中可清晰观察到,对于每一个特定的预测时间点(如院内死亡),模型均能提供高AUC值,表明其精准的区分能力。更重要的是,整个曲面在从短期(院内)到中长期(1年)的时间维度上保持了相对平滑和高位态势,仅随预测时间延长呈现缓慢下降,这从视觉上强有力地证实了本模型并非仅适用于短期预后评估,而是一个能够可靠地用于追踪和预测老年脓毒症患者远期死亡风险的动态工具,满足了临床对持续风险监控的需求。
| 时间节点 | 联合模型AUC | 最佳单指标AUC(ICU治疗) | 特异度 | 敏感度 |
| 院内 | 0.826 | 0.777 | 0.767 | 0.812 |
| 28 d | 0.778 | 0.741 | 0.75 | 0.743 |
| 90 d | 0.754 | 0.721 | 0.741 | 0.713 |
| 180 d | 0.736 | 0.707 | 0.746 | 0.678 |
| 1年 | 0.717 | 0.690 | 0.753 | 0.637 |
|
| 图 2 多因素联合模型预测各时间节点死亡风险的时间依赖ROC曲线 Fig 2 Time-dependent ROC curves of the multivariate combined model for predicting mortality risk at each time point |
|
|
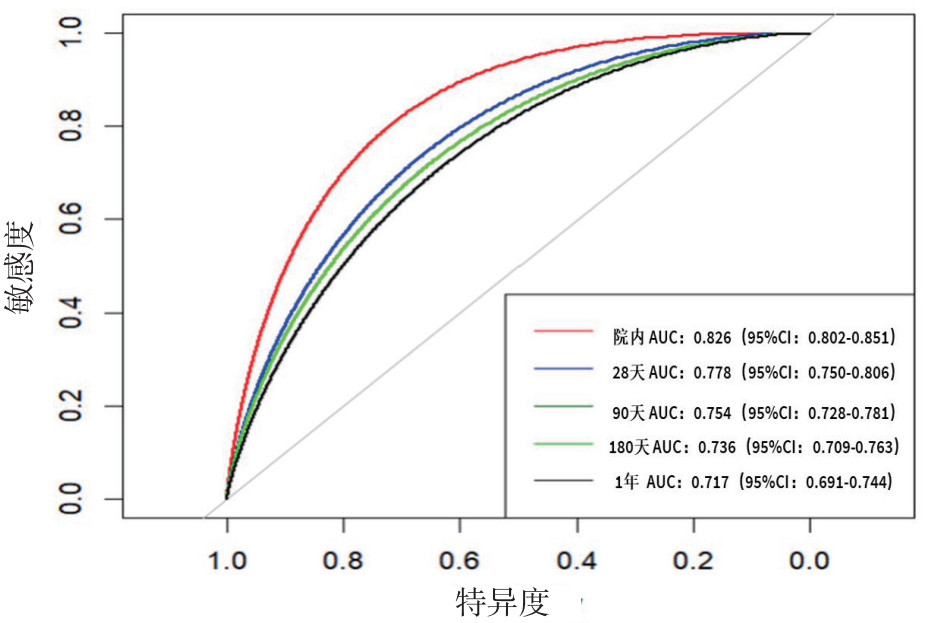
校准曲线显示模型在各时间点的预测概率与实际观察概率具有良好的一致性。DCA表明,在较宽的阈值概率范围内,应用该预测模型相比“全干预”或“全不干预”策略能带来更高的临床净获益(见图 3)。图 3综合评估了多因素联合预测模型的校准度与临床实用性。图 3A的校准曲线显示,在所有五个预测时间点上,模型预测的死亡风险概率(X轴)与实际观察到的死亡发生率(Y轴)高度一致,各时间点曲线均紧贴理想参考线(对角线)分布。这表明模型的预测结果准确可靠,具有优异的校准度,预测概率与实际风险偏差极小。图 3B的DCA结果表明,在广泛的阈值概率范围内(大致为5%~60%以上,因时间点而异),应用本预测模型进行临床决策(各条实线)所能获得的临床净获益均高于“对所有患者均干预”(虚线)和“对所有患者均不干预”(横轴)的两种极端策略。这证明了该模型具备良好的临床转化潜力,将其用于老年脓毒症患者的风险分层并指导干预措施(如对高危患者加强监护与治疗),能够为患者带来更优的临床结局,同时避免对低危患者的过度干预。
|
| 注:A:多因素联合预测模型在院内、28 d、90 d、180 d及1年时间点的校准曲线。图中对角线为理想参考线,各时间点曲线均紧贴参考线分布,提示模型预测死亡概率与实际观察概率具有良好的一致性,预测误差较小(各时间点Brier值分别为0.130、0.146、0.184、0.209、0.229)。B:各时间点的决策曲线分析(DCA)。曲线显示,在大多数阈值概率范围内,应用本模型(实线)相比“全部干预”(虚线)或“全不干预”(横轴)策略均能带来更高的临床净获益,表明该模型具有良好的临床实用性和干预指导价值 图 3 多因素联合预测模型在不同时间节点的校准曲线与决策曲线分析(DCA) Fig 3 Calibration curves and decision curve analysis (DCA) of the multivariate prediction model at different time points |
|
|
本研究成功构建并内部验证了一个整合qSOFA评分、淋巴细胞计数、呼吸机治疗、CRRT及ICU治疗五大关键因素的多因素联合预测模型,可用于预测老年脓毒症患者从院内至1年不同时间节点死亡风险的动态评估。结果显示,该模型在短期(院内、28 d)及中长期(90 d、180 d、1年)均展现出优异的区分度(AUC: 0.717~0.826)和良好的校准度,显著优于单一最佳预测指标(ICU入住),且具备明确的临床净获益。
ICU治疗作为最强死亡风险预测因子:本研究证实,需要入住ICU是老年脓毒症患者死亡的最强独立预测因素(HR=4.18, 95% CI: 3.32~5.26)。这与既往多项研究结果一致,深刻反映了需要ICU治疗的患者存在严重器官功能障碍或需要高级生命支持的危重状态,是疾病严重程度的终极体现[16-18]。这凸显了在急诊早期识别高危患者、积极阻止病情恶化的极端重要性。淋巴细胞计数的关键保护作用:本研究发现淋巴细胞计数(每增加1×109/L)是独立的保护性因素(HR=0.64, 95% CI: 0.52~0.79),可使死亡风险显著降低36%。这一发现具有重要的病理生理学意义。老年脓毒症患者常伴随与年龄相关的“免疫衰老”和脓毒症诱导的“免疫麻痹”,表现为淋巴细胞减少和功能受损[19]。低淋巴细胞计数是免疫抑制状态的重要标志,与继发感染风险增加、病原体清除能力下降及器官修复障碍密切相关[20-22]。本研究结果从大样本临床数据层面证实,基线淋巴细胞计数是评估老年脓毒症患者免疫状态和预后的强有力指标,为监测免疫调节治疗反应提供了潜在靶点。治疗强度指标(呼吸机治疗、CRRT)的预后价值:需要呼吸机治疗(HR=3.21)和CRRT(HR=2.05)同样被确定为重要的独立危险因素。这直接体现了呼吸衰竭和急性肾损伤(AKI)作为脓毒症常见且致命的并发症,对患者预后的决定性影响[23-25]。特别是呼吸机治疗的需求,其HR值仅次于ICU入住,强调了呼吸系统功能障碍在老年脓毒症患者不良结局中的核心地位。qSOFA评分的持续预测能力:qSOFA评分(每增加1分,HR=1.82)在本模型中保持了显著的预测价值。尽管其预测效能弱于ICU入住和呼吸机治疗,但其简便易行、床旁快速获取的优势使其在急诊分诊和早期风险分层中仍具有不可替代的作用[9, 26]。本研究结果支持qSOFA作为识别潜在危重老年脓毒症患者的有效工具。动态预测模型的独特优势:本模型的核心创新在于其动态预测能力,覆盖了从院内到1年的多个关键时间节点。传统的评分系统(如SOFA、APACHEⅡ)主要聚焦于短期(如ICU内或28 d)病死率,而老年脓毒症患者即使存活出院,仍面临显著升高的长期死亡风险[27-29]。本模型成功弥补了这一空白,其AUC值随预测时间延长仅呈现缓慢衰减(院内0.826→1年0.717),表明其整合的预测因子能够捕捉影响患者短期恢复和长期生存的共同及持续存在的病理生理学基础(如持续存在的免疫功能障碍、未完全恢复的器官功能储备、基础疾病负担等)。这为临床医生提供了贯穿患者诊疗全程的风险评估工具。
本研究建立的模型在预测因子的选择和模型构建方法上具有特色:多维度指标整合:与单纯依赖生理评分的模型(如SOFA、qSOFA)不同,本研究创新性地整合了反映器官功能障碍(qSOFA)、免疫状态(淋巴细胞计数)和治疗强度/资源需求(呼吸机治疗、CRRT、ICU治疗)三大维度的指标。这种整合更全面地刻画了疾病的严重程度、机体反应和医疗干预水平,是模型在中长期预测中保持较高效能的关键。专注于老年人群:本研究专门针对老年脓毒症高危群体构建模型,其预测因子(如淋巴细胞计数的重要性)更贴合老年患者的病理生理机制(如免疫衰老),其结果对指导老年脓毒症的精准诊疗更具针对性价值。动态预测能力:本研究明确评估并评价了模型在多个时间点的预测性能,提供了从短期到中长期的连续风险评估能力。
本模型可能具备临床转化潜力:急诊/早期风险分层与干预:在急诊或普通病房,利用该模型快速识别死亡高风险的老年脓毒症患者(例如,根据模型计算的预测风险值或探索的风险分层)。对这些患者应启动更积极的监测、早期目标导向治疗(EGDT)优化、及时请ICU会诊或转诊,并考虑探索免疫调节等个体化干预策略。资源优化配置:同时,模型有助于识别死亡低风险患者。对此类患者,在保证医疗安全的前提下,可避免不必要的ICU转诊和过度侵入性监测,合理分配ICU资源,降低医疗成本及操作相关风险。预后沟通与共享决策:量化的、动态的风险预测有助于医生与患者及其家属进行更客观、透明的预后沟通,为制定个体化的治疗目标(如积极抢救vs.姑息治疗)和出院后随访计划提供依据。研究终点选择与疗效评估:模型揭示的不同时间点风险变化提示,未来针对老年脓毒症的干预性研究应考虑将中长期生存率纳入主要或次要终点。
本研究存在以下局限性,需要在解读结果和应用模型时予以关注:单中心回顾性设计:数据来源于单一医疗中心,可能存在选择偏倚,且回顾性分析无法完全控制所有混杂因素。模型的普适性需在多中心、前瞻性队列中进行外部验证。竞争风险未考虑:在预测长期终点(如1年病死率)时,非脓毒症相关的死亡(如晚期肿瘤、严重心血管事件)可能构成竞争风险,本研究使用的Cox模型未专门处理此类情况。动态预测的实现方式:当前模型是基于基线(入院24 h内)指标预测未来风险。构建整合疾病进程中多时间点动态变化数据的模型,可能提供更精准的风险评估。
基于本研究的发现和局限性,未来研究可聚焦于:模型的外部验证与推广:在国内外不同地域、不同级别的医院进行大规模外部验证,评估模型的泛化能力。纳入新型生物标志物与组学数据:整合基因组学、转录组学、蛋白组学或更精细的免疫学指标(如单细胞测序),探索构建预测效能更优的整合模型。开发动态更新模型:收集患者住院期间关键指标(如SOFA评分、淋巴细胞计数、乳酸)的动态变化数据,构建可随病情演变更新风险预测的实时模型。构建在线计算器与临床决策支持系统:将列线图模型转化为便捷的在线计算工具或嵌入医院电子病历系统(EMR),便于临床医生实时使用。
总之,本研究成功构建并内部验证了一个整合qSOFA评分、淋巴细胞计数、呼吸机治疗、CRRT及ICU治疗五项指标的多因素联合预测模型。该模型能够有效动态评估老年脓毒症患者从院内至1年的死亡风险,具有较高的区分度(AUC 0.717~0.826)与良好的校准性能。ICU治疗是预测价值最强的危险因素,而淋巴细胞计数则为重要的保护性因素。该模型可为早期识别高危患者、优化临床干预与资源配置提供量化依据,具备良好的临床实用性。未来仍需通过多中心前瞻性研究进一步验证与优化。
利益冲突 所有作者声明无利益冲突
作者贡献声明 蒋坚、李增攀:数据整理分析,论文撰写;朱立军、赵益栋:临床资料和数据收集整理,制作图表;徐蕊、徐嘉明:预测模型构建与验证、统计分析、图表制作;杨诺南、刘雪兰:研究设计,论文撰写与修改
| [1] | Meyer NJ, Prescott HC. Sepsis and septic shock[J]. N Engl J Med, 2024, 391(22): 2133-2146. DOI:10.1056/nejmra2403213 |
| [2] | 刘峰宇, 李想, 孙同文. 中国脓毒症十年研究进展回顾及展望[J]. 中华急诊医学杂志, 2023, 32(10): 1291-1295. DOI:10.3760/cma.j.issn.1671-0282.2023.10.002 |
| [3] | Rudd KE, Johnson SC, Agesa KM, et al. Global, regional, and national sepsis incidence and mortality, 1990-2017:analysis for the Global Burden of Disease Study[J]. Lancet, 2020, 395(10219): 200-211. DOI:10.1016/s0140-6736(19)32989-7 |
| [4] | Xie JF, Wang HL, Kang Y, et al. The epidemiology of sepsis in Chinese ICUs: a national cross-sectional survey[J]. Crit Care Med, 2020, 48(3): e209-e218. DOI:10.1097/ccm.0000000000004155 |
| [5] | Fleischmann-Struzek C, Goldfarb DM, Schlattmann P, et al. The global burden of paediatric and neonatal sepsis: a systematic review[J]. Lancet Respir Med, 2018, 6(3): 223-230. DOI:10.1016/s2213-2600(18)30063-8 |
| [6] | Juneja D. Severe sepsis and septic shock in the elderly: an overview[J]. World J Crit Care Med, 2012, 1(1): 23. DOI:10.5492/wjccm.v1.i1.23 |
| [7] | Ferrante LE, Pisani MA, Murphy TE, et al. Functional trajectories among older persons before and after critical illness[J]. JAMA Intern Med, 2015, 175(4): 523. DOI:10.1001/jamainternmed.2014.7889 |
| [8] | Vincent JL, Moreno R, Takala J, et al. The SOFA (Sepsis-related Organ Failure Assessment) score to describe organ dysfunction/failure: On behalf of the Working Group on Sepsis-Related Problems of the European Society of Intensive Care Medicine (see contributors to the project in the appendix)[J]. Intensive Care Med, 1996, 22(7): 707-710. DOI:10.1007/bf01709751 |
| [9] | Seymour CW, Liu VX, Iwashyna TJ, et al. Assessment of clinical criteria for sepsis: for the third international consensus definitions for sepsis and septic shock (sepsis-3)[J]. Jama, 2016, 315(8): 762. DOI:10.1001/jama.2016.0288 |
| [10] | 李秋敬, 商娜, 王真, 等. 高龄脓毒症患者28天死亡预测模型的构建及验证[J]. 中华急诊医学杂志, 2024, 33(4): 542-548. DOI:10.3760/cma.j.issn.1671-0282.2024.04.015 |
| [11] | Raith EP, Udy AA, Bailey M, et al. Prognostic accuracy of the SOFA score, SIRS criteria, and qSOFA score for in-hospital mortality among adults with suspected infection admitted to the intensive care unit[J]. Jama, 2017, 317(3): 290. DOI:10.1001/jama.2016.20328 |
| [12] | van der Woude SW, van Doormaal FF, Hutten BA, et al. Classifying sepsis patients in the emergency department using SIRS, qSOFA or MEWS[J]. Neth J Med, 2018, 76(4): 158-166. |
| [13] | Cox DR. Regression models and life-tables[J]. J R Stat Soc Ser B Stat Methodol, 1972, 34(2): 187-202. DOI:10.1111/j.2517-6161.1972.tb00899.x |
| [14] | Harrell FE, Lee KL, Mark DB. Multivariable prognostic models: issues in developing models, evaluating assumptions and adequacy, and measuring and reducing errors[J]. Statist Med, 1996, 15(4): 361-387. DOI:10.1002/(sici)1097-0258(19960229)15:4<361::aid-sim168>3.0.co;2-4 |
| [15] | Singer M, Deutschman CS, Seymour CW, et al. The third international consensus definitions for sepsis and septic shock (sepsis-3)[J]. Jama, 2016, 315(8): 801. DOI:10.1001/jama.2016.0287 |
| [16] | Zimmerman JE, Kramer AA, McNair DS, et al. Acute Physiology and Chronic Health Evaluation (APACHE) Ⅳ: Hospital mortality assessment for today's critically ill patients[J]. Crit Care Med, 2006, 34(5): 1297-1310. DOI:10.1097/01.ccm.0000215112.84523.f0 |
| [17] | Vincent JL, Sakr Y, Sprung CL, et al. Sepsis in European intensive care units: Results of the SOAP study[J]. Crit Care Med, 2006, 34(2): 344-353. DOI:10.1097/01.ccm.0000194725.48928.3a |
| [18] | Bellomo R, Ronco C, Mehta RL, et al. Acute kidney injury in the ICU: from injury to recovery: reports from the 5th Paris International Conference[J]. Ann Intensive Care, 2017, 7: 49. DOI:10.1186/s13613-017-0260-y |
| [19] | Hotchkiss RS, Monneret G, Payen D. Sepsis-induced immunosuppression: from cellular dysfunctions to immunotherapy[J]. Nat Rev Immunol, 2013, 13(12): 862-874. DOI:10.1038/nri3552 |
| [20] | Drewry AM, Samra N, Skrupky LP, et al. Persistent lymphopenia after diagnosis of sepsis predicts mortality[J]. Shock, 2014, 42(5): 383-391. DOI:10.1097/shk.0000000000000234 |
| [21] | 杨宏富, 李平娜, 崔秋敏, 等. 脓毒症患者淋巴细胞亚群分析及其对预后的影响[J]. 中华危重病急救医学, 2023, 35(7): 702-706. DOI:10.3760/cma.j.cn121430-20221230-01135 |
| [22] | van der Poll T, Shankar-Hari M, Wiersinga WJ. The immunology of sepsis[J]. Immunity, 2021, 54(11): 2450-2464. DOI:10.1016/j.immuni.2021.10.012 |
| [23] | Brochard L, Slutsky A, Pesenti A. Mechanical ventilation to minimize progression of lung injury in acute respiratory failure[J]. Am J Respir Crit Care Med, 2017, 195(4): 438-442. DOI:10.1164/rccm.201605-1081cp |
| [24] | Fan E, Del Sorbo L, Goligher EC, et al. An official American thoracic society/European society of intensive care medicine/society of critical care medicine clinical practice guideline: mechanical ventilation in adult patients with acute respiratory distress syndrome[J]. Am J Respir Crit Care Med, 2017, 195(9): 1253-1263. DOI:10.1164/rccm.201703-0548st |
| [25] | Barbar SD, Clere-Jehl R, Bourredjem A, et al. Timing of renal-replacement therapy in patients with acute kidney injury and sepsis[J]. N Engl J Med, 2018, 379(15): 1431-1442. DOI:10.1056/nejmoa1803213 |
| [26] | Lambden S, Laterre PF, Levy MM, et al. The SOFA score: development, utility and challenges of accurate assessment in clinical trials[J]. Crit Care, 2019, 23(1): 374. DOI:10.1186/s13054-019-2663-7 |
| [27] | Prescott HC, Osterholzer JJ, Langa KM, et al. Late mortality after sepsis: propensity matched cohort study[J]. BMJ, 2016: : i2375. DOI:10.1136/bmj.i2375 |
| [28] | 郝翠平, 李秋华, 张翠翠, 等. 重症监护病房脓毒症存活者生活质量现状及其影响因素分析[J]. 中华危重病急救医学, 2024, 36(1): 23-27. DOI:10.3760/cma.j.cn121430-20230814-00632 |
| [29] | Yende S, Kellum JA, Talisa VB, et al. Long-term host immune response trajectories among hospitalized patients with sepsis[J]. JAMA Netw Open, 2019, 2(8): e198686. DOI:10.1001/jamanetworkopen.2019.8686 |
 2026, Vol. 35
2026, Vol. 35