急性心力衰竭(acute heart failure, AHF)是常见急重症,6个月再住院率约50%,5年病死率高达60%,因此,必须快速诊断评估和紧急救治[1-4]。血清胆碱酯酶(serum cholinesterase, SChE)作为一种由肝脏合成的酶,传统上用于评估肝功能和营养状态[5-6]。近年来在AHF患者预后评估中的作用逐渐受到关注,研究发现入院时SChE、出院前SChE均和AHF患者的预后相关[7-11]。本研究旨在明确入院时SChE、出院前SChE和住院期间SChE变化值与重症AHF患者90 d预后的相关性,并比较其优劣性。
1 资料与方法 1.1 研究对象采用回顾性队列研究方法,收集北京医院急诊科2022年2月至2025年4月期间重症AHF患者的临床资料(北京医院伦理委员会伦理批号:2021BJYYEC-358-02),患者或其家属均签署知情同意书。
入选标准:年龄≥18岁,满足《中国心力衰竭诊断和治疗指南2018》中AHF的诊断标准,美国纽约心脏病协会(New York Heart Association,NYHA)心功能分级Ⅲ~Ⅳ级。排除标准:住院期间死亡者、心源性休克、有明显瓣膜狭窄、肥厚型或限制型心肌病、缩窄性心包炎、原发性肝病合并肝损伤者、服用胆碱酯酶抑制剂者、临床资料不完整者。通过电话随访患者来诊后90 d是否存活,将其分为存活组和死亡组。
1.2 数据收集记录患者入院时的基线资料:年龄、性别、BMI、既往病史,以及血C-反应蛋白(CRP)、白细胞(WBC)、血红蛋白(HGB)、白蛋白(ALB)、肌酐(Scr)、氨基末端B型利钠肽前体(N-terminal pro-B-type natriuretic peptide, NT-proBNP)。记录患者入院24 h内SChE、出院前48 h内SChE,并计算住院期间SChE下降百分比=(入院时SChE-出院前SChE)/入院时SChE×100。记录患者住院期间的超声心动图:用改良辛普森法测定的左室射血分数(left ventricular ejection fraction,LVEF)。
1.3 统计学方法计量资料正态分布指标用均数±标准差(x±s)表示,非正态分布指标用中位数(四分位数)[M(Q1,Q3)]表示。正态分布计量指标采用独立样本t检验进行两组间比较,非正态分布计量指标采用Mann-Whitney U检验进行两组间比较。计数指标以例数(%)形式表示,组间比较应用χ2检验。应用受试者工作特征(receiver operating characteristic,ROC)曲线比较入院时SChE、出院前SChE以及住院期间SChE下降百分比预测重症AHF患者90 d死亡的曲线下面积(area under curve,AUC),并使用DeLong检验比较其差异。基于ROC曲线Youden指数确定的最佳截断值将患者分为两组,采用Kaplan-Meier法绘制生存曲线,Log-rank检验比较组间差异。应用Cox比例风险分析重症AHF患者90 d死亡的独立预测因素。应用SPSS 23.0和R语言进行统计分析,P<0.05为差异有统计学意义。
2 结果 2.1 患者的一般临床资料根据本研究纳入标准,共收集到121例符合条件的重症AHF患者。其中男性69例、女性52例;存活69例、死亡52例。两组患者的基线临床资料比较见表 1。与存活组相比,死亡组患者的年龄、NT-proBNP水平更高,HGB、ALB水平更低,两组比较差异有统计学意义(P < 0.05)。与存活组相比,死亡组入院时SChE、出院前SChE水平更低,住院期间SChE下降百分比更高,两组比较差异有统计学意义(P < 0.05),见表 2。
| 指标 | 存活组(n=69) | 死亡组(n=52) | t/χ2/Z值 | P值 |
| 临床资料 | ||||
| 年龄(岁) | 77.42 ± 11.99 | 82.40 ± 9.95 | 2.432 | 0.016 |
| 高龄a [例(%)] | 35(50.72%) | 35(67.31%) | 3.344 | 0.067 |
| 男性[例(%)] | 36(52.17%) | 33(63.46%) | 1.542 | 0.214 |
| BMI | 24.26 ± 3.80 | 23.74 ± 4.37 | -0.700 | 0.485 |
| 既往病史 | ||||
| 高血压[例(%)] | 57(82.61%) | 40(76.92%) | 0.603 | 0.437 |
| 糖尿病[例(%)] | 41(59.42%) | 27(51.92%) | 0.677 | 0.411 |
| 冠心病[例(%)] | 38(55.07%) | 32(61.54%) | 0.508 | 0.476 |
| 房颤[例(%)] | 16(23.19%) | 17(32.69%) | 1.350 | 0.245 |
| 慢性肾脏病[例(%)] | 27(39.13%) | 26(50.00%) | 1.423 | 0.233 |
| 超声心动图 | ||||
| LVEF(%) | 40(30,54) | 41(30,51) | -0.060 | 0.952 |
| 实验室数据 | ||||
| CRP(mg/L) | 14.00(5.53, 57.00) | 32.40(7.08, 61.96) | -1.056 | 0.291 |
| WBC(×109/L) | 8.85(7.05, 10.69) | 8.54(7.09, 10.67) | -0.094 | 0.925 |
| HGB(g/L) | 105.0(90.0, 102.5) | 91.0(78.0, 114.0) | -2.467 | 0.014 |
| ALB(g/L) | 36.26 ± 5.71 | 33.35 ± 5.07 | -2.916 | 0.004 |
| Scr(μmol/L) | 144.00(101.25, 222.75) | 195.00(107.00, 353.00) | -1.872 | 0.061 |
| NT-proBNP(pg/mL) | 6712(3 889, 16 908) | 16284(5 488, 27 797) | -2.617 | 0.009 |
| 注:BMI:体质指数;LVEF:左室射血分数;CRP:C-反应蛋白;WBC:血白细胞;HGB:血红蛋白;ALB:血白蛋白;Scr:血肌酐;NT-proBNP:氨基末端钠尿肽前体;高龄a:指年龄≥80岁 | ||||
| 指标 | 存活组(n=69) | 死亡组(n=52) | Z值 | P值 |
| 入院时SChE(U/L) | 5261.00(4437.00, 6323.00) | 3922.00(2614.75, 5253.75) | -4.262 | <0.001 |
| 出院前SChE(U/L) | 5007.00(4018.50, 6050.50) | 2850.50(1846.75, 4812.25) | -5.369 | <0.001 |
| 住院期间SChE下降百分比(%) | 4.19(-11.12, 17.80) | 20.82(3.25, 41.95) | -3.477 | 0.001 |
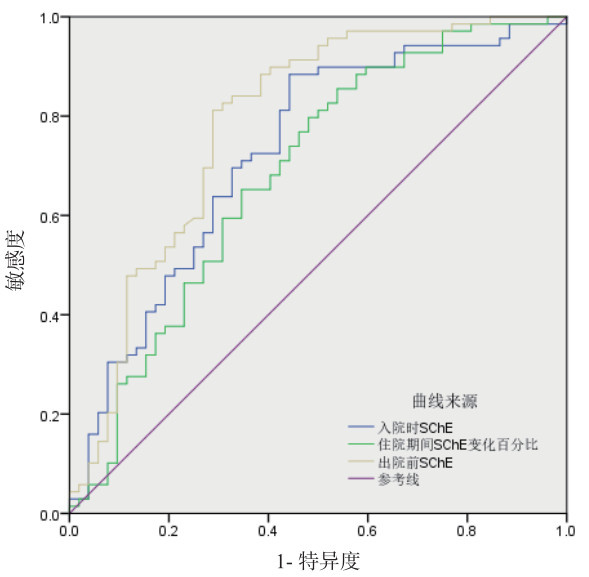
采用ROC曲线分析入院时SChE、出院前SChE以及住院期间SChE下降百分比对重症AHF患者的90 d死亡均有预测能力,但出院前SChE的预测能力最优(AUC=0.786,95%CI: 0.699~0.873,P<0.001)。DeLong检验显示,出院前SChE的预测效能显著优于住院期间SChE下降百分比(Z=2.438,P =0.015),但与入院时SChE的差异无统计学意义(Z=-1.610,P =0.107),入院时SChE与住院期间SChE下降百分比的预测能力差异无统计学意义(Z=0.617,P =0.537)。基于ROC曲线Youden指数确定的出院前SChE最佳截断值是3 881.5 U/L,其敏感度为81.2%,特异度为71.2%。见图 1、表 3。
|
| 图 1 入院时SChE、出院前SChE以及住院期间SChE下降百分比预测90 d死亡的ROC曲线 Fig 1 ROC curves for predicting 90-day mortality based on admission SChE, pre-discharge SChE, and in-hospital SChE reduction |
|
|
| 变量 | AUC | SE | 95%CI | P值 | Youden指数 | 截断值 | 敏感度(%) | 特异度(%) |
| 入院时SChE | 0.727 | 0.047 | 0.634~0.820 | 0.000 | 0.442 | 4 020.0 U/L | 88.4 | 55.8 |
| 出院前SChE | 0.786 | 0.044 | 0.699~0.873 | 0.000 | 0.524 | 3 881.5 U/L | 81.2 | 71.2 |
| 住院期间SChE下降百分比 | 0.685 | 0.050 | 0.587~0.783 | 0.001 | 0.317 | 22.4% | 46.2 | 85.5 |
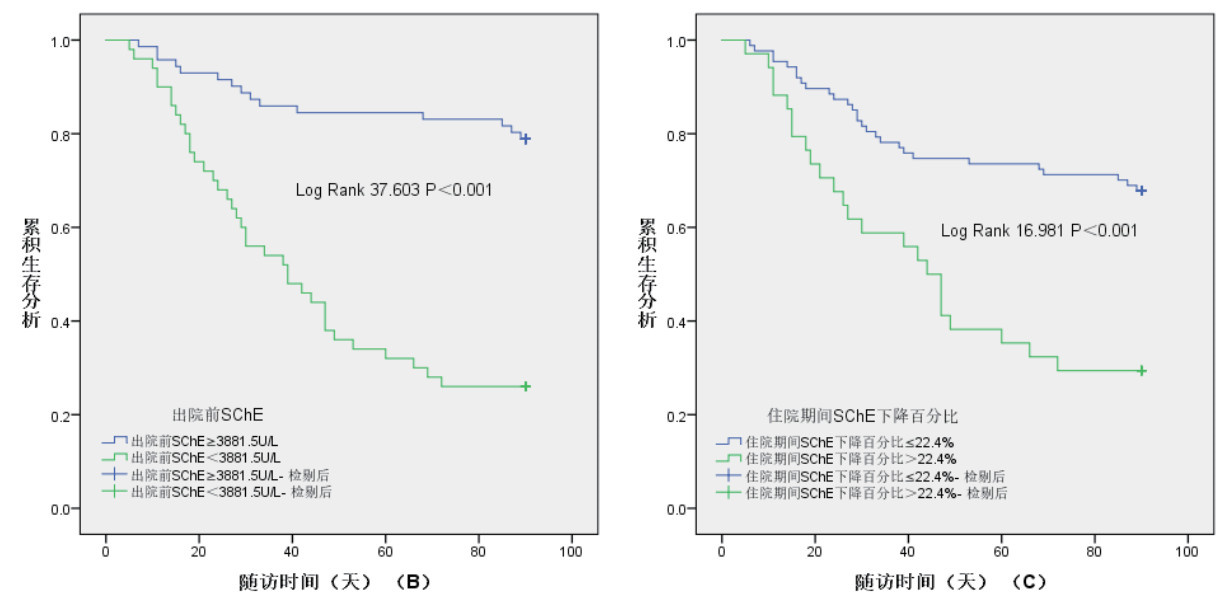
根据入院时SChE最佳截断值分为≥4 020 U/L和<4 020 U/L两组,Kaplan-Meier生存曲线显示<4 020 U/L组90 d累积生存率显著低于≥4 020U/L组(21.6% vs. 72.6%,Log-rank 38.025,P<0.001)(图 2A)。根据出院前SChE最佳截断值分为≥3 881.5 U/L和<3 881.5 U/L两组,Kaplan-Meier生存曲线显示<3 881.5 U/L组90 d累积生存率显著低于≥3 881.5 U/L组(26.0% vs. 78.9%,Log-rank 37.603,P<0.001)(图 2B)。根据住院期间SChE下降百分比最佳截断值分为≤22.4%和>22.4%两组,Kaplan-Meier生存曲线显示>22.4%组90 d累积生存率显著低于≤22.4%组(29.4% vs. 67.8%,Log-rank 16.981,P<0.001)(图 2C)。
|
| A为根据入院时SChE最佳截断值分组;B为根据出院前SChE最佳截断值分组;C为根据住院期间SChE下降百分比最佳截断值分组 图 2 根据入院时SChE(A)、出院前SChE(B)、住院期间SChE下降百分比(C)的最佳截断值分组的90天死亡Kaplan-Meier生存曲线 Fig 2 Kaplan-Meier survival curves for 90-day mortality, stratified by the optimal cutoff values of admission SChE (A), pre-discharge SChE (B), and in-hospital SChE reduction (C) |
|
|
多因素Cox回归分析显示,校正年龄、出院前HGB、ALB、NT-proBNP后,出院前SChE每升高1 000 U/L,重症AHF患者90 d死亡风险降低28.9%(HR=0.711,95%CI: 0.587~0.860,P < 0.001),提示出院前SChE是重症AHF患者90 d死亡的独立影响因素,其水平越高病死率越低。
3 讨论近年来,多种生物标志物和参数被用于AHF的预后评估,其中B型利钠肽(brain natriuretic polypeptide, BNP)/NT-proBNP是AHF诊断、危险分层和预后评估的首选生物标志物[12-14],但其水平易受年龄、性别、肾功能、肥胖等多种因素的干扰,且无法反映疾病对营养代谢的影响[15]。SChE作为反映肝功能与营养状态的标志物[16-17],近年来在AHF患者的预后评估中逐渐受到关注,研究发现入院时SChE通过反映基础营养储备状况,以及心力衰竭急性发作期肝淤血和多器官受累的严重程度[7-8],出院前SChE通过反映营养状况受损,以及治疗后肝脏淤血和多器官受累的缓解程度[9-11],均成为评估AHF患者预后的有效生物标志物。本研究旨在明确入院时SChE、出院前SChE和住院期间SChE变化值与重症AHF患者90 d预后的相关性,并比较其优劣性。
本研究结果显示,与存活组相比,死亡组患者入院时SChE、出院前SChE水平更低,两组比较差异有统计学意义(Z=-4.262,P < 0.001;Z=-5.369,P < 0.001),提示低入院时SChE、出院前SChE水平均与重症AHF患者的90 d不良预后相关。同时,与存活组相比,死亡组患者的入院时HGB、ALB水平更低,NT-proBNP水平更高,提示死亡组患者基础营养储备状况更差、心力衰竭程度更重。进一步采用ROC曲线分析得出入院时SChE、出院前SChE对重症AHF患者的90 d死亡均有显著预测能力(AUC=0.727,95%CI: 0.634~0.820,P<0.001;AUC=0.786,95%CI: 0.699~0.873,P<0.001)。同样,Shiba等[7]研究发现,入院时低SChE水平与AHF患者的肝淤血和营养不良相关,是AHF患者不良预后的独立预测因素;Seo等[9]研究发现,急性失代偿性心力衰竭患者出院前低SChE能精准识别治疗后仍处于高风险状态的患者。本研究发现了SChE与重症AHF患者营养状况和心力衰竭严重程度的相关性,并进一步验证了SChE在重症AHF患者90 d预后评估中的作用。
心力衰竭呈动态演变的过程,尤其是重症AHF具有病情重、变化快等特点。中国专家共识[18]中指出,与入院生物标志物水平相比,出院前和住院期间变化率与AHF者预后的关系更为显著。相比单点测量而言,生物标志物住院期间的变化情况可能更能反映病情的变化趋势[19-21]。本研究结果显示,与存活组相比,死亡组患者住院期间SChE下降百分比更高,两组比较差异有统计学意义(Z=-3.477,P =0.001),提示住院期间SChE下降百分比与重症AHF患者的90 d不良预后相关。进一步采用ROC曲线分析得出住院期间SChE下降百分比对重症AHF患者90 d死亡亦有一定的预测能力,但效能较弱(AUC=0.685,95%CI: 0.587~0.783,P =0.001)。分析可能与住院期间SChE变化情况仅纳入了入院时和出院前两个时间点,且仅计算其变化百分比,不能全面地反映病情变化的全过程及最终状态,进而削弱了其对预后的预测能力。Omar等[22]研究同样得出,住院期间BNP降幅预测AHF患者短期死亡的效能较差,分析与AHF患者BNP变化的复杂性及BNP本身的代谢特点有关,进而难以准确地体现治疗应答和预后关联。《心力衰竭生物标志物临床应用中国专家共识》[23]中推荐检测生物标志物基线水平,并动态监测治疗后其水平变化,以用于危险分层和疗效评估。未来可将单点测量和动态变化相结合,进一步验证其预测效能。
本研究进一步通过DeLong检验得出,出院前SChE的预测效能(AUC=0.786,95%CI: 0.699~0.873,P<0.001)显著优于住院期间SChE下降百分比(AUC=0.685,95%CI: 0.587~0.783,P =0.001),且两者的差异有统计学意义(Z=2.438,P =0.015);出院前SChE的预测效能(AUC=0.786,95%CI: 0.699~0.873,P<0.001)优于入院时SChE(AUC=0.727,95%CI: 0.634~0.820,P<0.001),但两者的差异未达到统计学意义(Z=-1.610,P =0.107)。分析出院前SChE作为治疗后的状态指标,综合了疾病的严重程度、治疗反应及机体的恢复能力,比仅反映急性病状态的入院时SChE和仅反映治疗反应的住院期间SChE下降百分比更能有效地预测重症AHF患者的预后。与既往研究结果类似[22, 24],相较于入院时或住院期间变化,出院时生物标志物(BNP)水平预测心力衰竭患者不良预后的能力最优。
本研究基于ROC曲线Youden指数确定的出院前SChE最佳截断值3 881.5 U/L(敏感度81.2%,特异度71.2%)进行分组,Kaplan-Meier生存曲线显示<3 881.5 U/L组90 d累积生存率显著低于≥3 881.5 U/L组(26.0% vs. 78.9%,Log-rank 37.603,P<0.001)。更进一步证实了出院前SChE作为重症AHF患者90 d预后评估的价值,同时为临床实践提供了客观依据,即对于出院前SChE<3 881.5 U/L的重症AHF患者,需加强出院后随访、优化治疗方案,以降低其90 d死亡风险。在一些临床实践指南中,也强调了基于生物标志物截断值对AHF患者进行分层管理的重要性,通过这种方式可优化医疗资源分配,实现个体化治疗,进而改善患者的预后[25-26]。
本研究基线临床资料显示,与存活组相比,死亡组患者的年龄、NT-proBNP水平更高,HGB、ALB水平更低,提示重症AHF患者的预后还受年龄、HGB、ALB、NT-proBNP等其他多种因素的影响。因此,本研究进一步采用多因素Cox回归分析结果显示,校正年龄、出院前HGB、ALB、NT-proBNP后,出院前SChE每升高1 000 U/L,重症AHF患者90 d死亡风险降低28.9%(HR=0.711,95%CI: 0.587~0.860,P < 0.001),得出出院前SChE是重症AHF患者90 d死亡的独立影响因素,其水平越高病死率越低。
局限性:本研究为单中心回顾性研究,可能存在选择偏倚、统计效能差、混杂因素控制不足等问题,需要多中心大样本前瞻性研究进一步验证。未来可开展前瞻性队列研究,并探索与其他生物标志物(如NT-proBNP)联合应用的预测效能,以进一步提高预后评估的准确性。
综上所述,与入院时SChE和住院期间SChE变化值相比,出院前SChE水平预测重症AHF患者90天预后的效能最优。出院前SChE水平是重症AHF患者90 d死亡的独立影响因素,其水平越高病死率越低。
利益冲突 所有作者声明无利益冲突
作者贡献声明 王凡:研究设计,研究实施,数据收集,数据整理,统计分析,论文撰写;温伟:研究设计,技术指导,论文修改,研究经费及行政支持
| [1] | 中国医师协会急诊医师分会, 中国心胸血管麻醉学会急救与复苏分会. 中国急性心力衰竭急诊临床实践指南(2017)[J]. 中华急诊医学杂志, 2017, 26(12): 1347-1357. DOI:10.3760/cma.j.issn.1671-0282.2017.12.003 |
| [2] | 中国医疗保健国际交流促进会急诊医学分会, 中华医学会急诊医学分会, 中国医师协会急诊医师分会, 等. 急性心力衰竭中国急诊管理指南(2022)[J]. 中华急诊医学杂志, 2022, 31(8): 1016-1041. DOI:10.3760/cma.j.issn.1671-0282.2022.08.003 |
| [3] | Cao LJ, Pei YY, Ma XL, et al. A risk prediction model for acute kidney injury following acute heart failure in an emergency department cohort in China[J]. World J Emerg Med, 2025, 16(4): 348. DOI:10.5847/wjem.j.1920-8642.2025.068 |
| [4] | Liu QY, Zhang YX, Sun J, et al. Early identification of high-risk patients admitted to emergency departments using vital signs and machine learning[J]. World J Emerg Med, 2025, 16(2): 113. DOI:10.5847/wjem.j.1920-8642.2025.031 |
| [5] | Liu JP, Shao TY, Chen HW, et al. Serum cholinesterase as a new nutritional indicator for predicting weaning failure in patients[J]. Front Med, 2023, 10: 1175089. DOI:10.3389/fmed.2023.1175089 |
| [6] | Abbas M, Abbas Z. Serum cholinesterase: a predictive biomarker of hepatic reserves in chronic hepatitis D[J]. World J Hepatol, 2017, 9(22): 967. DOI:10.4254/wjh.v9.i22.967 |
| [7] | Shiba M, Kato T, Morimoto T, et al. Serum cholinesterase as a prognostic biomarker for acute heart failure[J]. Eur Heart J Acute Cardiovasc Care, 2021, 10(3): 335-342. DOI:10.1093/ehjacc/zuaa043 |
| [8] | 赵香梅, 徐雅欣, 王泽华, 等. 血清胆碱酯酶在急性失代偿性心力衰竭患者预后评估中的作用[J]. 中华急诊医学杂志, 2024, 33(2): 234-241. DOI:10.3760/cma.j.issn.1671-0282.2024.02.017 |
| [9] | Seo M, Yamada T, Tamaki S, et al. Prognostic significance of serum cholinesterase in patients with acute decompensated heart failure: a prospective comparative study with other nutritional indices[J]. Am J Clin Nutr, 2019, 110(2): 330-339. DOI:10.1093/ajcn/nqz103 |
| [10] | Seo M, Yamada T, Tamaki S, et al. Prognostic significance of serum cholinesterase level in patients with acute decompensated heart failure with preserved ejection fraction: insights from the PURSUIT-HFpEF registry[J]. J Am Heart Assoc, 2020, 9(1): e014100. DOI:10.1161/jaha.119.014100 |
| [11] | Sato T, Yamauchi H, Suzuki S, et al. Serum cholinesterase is an important prognostic factor in chronic heart failure[J]. Heart Vessels, 2015, 30(2): 204-210. DOI:10.1007/s00380-014-0469-8 |
| [12] | 张宏亮, 吴丹, 陈立文, 等. 中心静脉-动脉二氧化碳分压差与动脉-中心静脉氧含量差比值联合外周灌注指数对急性心力衰竭合并低灌注患者预后的预测[J]. 中华急诊医学杂志, 2025, 34(5): 692-697. DOI:10.3760/cma.j.issn.1671-0282.2025.05.013 |
| [13] | Maisel AS, Krishnaswamy P, Nowak RM, et al. Rapid measurement of B-type natriuretic peptide in the emergency diagnosis of heart failure[J]. N Engl J Med, 2002, 347(3): 161-167. DOI:10.1056/nejmoa020233 |
| [14] | Castiglione V, Aimo A, Vergaro G, et al. Biomarkers for the diagnosis and management of heart failure[J]. Heart Fail Rev, 2022, 27(2): 625-643. DOI:10.1007/s10741-021-10105-w |
| [15] | 中国医师协会检验医师分会心血管专家委员会. B型利钠肽及N末端B型利钠肽前体实验室检测与临床应用中国专家共识[J]. 中华医学杂志, 2022, 102(35): 2738-2754. DOI:10.3760/cma.j.cn112137-20220714-01553 |
| [16] | Santarpia L, Grandone I, Contaldo F, et al. Butyrylcholinesterase as a prognostic marker: a review of the literature[J]. J Cachexia Sarcopenia Muscle, 2013, 4(1): 31-39. DOI:10.1007/s13539-012-0083-5 |
| [17] | Gokani RS, Jadav PA, Shaikh N, et al. Serum cholinesterase as diagnostic marker of liver disease[J]. Int J Biomed & Adv Res, 2014, 5(9): 439. DOI:10.7439/ijbar.v5i9.890 |
| [18] | 中国医疗保健国际交流促进会循证医学分会, 海峡两岸医药卫生交流协会老年医学专业委员会. 心力衰竭生物标志物中国专家共识[J]. 中华检验医学杂志, 2020, 43(2): 130-141. DOI:10.3760/cma.j.issn.1009-9158.2020.02.007 |
| [19] | Varga NI, Benea AT, Suba MI, et al. Predicting mortality in sepsis: the role of dynamic biomarker changes and clinical scores: a retrospective cohort study[J]. Diagnostics, 2024, 14(17): 1973. DOI:10.3390/diagnostics14171973 |
| [20] | Arbeev KG, Ukraintseva SV, Yashin AI. Dynamics of biomarkers in relation to aging and mortality[J]. Mech Ageing Dev, 2016, 156: 42-54. DOI:10.1016/j.mad.2016.04.010 |
| [21] | Salah K, Kok WE, Eurlings LW, et al. A novel discharge risk model for patients hospitalised for acute decompensated heart failure incorporating N-terminal pro-B-type natriuretic peptide levels: a European coLlaboration on Acute decompeNsated Heart Failure: éLAN-HF Score[J]. Heart, 2014, 100(2): 115-125. DOI:10.1136/heartjnl-2013-303632 |
| [22] | Omar HR, Guglin M. Discharge BNP is a stronger predictor of 6-month mortality in acute heart failure compared with baseline BNP and admission-to-discharge percentage BNP reduction[J]. Int J Cardiol, 2016, 221: 1116-1122. DOI:10.1016/j.ijcard.2016.07.117 |
| [23] | 中国医师协会心力衰竭专业委员会, 国家心血管病专家委员会心力衰竭专业委员会, 中华心力衰竭和心肌病杂志编辑委员会. 心力衰竭生物标志物临床应用中国专家共识[J]. 中华心力衰竭和心肌病杂志, 2022, 6(3): 175-192. DOI:10.3760/cma.j.cn101460-20220810-00071 |
| [24] | Kociol RD, Horton JR, Fonarow GC, et al. Admission, discharge, or change in B-type natriuretic peptide and long-term outcomes: data from organized program to initiate lifesaving treatment in hospitalized patients with heart failure (OPTIMIZE-HF) linked to medicare claims[J]. Circ Heart Fail, 2011, 4(5): 628-636. DOI:10.1161/circheartfailure.111.962290 |
| [25] | 中华医学会心血管病学分会, 中国医师协会心血管内科医师分会, 中国医师协会心力衰竭专业委员会, 中华心血管病杂志编辑委员会. 中国心力衰竭诊断和治疗指南2024[J]. 中华心血管病杂志, 2024, 52(3): 235-275. DOI:10.3760/cma.j.cn112148-20231101-00405 |
| [26] | McDonagh TA, Metra M, Adamo M, et al. 2023 Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure[J]. Eur Heart J, 2023, 44(37): 3627-3639. DOI:10.1093/eurheartj/ehad195 |
 2026, Vol. 35
2026, Vol. 35