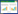急性播散性脑脊髓炎(acute disseminated encephalomyelitis,ADEM)和吉兰-巴雷综合征(Guillain-Barré syndrome,GBS)是两种神经系统自身免疫性疾病,ADEM是一种中枢神经系统脱髓鞘疾病,会导致脑部、脑干和/或脊髓出现脑病和多处白质病变,GBS则是周围神经系统的一种炎症性脱髓鞘疾病,主要影响周围神经及其脊髓根,导致多个肢体出现进行性的对称性运动无力,伴有反射减弱或无反射,通常表现为多种形式,如急性轴突神经病变[1-3]。尽管这2种疾病都表现为急性感染后或接种疫苗后的炎症性脱髓鞘病程,但它们实际上是不同的神经系统疾病,同时出现这两种疾病作为对同一刺激的免疫反应的情况非常少见,而由肺炎衣原体(chlamydia pneumoniae, CPN)感染诱发的ADEM和GBS重叠则更为罕见。现以一例成人CPN肺炎急性期合并ADEM和GBS重叠为例结合相关文献回顾分析该病的诊疗过程,以提高临床医师对该病的认识。本研究已获泉州市第一医院伦理委员会批准[批件号:泉一伦【2025】K487号]。
1 资料与方法 1.1 入院病历资料患者女性,36岁,因“反复发热7 d”于2025年6月25日入住本院感染科。入院7 d前出现发热,最高体温39℃,伴畏冷、寒战,6月24日就诊当地医院,查血常规未见明显异常,C反应蛋白26.2 mg/L,红细胞沉降率50 mm/h,纤维蛋白原5.69 g/L,血清生化,丙氨酸氨基转移酶331.9 U/L,天冬氨酸氨基转移酶246.6 U/L,谷氨酰转移酶120.7 U/L, 碱性磷酸酶109.1 U/L,胸部CT:左下肺异常密度影,炎症性病变可能”, 予保肝、“左氧氟沙星0.5 g静滴, 1次/d、头孢曲松2 g静滴, 1次/d”抗感染治疗,但仍反复发热,转诊本院,复查胸部CT:左肺下叶炎症改变,考虑感染性病变(图 1)。既往体健,否认任何毒物、药物上瘾史。入院查体:体温37℃,脉搏77次/min,呼吸20次/min,血压97/55 mmHg。神志清楚,精神疲乏,双肺呼吸音稍粗,双肺未闻及干湿性啰音。神经系统查体未见异常。入院诊断:社区获得性肺炎; 肝功能不全。
|
| 图 1 胸部CT提示: 左肺下叶见斑片状高密度影,部分呈磨玻璃样改变,可见支气管充气征,边缘模糊,密度不均(箭头所示) |
|
|
入院后予“奈诺沙星”抗感染及保肝等治疗。实验室检查:血常规、C反应蛋白、降钙素原正常; 肝素结合蛋白11.63 ng/mL。入院后第1~3天呈稽留高热,体温在38.4~40.4℃,伴畏冷、乏力、头晕。6月28日出现进食后呕吐,视物重影,对称性四肢无力,无法站立及行走,逐渐出现精神症状,调整奈诺沙星为阿奇霉素抗感染治疗并行腰椎穿刺检查,脑脊液压力300 mmH2O,外观无色透明,潘氏试验阳性(+),细胞计数59×106/L,多个核细胞3.4%,单个核细胞96.6%,脑脊液葡萄糖3.55 mmol/L,氯118.7 mmol/L,蛋白定量1 157 mg/L; 脑脊液目标序列捕获测序(targeted next-generation sequencing,tNGS)未检出致病微生物。持续高热不退,考虑结核病可能,予HRZE方案诊断性抗结核,并加用甲泼尼龙抗炎,甘露醇降颅压等处理,病情未见改善,逐渐出现昏迷、肢体抽搐,6月30日转入重症医学科,体温38.1℃,呈浅昏迷状态,双肺呼吸音稍粗,可闻及明显痰鸣音,颈强直,肌力检查无法配合,肌张力对称性稍增高,双侧巴氏征阴性。予气管插管接呼吸机支持、抗癫痫、镇痛及调整抗感染方案为美罗培南联合氟康唑及诊断性抗结核等处理。患者呕吐、抽搐、意识障碍及颈强直,并且脑脊液检查提示细胞数及蛋白定量异常,转科诊断:脑膜脑炎,予加用地塞米松10 mg静推抗炎并予完善肺泡灌洗液宏基因组二代测序(metagenomics next-generation sequencing,mNGS)发现CPN(序列数12318,相对丰度1.483%); CPN-IgM抗体阳性。脑脊液mNGS(DNA+RNA)未检出任何致病微生物,遂调整抗感染方案为莫西沙星0.4 g/d静滴联合多西环素0.1 g/12 h口服抗感染治疗。
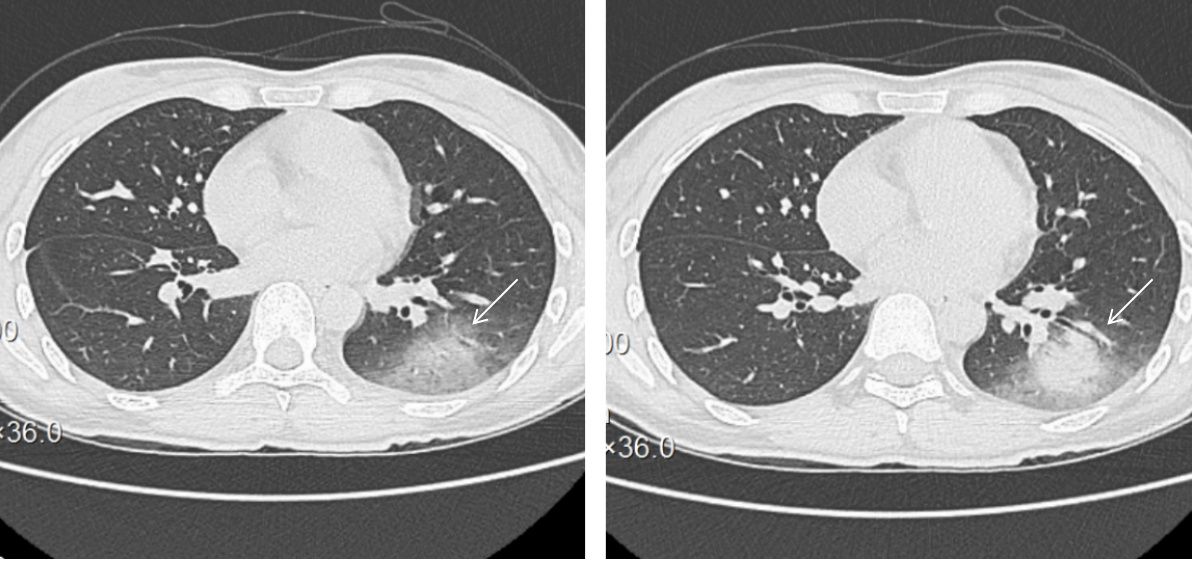
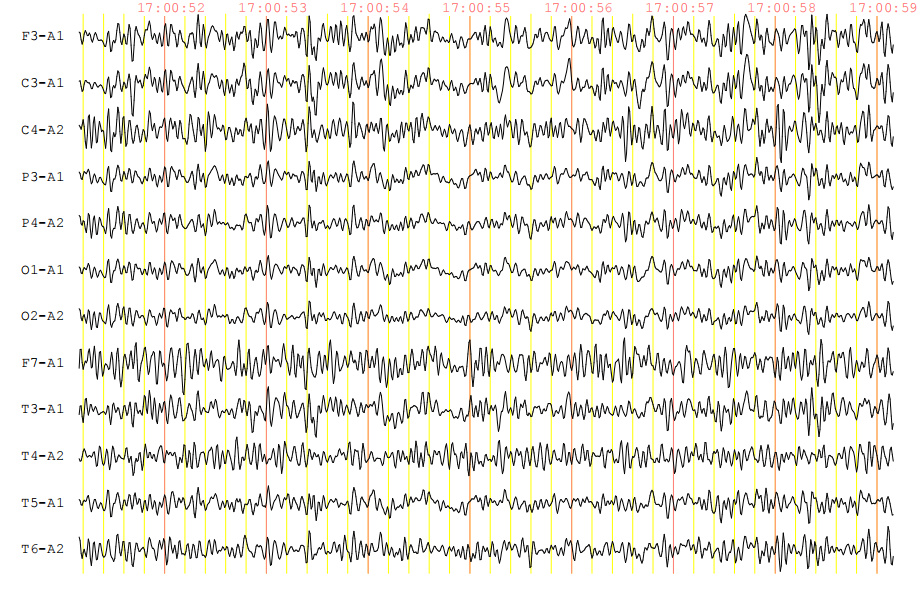
7月2日体温转正常,神志转清楚,但发现四肢肌力明显对称性减弱,医学研究委员会(MRC)总评分为0/60,上下肢肌张力稍微增高,全身感觉正常。复查腰椎穿刺检查,脑脊液压力135 mmH2O,脑脊液外观淡黄色,潘氏试验阳性,细胞计数63×106/L,单个核细胞100.0%,葡萄糖3.61 mmol/L(同期末梢指尖血糖9.3 mmol/L),氯125.9 mmol/L,蛋白定量1 399 mg/L; 动态脑电图提示:重度异常动态脑电图(图 2); 肌电图提示:左右胫前肌、左腓肠肌内侧头、右第一骨间肌未见明显纤颤、正尖波,轻重收缩募集相减少; 神经传导速度测定:左右腓总神经运动传导仅见微小波动,左右正中神经、左右尺神经、右胫神F波出现率降低或未引出; 重复神经电刺激未见明显异常。脑脊髓MRI提示:双侧额叶、右侧脑室后角旁白质及脑干多发异常信号并脑膜、脊膜强化,脑膜脑炎可能(图 3)。血清和脑脊液样本分别送检基于组织底物的间接免疫荧光法筛查三项、副肿瘤综合征18项抗体、自身免疫性脑炎21项抗体、中枢神经脱髓鞘7项抗体均为阴性; 血清周围神经病30项抗体中抗GT1a抗体IgM强阳性。修正诊断为CPN肺炎并ADEM和GBS重叠,予人免疫球蛋白(20 g/d,共5 d)和甲基强的松龙(80 mg/d,共3 d),然后口服泼尼松剂量[1 mg/(kg·d)],缓慢减少。治疗过程中发现颜面部肌肉瘫痪,口咽、颈部和上肢无力表现更为突出,患者在神志清楚,气道呛咳反射和咳嗽峰流速正常情况下因无法吞咽并气道保护能力差,拔管失败2次,随着治疗延续及康复干预,吞咽功能改善,气管插管17 d后才成功拔除气管插管。
|
| 图 2 脑电图示:双侧各程可见额区低波幅13c/s β波间断发放,未见明显α波,调节、调幅差可。未见眼动波及睡眠波。记录中未见典型的棘波、尖波发放 |
|
|
|
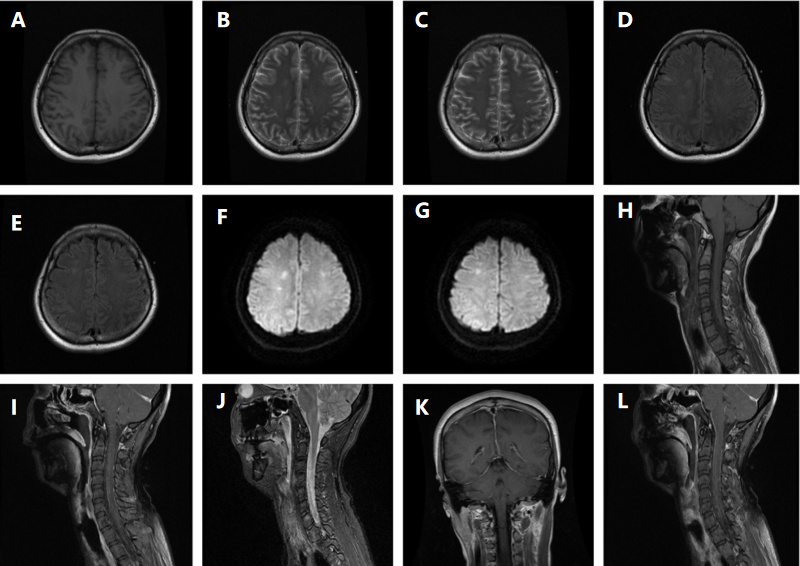
| MRI: 双侧额叶皮层下白质区、右侧脑室后角旁白质,T1WI呈等、稍低信号(A),T2WI(B、C)、T2flair呈高信号(D、E),DWI呈稍高信号(F、G); 脑干见多发斑点、斑片状异常信号, T1WI呈等、稍低信号(H),增强后未见强化(I),T2WI呈高信号(J); 增强扫描硬脑膜可见硬化(K、L) 图 3 颅脑脊髓 |
|
|
7月17日复查神经传导速度测定:左右腓总神经(趾短伸肌记录)运动传导仅见微小波动; 左右胫神经F波未引出; 左正中神经F波潜伏期正常范围、出现率降低; 神经学检查肌力明显改善,(MRC)总评分为50/60,转出重症医学科。7月31日患者肌力完全恢复,意识状态良好,复查脑MRI平扫+增强未见异常,泼尼松逐步减停,6个月后随访时,临床状况完全恢复。随访期间重复进行的神经传导检查结果为正常。
2 文献复习以“肺炎衣原体”和“脑炎”或“吉兰-巴雷综合征”或“急性播散性脑脊髓炎”为检索词,在万方数据库、中国知网,检索2025年12月25日之前所有报道的国内病例。以“Chlamydia pneumoniae”和“encephalitis”或“Guillain–Barré syndrome”或“acute disseminated encephalomyelitis”为检索词,在PubMed上检索2025年12月25日之前的病例。
报道了11例与CPN有关的急性脑炎病例[4-14], 主要涉及年轻患者(其中2例年龄大于60岁),有1例长期口服强的松[14],神经系统症状通常发生在急性呼吸道感染后(2 d至3周)。这些患者的预后通常是良好的,然而,在1个病例中,由于医院内感染导致病情复杂化[5]; 在另1个病例中合并噬血细胞综合征,部分恢复[12]; 在另2个病例中报告了包括记忆力减退和癫痫在内的神经系统后遗症[8, 14],还有另1个病例出现了哮喘[11]; 1名高龄患者死于吸入性肺炎[7]。
检索到一些与CPN有关的ADEM或GBS病例[15-18](表 1),发病前均有发热等呼吸道感染症状,逐渐出现神经系统症状,经免疫球蛋白、激素等治疗,普遍预后较好,但其中1例因继发念珠菌血症,给诊疗增加了困难[17]。Azumagawa等[16]报道的为接种麻疹风疹二联疫苗加强剂及日本脑炎疫苗加强剂第2天出现发热、头痛及呕吐症状,在发病第10天考虑接种后ADEM,予静脉注射大剂量甲泼尼龙[30mg/(kg·d)]后续贯泼尼松20 mg/d口服,症状于第15天完全消失,减量激素过程中有症状反复,调整激素用量后控制,逐渐停用激素,在3个月后再次出现发热、头痛、复视,血清中CPN- IgM和IgG抗体呈阳性反应,考虑CPN相关多相播散性脑脊髓炎(multiphasic disseminated encephalomyelitis,MDEM),予10~20 mg/d泼尼松龙维持治疗两年。
| 文献 | Heick A[15] | Azumagawa K[16] | Wong CK[17] | Papantoniou M[18] | 本例 |
| 性别/年龄(岁) | 女/18 | 男/6 | 男/48 | 男/60 | 女/36 |
| 呼吸道症状 | 发热、干咳、胸痛一周 | 接种后ADEM康复后再次出现发热、头痛等流感症状 | 无呼吸道症状 | 上呼吸道感染症状 | 发热 |
| 神经系统症状 | 呼吸道症状7 d后出现左侧偏瘫, 并注意到共济失调。左侧眼球震颤、左侧外展肌麻痹和中央面瘫 | 颈部僵硬及性格改变(易怒)复视 | 发热、头痛、视力模糊和呕吐,言语不连贯,昏睡,双侧面部无力、眼肌麻痹伴共济失调以及四肢无力 | 3周后出现烦躁、行走困难、全身肌肉无力和麻木,尤其是左下肢 | 10 d后出现呕吐、视物重影、四肢无力、昏迷、抽搐,颈部强直 |
| 脑脊液检查 | 蛋白升高770 mg/L和细胞数25×106/L | 细胞数99×106/L,髓鞘碱性蛋白0.446 mg/L,复发时未行腰椎穿刺 | 脑脊液蛋白883 mg/L,细胞数量较少,细胞白蛋白分离现象 | 细胞数12×106 /L,蛋白1 070 mg/L | 细胞数59×106/L,蛋白定量1 157 mg/L |
| 肺炎衣原体病原学证据 | 血清肺炎衣原体IgM抗体呈阳性。咽拭子PCR检测显示肺炎衣原体核酸阳性。脑脊液肺炎衣原体PCR检测阴性 | 血清肺炎衣原体IgM和IgG抗体呈阳性 | 血清肺炎衣原体IgM阳性 | 血清肺炎衣原体IgM和IgG抗体阳性 | 肺泡灌洗液mNGS检出肺炎衣原体序列,血清肺炎衣原体IgM阳性,脑脊液tNGS、mNGS(DNA+RNA)阴性 |
| 磁共振 | 脑MRI显示典型ADEM的局灶性异常,主要在右侧,从延髓延伸到右侧内囊 | 脑MRI显示T2加权和FLAIR序列中脑背侧区域存在病灶 | 脑MRI显示,在T2加权和FLAIR序列中,左侧枕叶区域出现环状高信号 | 脑MRI显示T2加权和FLAIR序列双侧大脑半球、小脑及周围区域信号病变 | 脑脊髓MRI提示双侧额叶、右侧脑室后角旁白质及脑干多发异常信号并脑膜、脊膜强化,脑膜脑炎可能 |
| 诊断的神经系统自身免疫性疾病 | 肺炎衣原体相关ADEM | 接种后ADEM,CPN相关多相播散性脑脊髓炎 | 肺炎衣原体相关脑干脑炎和GBS重叠 | 肺炎衣原体相关ADEM和GBS重叠 | 肺炎衣原体相关ADEM和GBS重叠 |
| 相关抗体检测 | NA | 血清抗MOG IgG抗体 | NA | 抗MOG-IgG抗体和抗硫酸酯IgG抗体阳性 | 抗GT1a抗体IgM强阳性 |
| 治疗方案 | 多西环素200 mg/8 h负荷剂量后,100 mg/8 h 2周抗感染; 静脉注射甲泼尼龙120 mg/d共10 d | 10~20 mg/d泼尼松龙维持2年 | 静脉注射免疫球蛋白[0.4 g/(kg· d)]和甲基强的松龙(1 g/d)共5 d | 静脉注射免疫球蛋白(30 g/d,共5 d)和甲基强的松龙(1 000 mg/d,共3 d) | 静脉注射免疫球蛋白(20 g/d,共5 d)和甲基强的松龙(80 mg/d,共3 d),续贯激素减量 |
| 预后 | 完全康复 | 康复 | 完全康复 | 康复 | 康复 |
| 注:ADEM急性播散性脑脊髓炎; GBS吉兰-巴雷综合征; mNGS宏基因组二代测序; tNGS目标序列捕获测序; NA未检查 | |||||
这些病例除本例通过mNGS精准定位病原菌,其余均通过检查血清和或脑脊液CPN相关抗体并结合临床表现诊断为CPN导致的急性脑炎及ADEM和(或)GBS,除了两者发生时间接近、同时好转,以及没有其他明显的脑炎病因外,没有临床或辅助检查证据能够明确将肺炎衣原体感染与脑炎联系起来。2007年法国学者对253例脑炎病例进行了系统筛查,但未发现与肺炎衣原体相关的感染[19],然而1997年芬兰学者进行的另一项前瞻性研究中,对175例儿童急性脑炎病例进行研究,报告称有4名患者血清学特征与肺炎衣原体感染相符[20]。
3 讨论ADEM和GBS的诊断主要基于病史和神经系统体格检查,结合脑脊液和电生理检查结果,进行综合判断[1, 3]。本例患者病史特点: (1)青年女性, 急性起病; (2)发病前有反复发热,随后证实为CPN肺炎; (3)有颅脑受损的症状及体征, 如呕吐、视物重影、肢体无力、颈部强直,发展至昏迷、抽搐; (4)脑脊液检查提示明显蛋白细胞分离,且脑脊液多次病原学检查,包括细菌培养、tNGS、mNGS均为阴性; (5)脑脊髓MRI检查有脑实质受累; (6)脑电图和肌电图出现异常表面; (7)血清周围神经病抗体中抗GT1a抗体IgM强阳性。结合患者病史、查体及各项检查结果, 为ADEM和GBS重叠。中枢和周围神经系统联合脱髓鞘疾病(combined central and peripheral demyelination,CCPD)是一种罕见的神经障碍,为自身免疫介导的同时或相继发生的中枢神经系统和周围神经系统脱髓鞘疾病[21, 22]。CCPD的诊断需要满足以下标准[23] : (1)中枢神经受累的标准:存在颅内、脊髓或视神经MRI-T2WI高信号或视觉诱发电位异常; (2)周围神经受累的标准:神经传导速度检测提示正中神经、尺神经或胫神经至少2条神经存在神经传导延迟、传导阻滞、波形离散、F波异常等周围神经系统脱髓鞘的证据; (3)排除标准:除外直接感染性疾病、系统免疫性疾病、线粒体病、代谢、中毒、脑血管疾病、肿瘤及遗传疾病等所致的MRI-T2WI高信号改变。本例患者排除了其他疾病,符合CCPD诊断标准。CCPD多于感染或疫苗接种后发病,约65%的患者有前驱感染史[22, 24],约2/3的GBS患者在发病前6周内有前驱事件,以上呼吸道感染和腹泻多见,包括巨细胞病毒、寨卡病毒、新型冠状病毒以及肺炎支原体或其他病原体感染[3],本病例的特点是肺炎衣原体肺炎诊疗过程出现神经功能障碍并排除其他疾病,所以笔者考虑为肺炎衣原体相关性CCPD。
CPN是一类具有独特双相发育周期的专性胞内寄生菌,是成人和5岁以上儿童通过飞沫传播引起急慢性呼吸道传染病的常见病原体[25]。CPN感染的诊断依靠病原学检测,而病原学检测基于微生物学培养、血清学检测及分子学技术,由于CPN不能在体外存活,需进行接种培养,微生物学培养操作复杂且耗时[26],不适用于临床诊断。血清学检测方法在诊断CPN感染最为常用,其中微量免疫荧光可以检测IgG、IgM和IgA抗体,因此血清学分析现已成为该病的常规诊断方法,但CPN- IgM抗体出现较晚,阳性IgM结果可能在肺炎消退后才能被检测到,会导致CPN感染诊断困难[27]。PCR适合快速诊断,多重PCR采用多重引物,针对不同病原体核酸或耐药基因进行特异度扩增,可以同时检测同一样本中的中CPN和其他微生物,近年来兴起的mNGS方法对临床病原微生物的快速精确诊治具有较高的应用价值[26, 28]。该患者入院时咽拭子13项多重PCR(包括CPN)结果是阴性,在入ICU后进行肺泡灌洗液mNGS中检测出CPN序列数,随后的CPN- IgM抗体也提示阳性,证实CPN肺炎。近年来,越来越多的研究报告指出在慢性非呼吸系统疾病中,如常见的反应性关节炎、动脉粥样硬化、神经系统疾病(多发性硬化症、中风、阿尔茨海默病)中检测到CPN,被认为参与了这些疾病的发生发展[25]。少数报告指出CPN可能与急性播散性脑脊髓炎或吉兰-巴雷综合征有关,尤其是在年轻患者中,这些患者在接受抗生素和/或免疫抑制治疗后通常有较好的预后,这表明该微生物与这些疾病的强烈关联[15-18]。分子模拟以及针对髓鞘蛋白抗原的交叉反应性自身免疫反应被认为是GBS和ADEM的最常见发病机制[29-30]。另一种假说提出,一种抗体介导的感染后综合征可导致累及周围神经系统和中枢神经系统的连续临床谱系,表明致病病原体携带了周围和中枢髓鞘的共同抗原,正如在伴有抗GQ1b抗体的Fisher–Bickerstaff综合征中所见[31]。笔者假设肺炎衣原体感染引发了GBS和ADEM, 就本例的患者情况而言, CPN感染会生产抗体的常见抗原靶点,CPN感染可能与抗神经节苷脂阳性的吉兰-巴雷综合征有关,因此很有可能它也会引发同时出现GBS和ADEM(正如本例患者所表现的那样),但确切的机制仍不清楚。另外在我们的病例中,因呼吸系统症状和神经系统症状出现的时间间隔较短,出现明显脑膜刺激征(颈部强直),脑脊液检查提示细胞数轻度增高,相应的抗生素治疗后体温得到控制,在诊疗过程中也一度考虑是否为CPN导致的脑膜脑炎,但是送检的脑脊液细菌培养和tNGS、mNGS(DNA+RNA)均为阴性,经免疫球蛋白及激素等药物治疗后患者神经系统症状逐渐改善。复习文献发现报道了11例与CPN有关的急性脑炎病例,但这些病例均通过检查血清和或脑脊液CPN相关抗体结合临床表现诊断为CPN导致的脑炎和脑膜炎,但CPN在急性中枢神经系统炎症中的病理机制尚不明确[13],故笔者认为颅内CPN感染病原学依据是不充分的,可能高估了CPN致脑膜脑炎的发病率。同理,在我们的患者中观察到了感染CPN后出现进行加重的神经功能障碍,在复习的文献中病例,一位CPN相关多相播散性脑脊髓炎(MDEM)6岁儿童,CPN感染诱导复发时检查出血清抗MOG IgG抗体阳性; 另一位患有ADEM和GBS重叠和CPN感染的60岁男性,也发现抗MOG-IgG抗体和抗硫酸酯IgG抗体阳性[18]; 而本病例中CPN感染后出现GBS和ADEM重叠的年轻女性中发现了抗神经节苷脂GT1a抗体IgM强阳性。在这些案例中,作者认为这些神经功能障碍可能是由CPN引起的,并且这种关联可能被低估了。
抗神经节苷脂抗体阳性有助于GBS诊断,抗GM1、GD1a抗体阳性常见于急性运动轴索性神经病和急性运动感觉轴索性神经病; 截瘫型可有抗GM1或GD1b抗体阳性,而急性炎性脱髓鞘性多发神经根神经病通常无特异度抗体阳性; 抗GQ1b、GT1a抗体阳性常见于Miller-Fisher综合征和Bickerstaff脑干脑炎,也可见于咽颈臂型[33]。因为GT1a更多表达于舌咽神经和迷走神经,抗GT1a抗体更多见于咽颈臂无力,在本病例中患者出现颈部强直,神志、肌力改善后仍存在咽、颈肌肉无力,停呼吸机后仍长时间因吞咽困难、气道保护能力弱而无法拔除气管插管与此咽颈臂变异型临床表现相符的。典型GBS患者血清中的抗神经节苷脂抗体阳性率较低,抗神经节苷脂抗体检测价值有限[3]。故在进行抗神经节苷脂抗体检测要求结合临床具体情况,不应盲目进行相关抗体检测。CCPD是一种罕见的自身免疫性疾病,目前尚无针对该病治疗的随机临床试验,本例在治疗CPN的情况下,同时静脉注射免疫球蛋白和激素病情明显改善,这和相关报道是相符[23]。然而,糖皮质激素治疗GBS、ADEM尚缺乏循证医学证据的支持[1, 3],Korman等[5]与Wong等[17]报道的病例因继发包括念珠菌血症的院内感染,不排除与激素冲击治疗有关,我们的患者激素的使用剂量及时间与既往报道相比剂量小、时间短但患者预后却是良好的,所以激素的作用可能存在争议的。
本研究报告了一例罕见的成人患者同时患有GBS和ADEM的病例,该患者在接受抗感染和免疫抑制治疗后预后良好。尽管此前已有数例CCPD的病例被报道,但据我们所知,这是首例抗GT1a抗体阳性且与CPN相关的并发GBS和ADEM的病例。本病例提示CPN感染后并发CCPD虽属罕见,但其实际发生率可能被低估, 因此,临床医生在诊治急性感染后继发神经系统异常的患者时,需警惕自身免疫性神经系统疾病的可能,同样,对于以神经系统症状为主诉就诊的患者,也应常规询问并检测其近期感染史,这有助于明确感染与神经系统症状之间的关联。未来仍需进一步研究以阐明此类疾病的发病机制及其潜在关联。
利益冲突 所有作者声明无利益冲突
作者贡献声明 曾海文:数据收集、数据分析、论文撰写; 陈巧莉苏婉婷:数据收集、数据分析; 林天来:论文审阅、指导
| [1] | Singh NK, Gupta V, Mishra SK. Acute disseminated encephalomyelitis-a monophonic illness[J]. Int Rev Neurobiol, 2025: 180-499. DOI:10.1016/bs.irn.2025.04.004 |
| [2] | 黄磊, 苏磊, 田德财, 等. 我国主要神经系统自身免疫性疾病的发病率[J]. 中华神经科杂志, 2022, 55(4): 372-378. DOI:10.3760/cma.j.cn113694-20211130-00849 |
| [3] | 中华医学会神经病学分会, 中华医学会神经病学分会周围神经病协作组. 中国吉兰-巴雷综合征诊治指南2024[J]. 中华神经科杂志, 2024, 57(9): 936-944. DOI:10.3760/cma.j.cn113694-20240220-00099 |
| [4] | Socan M, Beovic B, Kese D. Chlamydia pneumonia and meningoencephalitis[J]. N Engl J Med, 1994, 331(6): 406. DOI:10.1056/nejm199408113310618 |
| [5] | Korman TM, Turnidge JD, Grayson ML. Neurological complications of chlamydial infections: case report and review[J]. Clin Infect Dis, 1997, 25(4): 847-851. DOI:10.1086/515536 |
| [6] | Anton E, Otegui A, Alonso A. Meningoencephalitis and Chlamydia pneumoniae infection[J]. Euro J Neurology, 2000, 7(5): 586. DOI:10.1046/j.1468-1331.2000.t01-1-00129.x |
| [7] | Guglielminotti J, Lellouche N, Maury E, et al. Severe meningoencephalitis: an unusual manifestation of Chlamydia pneumoniae infection[J]. Clin Infect Dis, 2000, 30(1): 209-210. DOI:10.1086/313633 |
| [8] | Airas L, Kotilainen P, Vainionpää R, et al. Encephalitis associated withChlamydia pneumoniae[J]. Neurology, 2001, 56(12): 1778-1779. DOI:10.1212/wnl.56.12.1778 |
| [9] | Boschin C, Kreisler A, Legout L, et al. Can meningoencephalitis be caused by Chlamydiae pneumoniae?[J]. Rev Neurol (Paris), 2005, 161(10): 979-83. DOI:10.1016/s0035-3787(05)85164-1 |
| [10] | Xavier M, Correa B, Coromina M, et al. Sudden psychotic episode probably due to meningoencephalitis and Chlamydia pneumoniaeacute infection[J]. Clin Pract Epidemiol Ment Health, 2005, 1(1): 15. DOI:10.1186/1745-0179-1-15 |
| [11] | Cunha BA, Pherez FM.. C. pneumoniae community-acquired pneumonia (CAP) in mimicking Mycoplasma pneumoniae meningoencephalitis complicated by asthma[J]. Heart Lung, 2009, 38(6): 530-533. DOI:10.1016/j.hrtlng.2009.01.003 |
| [12] | Yagi K, Kano G, Shibata M, et al. Chlamydia pneumoniae infection-related hemophagocytic lymphohistiocytosis and acute encephalitis and poliomyelitis-like flaccid paralysis[J]. Pediatr Blood Cancer, 2011, 56(5): 853-855. DOI:10.1002/pbc.22889 |
| [13] | Elargoubi A, Verhoeven PO, Grattard F, et al. Acute encephalitis associated to a respiratory infection due to Chlamydophila pneumoniae[J]. Médecine Mal Infect, 2013, 43(8): 345-349. DOI:10.1016/j.medmal.2013.06.015 |
| [14] | 李海涛, 戴建军, 邱方, 等. 长期服用强的松致肺炎衣原体脑炎1例[J]. 中国综合临床, 2004, 20(1): 66. DOI:10.3760/cma.j.issn.1008-6315.2004.01.052 |
| [15] | Heick A, Skriver E. Chlamydia pneumoniae-associated ADEM[J]. Euro J Neurology, 2000, 7(4): 435-438. DOI:10.1046/j.1468-1331.2000.00090.x |
| [16] | Azumagawa K, Nomura S, Shigeri Y, et al. Post-vaccination MDEM associated with MOG antibody in a subclinical Chlamydia infected boy[J]. Brain Dev, 2016, 38(7): 690-693. DOI:10.1016/j.braindev.2016.02.004 |
| [17] | Wong CK, Ng CF, Tan HJ, el al. Bickerstaff brainstem encephalitis with Guillain-Barré syndrome overlap following chlamydia infection[J]. BMJ Case Rep, 2021, 14(5): e242090. DOI:10.1136/bcr-2021-242090 |
| [18] | Papantoniou M, Panagopoulos G. Concurrent acute sensorimotor axonal neuropathy and disseminated encephalitis associated with Chlamydia pneumoniae in an adult patient with anti-MOG and anti-sulfatide antibodies: a case report[J]. Ther Adv Neurol Disord, 2024, 17: 17562864241237850. DOI:10.1177/17562864241237850 |
| [19] | Mailles A, Stahl JP. Infectious encephalitis in France in 2007:a national prospective study[J]. Clin Infect Dis, 2009, 49(12): 1838-1847. DOI:10.1086/648419 |
| [20] | Koskiniemi M, Korppi M, Mustonen K, et al. Epidemiology of encephalitis in children. A prospective multicentre study[J]. Eur J Pediatr, 1997, 156(7): 541-545. DOI:10.1007/s004310050658 |
| [21] | Bhagavati S. Autoimmune disorders of the nervous system: pathophysiology, clinical features, and therapy[J]. Front Neurol, 2021, 12: 664664. DOI:10.3389/fneur.2021.664664 |
| [22] | Andrusiów S, Dziadkowiak E, Koszewicz M. Clinical and electrophysiological features of adult patients with combined central and peripheral demyelination- a systematic review[J]. Front Immunol, 2025, 16: 1572507. DOI:10.3389/fimmu.2025.1572507 |
| [23] | 张丽丽, 胡梦含, 王敏, 等. 水痘-带状疱疹病毒感染后中枢和周围神经联合脱髓鞘疾病1例[J]. 中华神经科杂志, 2023, 56(4): 434-437. DOI:10.3760/cma.j.cn113694-20220816-00622 |
| [24] | Papadopoulou M, Tzanetakos D, Moschovos C, et al. Combined central and peripheral demyelination (CCPD) associated with MOG antibodies: report of four new cases and narrative review of the literature[J]. J Clin Med, 2024, 13(12): 3604. DOI:10.3390/jcm13123604 |
| [25] | Ma YC, Sun JL, Che GH, et al. Systematic infection of Chlamydia Pneumoniae[J]. Clin Lab, 2022, 68(8). DOI:10.7754/clin.lab.2021.210908 |
| [26] | Tagini F, Puolakkainen M, Greub G. From coughs to complications: the story of Chlamydia pneumoniae: This article is part of the JMM Profiles collection[J]. J Med Microbiol, 2025, 74(4): 002006. DOI:10.1099/jmm.0.002006 |
| [27] | Miyashita N. Atypical pneumonia: Pathophysiology, diagnosis, and treatment[J]. Respir Investig, 2022, 60(1): 56-67. DOI:10.1016/j.resinv.2021.09.009 |
| [28] | 张玉林, 曹彬. 呼吸道感染的病原学检测及其临床应用[J]. 中华结核和呼吸杂志, 2024, 47(5): 497-500. DOI:10.3760/cma.j.cn112147-20240227-00109 |
| [29] | Garg RK. Acute disseminated encephalomyelitis[J]. Postgrad Med J, 2003, 79(927): 11-17. DOI:10.1136/pmj.79.927.11 |
| [30] | van Doorn PA, Ruts L, Jacobs BC. Clinical features, pathogenesis, and treatment of Guillain-Barré syndrome[J]. Lancet Neurol, 2008, 7(10): 939-950. DOI:10.1016/s1474-4422(08)70215-1 |
| [31] | Yuki N. Fisher syndrome and Bickerstaff brainstem encephalitis (Fisher-Bickerstaff syndrome)[J]. J Neuroimmunol, 2009, 215(1/2): 1-9. DOI:10.1016/j.jneuroim.2009.05.020 |
| [32] | Liberatore G, De Lorenzo A, Giannotta C, et al. Frequency and clinical correlates of anti-nerveantibodies in a large population of CIDP patients included in the Italian database[J]. Neurol Sci, 2022, Jun; 43(6): 3939-3947. DOI:10.1007/s10072-021-05811-0 |
 2026, Vol. 35
2026, Vol. 35