2. 昆明理工大学医学部, 云南省第一人民医院医务处, 昆明 650500
脓毒症是由病原体感染引发的宿主免疫系统失调性疾病,可导致器官功能障碍甚至死亡,是全球性的重大健康问题,也是重症监护室死亡的主要原因之一。据近期全球分析估计,2017年脓毒症人数占全球总死亡人数的19.7%[1]。中国脓毒症病死率同样居高不下[2],其治疗仍主要依赖抗生素和器官支持疗法[3],且近年来治疗方案未有显著变革。现有研究发现,某些细菌来源的EVs在脓毒症进程中能抑制全身炎症、促进组织修复[4],有望成为治疗脓毒症的新靶点。
1 脓毒症与肠道菌群肠道菌群是定植于胃肠道的细菌,通常与人体共生或互利,在宿主营养代谢、维持肠道黏膜屏障结构完整性、免疫调节及抵御病原体等方面发挥多种特定功能[8]。肠道菌群的代谢产物,如短链脂肪酸、胆汁酸、色氨酸等,对维持人体正常生理功能具有重要作用[9]。脓毒症发生时,炎症因子被大量激活,肠道屏障功能严重受损。此时,即使在正常生理条件下有益的细菌,也可能在肠道屏障破坏后发生易位,引发炎症反应和器官损伤,从而加剧脓毒症进程[5]。人体肠道菌群以拟杆菌门和厚壁菌门为主,而脓毒症患者的肠道菌群组成与健康人显著不同[10],拟杆菌增加,厚壁菌门下降,二者的比例变化被视为菌群失调的标志[11]。肠道菌群参与形成肠道屏障的微生物屏障,对于防止潜在有害物质和病原体侵入内环境至关重要[12]。菌群失调可导致肠道通透性增加(即“肠漏”现象),引发一系列不良后果,如微生态失衡、微生物易位和异常免疫反应等,最终形成疾病的恶性循环[13]。值得注意的是,肠道菌群均可释放EVs,这些源自不同细菌的EVs构成了一个复杂“囊泡通讯网络”。细菌可以将信号分子(包括蛋白质、脂质和核酸)包装在EVs中,以避免快速降解和逃避免疫监视等,从而介导局部和长距离细胞间通讯[6]。由此可知,肠道菌群的EVs在菌群-宿主互作中扮演着不可或缺的角色,参与调控脓毒症发生发展。
2 EVs的特性和功能细胞外囊泡(EVs)是细胞在生理或病理条件下释放的一类异质性膜包被纳米颗粒。细胞可将蛋白质、脂质、代谢物、DNA、RNA(如microRNA, mRNA, lncRNA)等多种信号分子包装入EVs中参与信息传递,并诱导受体细胞改变其生物行为,包括基因表达、增殖和凋亡等过程[14]。相比病毒、真菌等微生物,细菌感染在脓毒症的病因中占主导地位[15]。细菌释放含有其母细胞成分的EVs,常称为细菌细胞外囊泡(bacterial extracellular vesicles, BEVs),根据母体细菌的细胞壁差异及其囊泡的生物发生途径,BEVs主要包括两大类:革兰氏阴性菌产生的经典外膜囊泡(outer membrane vesicles, OMVs),以及革兰氏阳性菌产生的细胞质膜囊泡(membrane vesicles,CMVs)。OMVs和CMVs分别通过外膜出芽及质膜出芽形成,自然包裹蛋白质、核酸、毒素、酶、信号分子等,包裹在其中的物质受到膜结构的保护,不易被蛋白酶降解,适合在消化道等恶劣环境中递送生物信号。OMVs能穿透肠道屏障层,甚至进入血液循环,调节局部与系统的生物效应。BEVs可通过内吞作用、脂筏介导的内化或直接膜融合等方式进入宿主细胞,携带病原相关分子模式(PAMPs)激活或抑制宿主免疫反应。基于上述特征,BEVs被认为是细菌零型分泌系统[16-17]。肠道菌群来源的EVs在脓毒症病理进程中呈现出显著的双重调控作用[18],即病原菌来源EVs可包装毒力因子、PAMPs、甚至抗生素耐药基因驱动脓毒症恶化,而益生菌来源的EVs则能递送保护性内容物发挥重要的保护效应[19]。在细菌感染所致的脓毒症中,BEVs发挥着极为重要的作用,其双重性使肠道菌群来源的EVs成为理解脓毒症病理生理机制和开发治疗手段的重要窗口。
3 EVs在脓毒症与道菌群互作中的核心机制 3.1 病原菌来源EVs的致病机制肠道微生物是人体BEVs的主要生产者。宿主免疫系统的模式识别受体(PRRs)识别BEVs的PAMPs后,会触发显著的促炎反应。这可能导致死亡或濒死细胞释放损伤相关分子模式,进一步促进先天免疫细胞活化和炎性细胞因子(如TNF-α和IL-1β)的释放。病原菌BEVs的具体致病机制包括:
(1)激活炎症信号通路与细胞焦亡:BEVs激活Toll样受体(TLRs)是触发脓毒症、导致多器官衰竭、休克乃至死亡的关键环节[20]。TLR4主要识别OMVs表面的脂多糖(LPS),激活MyD88依赖通路, 进而通过NF-κB诱导炎症因子如TNF-α、IL-6、INF-β等的表达。TLR2识别CMVs表面的脂磷壁酸(lipoteichoic acid, LTA),以及OMVs和CMVs的脂蛋白,激活下游通路诱导炎症因子分泌。若BEVs携带鞭毛素,则可被TLR5识别,NOD1/NOD2识别进入胞质的BEVs的肽聚糖片段,激活NF-κB和MAPK通路[21]。此外,OMVs被宿主细胞内化后,其携带的成分(如促凋亡蛋白Bax/Bak)可导致线粒体损伤并释放DAMPs(如mtDNA、ROS),进而激活NLRP3炎症小体,NLRP3激活导致caspase-1介导的IL-1β和IL-18成熟与分泌,驱动强烈的炎症反应[28]。
(2)破坏肠道屏障功能:BEVs可破坏肠上皮细间的紧密连接。例如,黏附侵袭性大肠埃希菌的OMVs可下调紧密连接蛋白(如occludin、ZO-1)的mRNA和蛋白表达,同时上调促屏障破坏蛋白(如claudin-2)的表达,导致肠道通透性增加和菌群易位[22]。幽门螺杆菌EVs中的毒力蛋白CagA也能促进紧密连接的破坏[23]。
(3)促凝血与弥散性血管内凝血(disseminated intravascular coagulation,DIC):DIC是脓毒症的严重并发症,可促进多器官功能障碍和死亡。BEVs内的脂多糖(LPS)可激活Caspase-11(人源为Caspase-4/5),活化的Caspase-11切割Gasdermin D(GSDMD)形成细胞膜孔道,导致细胞焦亡(pyroptosis),并释放组织因子(TF)、组蛋白等强促凝物质,最终诱发DIC[24]。
(4)介导抗生素耐药性传播:OMVs是细菌抗生素耐药基因(ARGs)传播的重要载体[25]。例如,源自碳青霉烯类耐药肺炎克雷伯菌(CRKP)的OMVs可携带blaNDM-1基因,并将耐药性传递给其他肺炎克雷伯菌菌株[26]。
3.2 肠道益生菌来源EVs的抑炎与保护作用(1)调节先天免疫:与病原菌EVs的致病性不同,益生菌细胞外囊泡(probiotic extracellular vesicles, pEVs)可通过传递免疫调节信号维持宿主稳态并抵御疾病[27]。如乳酸杆菌、双歧杆菌的EVs中某些活性成分(如脂蛋白)可作为TLR2的配体。TLR2激活宿主免疫细胞(如巨噬细胞、树突状细胞)后导致促炎因子(IL-6、TNF-α)和抗炎因子(IL-10、TGF-β)的平衡表达,形成一种“免疫微调”效应。这种双向调节既能增强先天免疫防御病原体,又通过IL-10等维持免疫耐受,防止过度炎症反应[28]。此外,Gong等人证明,pEVs能抑制IKK复合体的磷酸化进而抑制NF-κB通路,并激活STAT3/STAT6等通路促进巨噬细胞向抗炎的M2型极化[29]。
(2)减轻肠-器官轴炎症损伤:肠道微生态可影响各器官功能(如肠-肺轴、肠-脑轴、肠-肝轴等)[30]。脓毒症常伴随着多器官功能障碍,肠道EVs被认为是远端器官之间通讯的信号,通过EVs递送保护因子能减轻脓毒症相关的远端器官损伤[31]。例如,物乳植杆菌衍生的EVs(LpEVs)递送靶向抑制铁死亡关键基因Acsl4的cbn-let-7和NF-κB/NLRP3通路,通过抗铁死植亡和抗炎减轻肺损伤[32]肠道益生菌鲁伊托氏乳酸杆菌衍生的EVs抑制MAPK和NF-κB通路调节小胶质细胞极化,改善血脑屏障功能并减轻神经炎症[33]。此外,AKK衍生的EVs通过阻断NLRP3寡聚化、增强紧密连接,减少内毒素入肝、抑制巨噬细胞中的TLR4/NF-κB通路等减轻肝脏炎症[34]。还有研究表明,EVs可通过递送lncRNA有效减轻脓毒症诱导的器官损伤[35]。
(3)调节肠道炎症与肠道菌群:益生菌衍生的EVs可作为“后生元(postbiotics)”[36],发挥抗菌、免疫调节、抗氧化和抗增殖等多重活性,通过调节肠道微环境,降低脓毒症发生风险并改善脓毒症患者预后[37]。另外,多种益生菌衍生的EVs能抑制肠道炎症,如副干酪乳杆菌(lactobacillus paracasei)的EVs则通过特异度靶向并增强IRE1α-XBP1内质网应激通路,诱导TRAF2降解,进而抑制NF-κB信号通路来减轻肠道炎症[38]。更重要的是,益生菌EVs能有效保护肠道屏障完整性,甚至影响肠道菌群组成,Hua等证明,罗斯氏菌能增加肠道双歧杆菌属、柯林斯菌属和安德克氏菌属[39]。
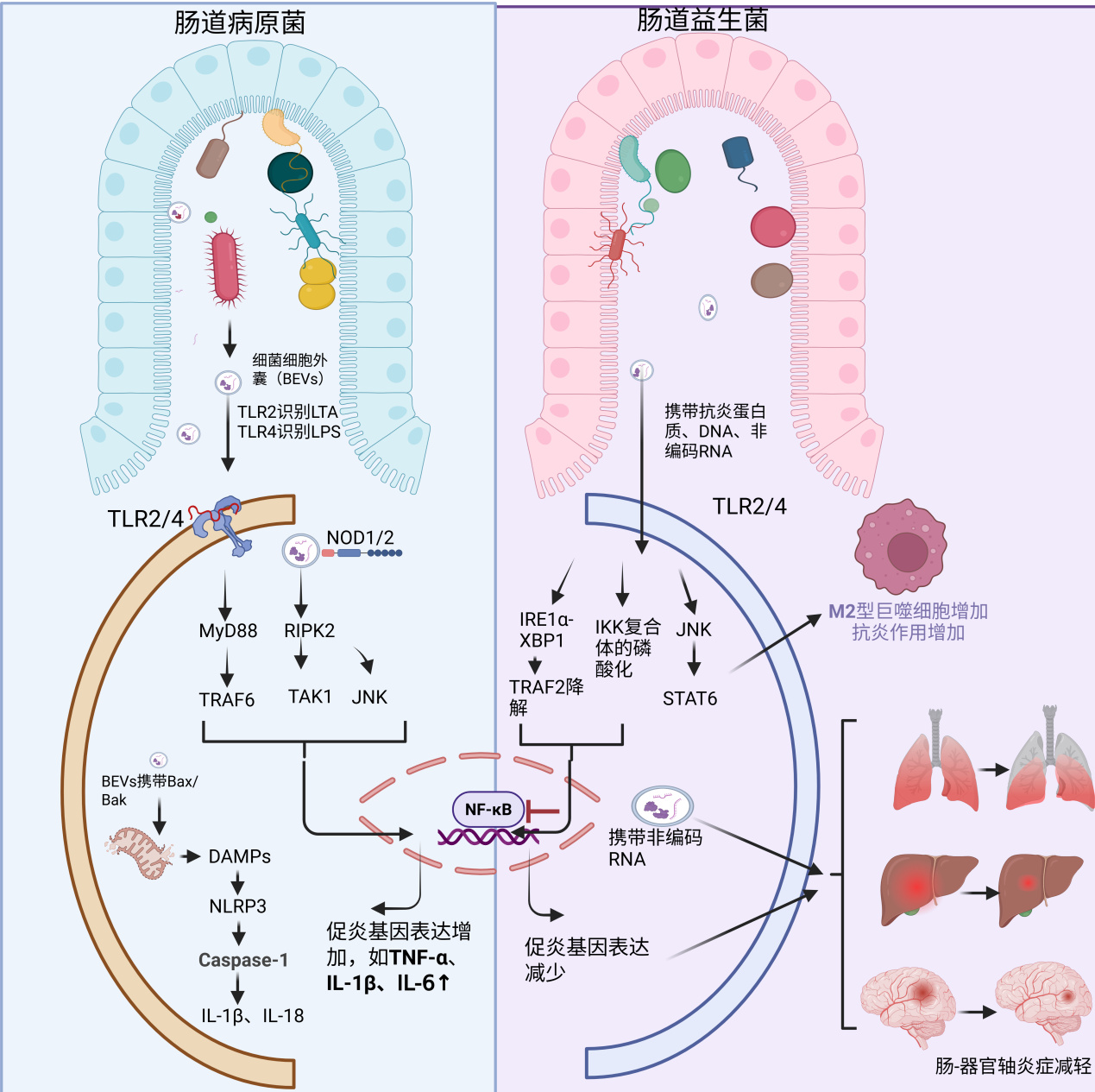
4 肠道菌群衍生的EVs在脓毒症治疗中的潜在应用肠道EVs在脓毒症治疗中具有广阔前景,细菌产生的EVs内容物有所不同,且具有选择性靶向各种组织或器官的能力,可使所负载的活性物质靶向释放,已成为疫苗、生物标志物、免疫治疗剂和纳米药物递送系统。见图 1。
|
| 图 1 肠道病原菌与益生菌EVs在脓毒症中的作用对比 |
|
|
(1)疫苗开发:OMVs有多种病原体相关抗原, 同时含有跨膜和膜锚定蛋白,可增强内吞作用以促进其内容物递送。凭借其高稳定性、良好的组织渗透性,成为了疫苗开发的宝贵资源[40]。伤寒沙门氏菌、痢疾杆菌、大肠杆菌等衍生的OMVs正在用于开发疫苗[41]。基于肠道菌群细胞外囊泡的疫苗可用,可帮助对抗疾病和满足医疗需求。
(2)诊断生物标志物:脓毒症患者血清中的外泌体内容物会发生显著改变,可作为脓毒症诊断标物[42-43]。例如,在血清外泌体差异表达蛋白(DEPs)中,过氧化物还原蛋白-1(PRDX1)仅存在于脓毒症患者中,而在健康个体中未检出[44]。
(3)抗菌与抗病毒载体:抗生素是脓毒症治疗基石,而革兰氏阴性菌耐药性是最大威胁。OMVs具有跨细菌细胞包膜递送功能性物质的独特能力,使其有潜力作为天然的抗菌递送载体。在抗病毒方面,克雷伯菌、大肠杆菌和沙门氏菌的MVs可通过TLR4-TRIF信号通路诱导巨噬细胞产生抗病毒免疫,减少病毒在巨噬细胞、肺泡上皮细胞及肺组织中的复制,对细菌-病毒混合感染的结局具有重要影响[45]。
(4)工程化药物递送平台:通过基因工程、膜融合、化学修饰或物理修饰等方法,可将靶向分子引入EVs,赋予其在疾病管理中更广泛和精准的应用潜力[46]。例如,将AKK用修饰后的外泌体包封,可保护AKK免受胃酸、胆汁盐和消化酶的破坏,显著增强其在胃肠道的定植潜力[47]。AKK已被证明能有效减缓肠道炎症,又如,将抗肿瘤药物阿霉素装载入拉氏链球菌EVs中,可成功将其递送至人体细胞内[48]。长远来看,EVs研究不仅将深化我们对脓毒症发病机制的理解,也可能为其他感染性和炎症性疾病的治疗提供全新范式。
5 挑战与展望EVs相关研究进一步强化了脓毒症作为一种高度异质性疾病的观点。未来的疾病分类系统可能需要整合EVs的特征信息(如来源细胞、特异度分子标记物等),以实现更精准的疾病分型和个体化治疗。此外,EVs介导的菌群-宿主互作机制,凸显了调节肠道微生态平衡在脓毒症治疗中的核心重要性。靶向肠道菌群EVs的策略(如补充益生菌EVs、中和致病菌EVs)有望成为脓毒症综合治疗的新组分。然而,当前EVs研究与应用仍面临诸多挑战。EVs大规模分离纯化、标准化储存、有效剂量确定及功能评估方法的标准化是亟待解决的关键难题[49]。在EVs大规模生产过程中,同时获得高纯度和高产率仍具挑战性。迫切需要推进EVs生产流程的标准化和基础机制研究,以合理设计治疗策略并准确预测潜在风险。通过持续的多学科协作努力,EVs有望被转化为强大的医学工具,最终惠及广大脓毒症患者。
利益冲突 所有作者声明无利益冲突
| [1] | Rudd KE, Johnson SC, Agesa KM, et al. Global, regional, and national sepsis incidence and mortality, 1990-2017:analysis for the Global Burden of Disease Study[J]. Lancet, 2020, 395(10219): 200-211. DOI:10.1016/s0140-6736(19)32989-7 |
| [2] | 刘峰宇, 李想, 孙同文. 中国脓毒症十年研究回顾及展望[J]. 中华急诊医学杂志, 2023, 32(10): 1291-1295. DOI:10.3760/cma.j.issn.1671-0282.2023.10.002 |
| [3] | Evans L, Rhodes A, Alhazzani W, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021[J]. Intensive Care Med, 2021, 47(11): 1181-1247. DOI:10.1007/s00134-021-06506-y |
| [4] | You BS, Yang Y, Wei J, et al. Pathogenic and therapeutic roles of extracellular vesicles in sepsis[J]. Front Immunol, 2025, 16: 1535427. DOI:10.3389/fimmu.2025.1535427 |
| [5] | 王国鑫, 万红阳, 闵婕, 等. 肠道菌群在感染性胰腺坏死中的作用[J]. 中华急诊医学杂志, 2025, 34(6): 902-906. DOI:10.3760/cma.j.issn.1671-0282.2025.06.030 |
| [6] | Jeppesen DK, Zhang Q, Franklin JL, et al. Extracellular vesicles and nanoparticles: emerging complexities[J]. Trends Cell Biol, 2023, 33(8): 667-681. DOI:10.1016/j.tcb.2023.01.002 |
| [7] | 赵奕琳, 刘田恬, 王春霞. 外泌体参与脓毒症发生发展及临床诊治方面的研究进展[J]. 中华危重病急救医学, 2024, 36(2): 221-224. DOI:10.3760/cma.j.cn121430-20230809-00601 |
| [8] | Meawad M, Singh D, Deng A, et al. Functional archetypes in the human gut microbiome reveal metabolic diversity, stability, and influence disease-associated signatures[J]. Microbiome, 2025, 13(1): 241. DOI:10.1186/s40168-025-02240-5 |
| [9] | 莫春燕, 娄熙冉, 陈国兵. 肠道菌群代谢产物在脓毒症中的研究进展[J]. 中国急救医学, 2023, 43(3): 239-242. DOI:10.3969/j.issn.1002-1949.2023.03.014 |
| [10] | Lou XR, Xue JF, Shao RF, et al. Fecal microbiota transplantation and short-chain fatty acids reduce sepsis mortality by remodeling antibiotic-induced gut microbiota disturbances[J]. Front Immunol, 2023, 13: 1063543. DOI:10.3389/fimmu.2022.1063543 |
| [11] | Karačić A, Renko I, Krznarić Ž, et al. The association between the firmicutes/bacteroidetes ratio and body mass among European population with the highest proportion of adults with obesity: an observational follow-up study from Croatia[J]. Biomedicines, 2024, 12(10): 2263. DOI:10.3390/biomedicines12102263 |
| [12] | Di Vincenzo F, Del Gaudio A, Petito V, et al. Gut microbiota, intestinal permeability, and systemic inflammation: a narrative review[J]. Intern Emerg Med, 2024, 19(2): 275-293. DOI:10.1007/s11739-023-03374-w |
| [13] | Mishra S, Jain S, Agadzi B, et al. A cascade of microbiota-leaky gut-inflammation- is it a key player in metabolic disorders?[J]. Curr Obes Rep, 2025, 14(1): 32. DOI:10.1007/s13679-025-00624-0 |
| [14] | Fusco C, De Rosa G, Spatocco I, et al. Extracellular vesicles as human therapeutics: a scoping review of the literature[J]. J Extracell Vesicles, 2024, 13(5): e12433. DOI:10.1002/jev2.12433 |
| [15] | S Alharbi Azzah, Sanyi Raghad Hassan, I Azhar Esam. Bacteria and host: what does this mean for sepsis bottleneck?[J]. World J Emerg MED, 2025, 16(1): 10-17. DOI:10.5847/wjem.j.1920-8642.2025.001 |
| [16] | Gong X, Liu S, Xia BZ, et al. Oral delivery of therapeutic proteins by engineered bacterial type zero secretion system[J]. Nat Commun, 2025, 16: 1862. DOI:10.1038/s41467-025-57153-6 |
| [17] | Xiao M, Li GD, Yang HF. Microbe-host interactions: structure and functions of Gram-negative bacterial membrane vesicles[J]. Front Microbiol, 2023, 14: 1225513. DOI:10.3389/fmicb.2023.1225513 |
| [18] | Tarashi S, Zamani MS, Omrani MD, et al. Commensal and pathogenic bacterial-derived extracellular vesicles in host-bacterial and interbacterial dialogues: two sides of the same coin[J]. J Immunol Res, 2022, 2022: 8092170. DOI:10.1155/2022/8092170 |
| [19] | Saleh NA, Gagea MA, Vitija X, et al. Harnessing extracellular vesicles for stabilized and functional IL-10 delivery in macrophage immunomodulation[J]. bio Rxiv, 2025: 2025. DOI:10.1101/2025.01.14.633016 |
| [20] | Effah CY, Ding XF, Drokow EK, et al. Bacteria-derived extracellular vesicles: endogenous roles, therapeutic potentials and their biomimetics for the treatment and prevention of sepsis[J]. Front Immunol, 2024, 15: 1296061. DOI:10.3389/fimmu.2024.1296061 |
| [21] | Toyofuku M, Schild S, Kaparakis-Liaskos M, et al. Composition and functions of bacterial membrane vesicles[J]. Nat Rev Microbiol, 2023, 21(7): 415-430. DOI:10.1038/s41579-023-00875-5 |
| [22] | Nadalian B, Nadalian B, Zali MR, et al. Outer membrane vesicles derived from adherent-invasive Escherichia coli induce inflammatory response and alter the gene expression of junction-associated proteins in human intestinal epithelial cells[J]. Can J Infect Dis Med Microbiol, 2024, 2024: 2701675. DOI:10.1155/2024/2701675 |
| [23] | González MF, Díaz P, Sandoval-Bórquez A, et al. Helicobacter pylori outer membrane vesicles and extracellular vesicles from Helicobacter pylori-infected cells in gastric disease development[J]. Int J Mol Sci, 2021, 22(9): 4823. DOI:10.3390/ijms22094823 |
| [24] | Peng Y, Gao M, Liu YK, et al. Bacterial outer membrane vesicles induce disseminated intravascular coagulation through the caspase-11-gasdermin D pathway[J]. Thromb Res, 2020, 196: 159-166. DOI:10.1016/j.thromres.2020.08.013 |
| [25] | Zhao MY, He M, Lin XL, et al. Identification of outer membrane vesicles as a new vehicle mediating antibiotic resistance gene transfer inCampylobacter[J]. J Extracell Vesicles, 2025, 14(11): e70195. DOI:10.1002/jev2.70195 |
| [26] | Tang B, Yang AW, Liu PL, et al. Outer membrane vesicles TransmittingblaNDM-1Mediate the emergence of carbapenem-resistant hypervirulent Klebsiella pneumoniae[J]. Antimicrob Agents Chemother, 2023, 67(5): e01444-e01422. DOI:10.1128/aac.01444-22 |
| [27] | Schmid AM, Razim A, Wysmołek M, et al. Extracellular vesicles of the probiotic bacteria E. coli O83 activate innate immunity and prevent allergy in mice[J]. Cell Commun Signal, 2023, 21(1): 297. DOI:10.1186/s12964-023-01329-4 |
| [28] | Morishita M, Sagayama R, Yamawaki Y, et al. Activation of host immune cells by probiotic-derived extracellular vesicles via TLR2-mediated signaling pathways[J]. Biol Pharm Bull, 2022, 45(3): 354-359. DOI:10.1248/bpb.b21-00924 |
| [29] | Gong S, Zeng RX, Liu L, et al. Extracellular vesicles from a novel Lactiplantibacillus plantarum strain suppress inflammation and promote M2 macrophage polarization[J]. Front Immunol, 2024, 15: 1459213. DOI:10.3389/fimmu.2024.1459213 |
| [30] | Tang XY, Peng XC. The gut microbiota-polyphenol interplay and its role in gut-organ axes: From mechanisms to functional outcomes[J]. Trends Food Sci Technol, 2025, 163: 105192. DOI:10.1016/j.tifs.2025.105192 |
| [31] | Zhang M, Xie JG, Zhang PY, et al. Bidirectional regulatory roles in the immune modulation, organ dysfunction, and therapy of sepsis[J]. Int J Nanomediline, 2025, 20: 13527-13541. DOI:10.2147/ijn.s542937 |
| [32] | Zhao Q, Lai JB, Jiang Y, et al. Lactiplantibacillus plantarum-derived extracellular vesicles alleviate acute lung injury by inhibiting ferroptosis of macrophages[J]. J Nanobiotechnology, 2025, 23(1): 307. DOI:10.1186/s12951-025-03405-y |
| [33] | Sun MD, Ma JH, Zhang G, et al. Brain targeting bacterial extracellular vesicles enhance ischemic stroke therapy via efficient ROS elimination and suppression of immune infiltration[J]. ACS Nano, 2025, 19(16): 15491-15508. DOI:10.1021/acsnano.4c16161 |
| [34] | Raftar SKA, Ashrafian F, Abdollahiyan S, et al. The anti-inflammatory effects of Akkermansia muciniphila and its derivates in HFD/CCL4-induced murine model of liver injury[J]. Sci Rep, 2022, 12: 2453. DOI:10.1038/s41598-022-06414-1 |
| [35] | Ma WT, Zhang WH, Cui B, et al. Functional delivery of lncRNA TUG1 by endothelial progenitor cells derived extracellular vesicles confers anti-inflammatory macrophage polarization in sepsis via impairing miR-9-5p-targeted SIRT1 inhibition[J]. Cell Death Dis, 2021, 12(11): 1056. DOI:10.1038/s41419-021-04117-5 |
| [36] | Zhang XM, Wang Y, E Q, et al. The biological activity and potential of probiotics-derived extracellular vesicles as postbiotics in modulating microbiota-host communication[J]. J Nanobiotechnology, 2025, 23(1): 349. DOI:10.1186/s12951-025-03435-6 |
| [37] | Lou XR, Xue JF, Shao RF, et al. Postbiotics as potential new therapeutic agents for sepsis[J]. Burns Trauma, 2023, 11: tkad022. DOI:10.1093/burnst/tkad022 |
| [38] | Choi JH, Moon CM, Shin TS, et al. Lactobacillus paracasei-derived extracellular vesicles attenuate the intestinal inflammatory response by augmenting the endoplasmic reticulum stress pathway[J]. Exp Mol Med, 2020, 52(3): 423-437. DOI:10.1038/s12276-019-0359-3 |
| [39] | Han HS, Hwang S, Choi SY, et al. Roseburia intestinalis-derived extracellular vesicles ameliorate colitis by modulating intestinal barrier, microbiome, and inflammatory responses[J]. J Extracellular Vesicle, 2024, 13(8): e12487. DOI:10.1002/jev2.12487 |
| [40] | Weyant KB, Oloyede A, Pal S, et al. A modular vaccine platform enabled by decoration of bacterial outer membrane vesicles with biotinylated antigens[J]. Nat Commun, 2023, 14: 464. DOI:10.1038/s41467-023-36101-2 |
| [41] | Micoli F, Adamo R, Nakakana U. Outer membrane vesicle vaccine platforms[J]. BioDrugs, 2024, 38(1): 47-59. DOI:10.1007/s40259-023-00627-0 |
| [42] | Xiao YJ, Yuan YX, Hu DH, et al. Exosome-derived microRNA: potential target for diagnosis and treatment of sepsis[J]. J Immunol Res, 2024, 2024: 4481452. DOI:10.1155/2024/4481452 |
| [43] | Gebeyehu GM, Rashidiani S, Farkas B, et al. Unveiling the role of exosomes in the pathophysiology of sepsis: insights into organ dysfunction and potential biomarkers[J]. Int J Mol Sci, 2024, 25(9): 4898. DOI:10.3390/ijms25094898 |
| [44] | Li L, Huang L, Huang CY, et al. The multiomics landscape of serum exosomes during the development of sepsis[J]. J Adv Res, 2022, 39: 203-223. DOI:10.1016/j.jare.2021.11.005 |
| [45] | Bierwagen J, Wiegand M, Laakmann K, et al. Bacterial vesicles block viral replication in macrophages via TLR4-TRIF-axis[J]. Cell Commun Signal, 2023, 21(1): 65. DOI:10.1186/s12964-023-01086-4 |
| [46] | Zhao S, Di YF, Fan HL, et al. Targeted delivery of extracellular vesicles: the mechanisms, techniques and therapeutic applications[J]. Mol Biomed, 2024, 5(1): 60. DOI:10.1186/s43556-024-00230-x |
| [47] | Hao LL, Liu YX, Szeto IM, et al. Milk exosome-based delivery system for probiotic encapsulation that enhances the gastrointestinal resistance and adhesion of probiotics[J]. Nutrients, 2025, 17(5): 923. DOI:10.3390/nu17050923 |
| [48] | Mierzejewska J, Kowalska P, Marlicka K, et al. Exploring extracellular vesicles of probiotic yeast as carriers of biologically active molecules transferred to human intestinal cells[J]. Int J Mol Sci, 2023, 24(14): 11340. DOI:10.3390/ijms241411340 |
| [49] | Welsh JA, Goberdhan DCI, O'Driscoll L, et al. Minimal information for studies of extracellular vesicles (MISEV2023): From basic to advanced approaches[J]. J Extracell Vesicles, 2024, 13(2): e12404. DOI:10.1002/jev2.12404 |
 2026, Vol. 35
2026, Vol. 35