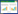2. 浙江省人民医院(杭州医学院附属人民医院)核医学科, 杭州 310014
脑卒中作为全球第二大疾病,具有极高的致死率和致残率[1]。针对脑卒中,常规方法治疗效果不佳[2],亟需开发新疗法以提高疗效及改善预后。近年来,基于干细胞开发出一种与人脑结构类似的三维培养系统,即脑类器官[3],对神经系统疾病的研究和治疗具有巨大潜力[4]。本文现对脑类器官研究的最新进展进行综述。
|
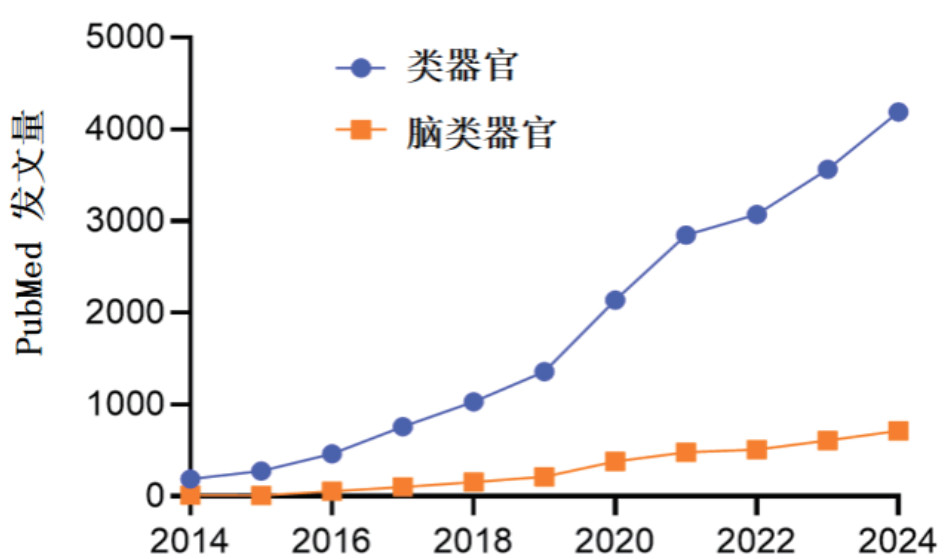
近年来,随着类器官研究领域的不断扩展,类器官特别是脑类器官已成为研究者日益关注的热点,相关研究近十年均呈逐年增长趋势(图 1)。脑类器官是干细胞衍生的三维组织,它在体外概括了早期大脑发育和脑微环境形成过程,被用于体外研究和模拟各种神经系统疾病[5-6]。
|
| 图 1 2014—2024年类器官和脑类器官相关研究的PubMed收录文章数量 |
|
|
类器官起源于20世纪70年代,Howard Green最开始证明原代人角质形成细胞和成纤维细胞共培养可以形成类似于人表皮的分层鳞状上皮集落[7]。2009年, Sato等[8]开发了一种3D培养物来重建肠道干细胞的体外环境并获得微型肠道类器官。随后,在3D培养技术不断发展的基础上, 科学家们先后培养出了脑、心脏、肾脏、肝脏、胰腺等类器官。目前, 类器官已广泛应用于疾病建模、药物毒性检测、基因和细胞治疗等领域[9]。
1.3 脑类器官研究脑类器官的起源标志着干细胞研究和再生医学领域的一大飞跃[10]。1998年,James Thomson首次从捐赠的人类胚胎分离得到人胚胎干细胞(embryonic stem cells,ESCs),为人类干细胞研究奠定了基础[11]。2006年,Takahashi和Yamanaka教授[12]通过引入Oct3/4、Sox2、c-Myc和Klf4四种因子,成功制造出人诱导多功能干细胞(induced pluripotent stem cells,iPSCs),为人类提供了一种不依赖胚胎的干细胞来源。2013年,Lancaster首次建立了包含多个脑区的脑类器官培养方法,标志着脑类器官技术的正式诞生[5]。随后,Sasai课题组应用其研制的无血清培养基,通过在不同时间点加入不同的形态发生因子,从人源ESCs培养出脑类器官[13]。上述进展推动了对大脑发育和疾病机制的理解,也为疾病模型的建立和再生医学的应用开辟了新途径。
2 脑类器官的分化和培养脑类器官是一种三维球状细胞聚集体,具备与活体组织相仿的生理和结构特性。它主要由人多能干细胞(human pluripotent stem cells,hPSCs)分化而成,其中hPSCs包括人ESCs和iPSCs[14]。生成脑类器官的方法可以分为两大类:非诱导分化和诱导分化。非诱导分化是指完全依赖于自发形态发生和hPSCs聚集物的内在分化能力,自发形成全脑类器官。诱导分化是需要补充外部模式因子来诱导hPSCs向特定细胞类型分化,形成具有区域特征的脑类器官,比如:视杯、下丘脑、海马类器官等。
2.1 非诱导分化非诱导分化方法主要依赖于hPSCs的自发形态发生和内在信号传导能力,以生成包含多种细胞谱系特征的脑类器官[15]。在这种方法中,hPSCs在基质胶中悬浮生长[5],能够自然发育成各种细胞类型,包括背侧前脑、腹侧前脑、中脑、后脑、海马、脉络丛等细胞[15]。然而,鉴于分化过程具有较高的随机性,每个类器官中不同细胞谱系的比例和分布难以预测。尽管该方法能够模拟自然发育过程,但其可重复性和一致性相对较弱。
2.2 诱导分化诱导分化是利用小分子和生长因子诱导形成特定脑区的细胞和结构。通常通过抑制BMP/TGF-β信号通路促进神经谱系形成,并使用相关生长因子(如fibroblast growth factor 2和胰岛素等)诱导脑类器官进一步定向分化。在诱导分化中,聚集的hPSCs被赋予外胚层命运,随后发育为区域特异度的类器官[16]。例如,科学家通过增强Wnt(wingless and int-1)信号通路的激活以促进神经上皮细胞的增殖和大脑皮质神经元的产生,同时使用骨形态发生蛋白(bone morphogenetic protein, BMP)拮抗剂可以使脑类器官特化为腹侧端脑类器官[17]; 通过增加特定转录因子如FOXA2和MSX1/2的表达,以及使用脑源性神经营养因子、胶质细胞源性神经营养因子来促进纹状体前体细胞的分化,从而获得纹状体脑类器官[18]。Eiraku等证明ESCs可以在快速无血清胚状体中自我组织形成具有顶基极性的皮质组织。此外,通过加入相关因子可以有选择地控制生成的皮质组织分化为嗅球、前脑、脑干、纹状体和脉络丛等[18]。Qian开发了一种微型旋转生物反应器生成了特定的脑类器官,包括前脑、中脑和下丘脑类器官[19]。Jo等[20]成功地从hPSCs中诱导形成了类似中脑的类器官。这些类器官含有功能性的多巴胺能神经元和产生黑色素的神经元,模拟了人类中脑的特征,同时还产生了与黑色素颗粒结构相似的类神经黑色素颗粒。Atamian等[21]成功开发了人源小脑类器官,该类器官能够发育出胎儿小脑复杂的细胞多样性,包括此前从未在体外生成的人类特异度菱唇祖细胞群,并且神经元之间能够建立功能连接和发生网络活动。与非诱导分化方式相比,诱导分化获得的脑类器官在批次和细胞系之间的差异较小,更具可重复性和一致性。
2.3 基于水凝胶的脑类器官培养脑类器官培养主要依赖于细胞外基质(extracellular matrix, ECM),基质胶作为支架材料能促进神经上皮芽的扩张和类器官的生长。水凝胶是一种具有高生物相容性和生物可降解性的合成聚合物,因其高稳定性、成分均匀性以及高通量特性,近年来其在脑类器官技术中的应用越来越广泛。
水凝胶已被用于通过调节干细胞微环境来促进神经分化和脑类器官的形成。透明质酸水凝胶作为中枢神经系统的ECM成分之一,在神经分化中发挥多种作用[22]。Simsa等[23]研究使用去细胞化猪脑ECM水凝胶作为支架材料来支持hESCs来源的大脑类器官的形成。此外,Cell-Mate 3D水凝胶显示出高弹性模量以促进神经分化,所产生的类器官表现出类似于体内早期皮质生成的神经管样结构,并显示出限定的脑区域,包括前脑、中脑和后脑[24]。Lancaster使用聚乳酸-羟基乙酸共聚物纤维微丝作为浮动支架来生成细长的类胚体,显示出增强的神经外胚层形成和改善的皮质发育,能够模拟大脑皮层的独特径向组织,并可用于研究神经元迁移[25]。总之,水凝胶有助于提高脑类器官模型的生物相容性和功能性,基于水凝胶的脑类器官形成方法为研究神经发育障碍、阐明相关病理机制和开发神经疾病的治疗方法提供了潜在的策略。
3 利用脑类器官构建体外研究模型 3.1 血管化的脑类器官神经血管单元(neurovascular unit, NVU)由微血管内皮细胞、周围神经元、星形胶质细胞、周细胞和基质体组成[26]。它通过神经血管偶联过程调节血流,提供营养支持,产生生长因子和旁分泌信号,指导神经元分化,并招募少突胶质细胞等[27]。由于脑类器官来源于神经外胚层组织,因此缺乏中胚层起源的脑血管。脑类器官可以在体外培养一年以上,但是实际上在几个月后会停止增长,这是因为类器官核心区域的细胞会死亡,营养物质不能到达距离表面超过200~400 µm的细胞[5]。特定的设备,如轨道振荡器或生物反应器已被用来促进氧气和营养供应[28]。所以,为了更好的模拟体外疾病模型,在脑类器官内建立有效的神经血管系统是必须的。Cakir通过在人ESCs中表达人类ETS变体转录因子2,成功诱导了血管样结构的形成。这些血管样结构在脑类器官中形成了复杂的网络,并且这些血管化的脑类器官表现出了更好的健康状况,如细胞死亡减少等[29]。此外血管化的脑类器官还可以使成熟神经元的数量增加[30]。但是,血管化的脑类器官仍不完美,在能够精确再现神经血管系统的发育、功能和病理之前,仍需进一步优化。
3.2 脑类器官模拟脑卒中模型脑卒中一直使用动物进行建模,由于种属间差异,动物模型存在一定局限性。而脑类器官能够克服种属间差异,并且可以展示出不同细胞类型间的相互作用,能更好地模拟体内微环境[31]。脑类器官已被用于模拟神经退行性疾病,但是其缺乏血管系统和小胶质细胞仍然是卒中建模的限制因素[32]。尽管如此,不少研究者在脑类器官模拟脑卒中模型方向进行了成功的尝试。Wang等[33]利用脑类器官创建了一个模拟缺血性脑卒中的模型。该研究用脑类器官建立氧糖剥夺(oxygen glucose deprivation, OGD)诱导的缺血性脑卒中模型,结果提示随着OGD暴露时间的延长,脑类器官的缺血损伤加重。该研究还验证了模型对缺血损伤和相关治疗的敏感度等。De Paola等[34]利用人iPSCs形成的脑类器官作为研究脑缺血神经毒性模型,结果提示脑类器官的神经元损伤程度与OGD的严重程度成正比。Iwasa等[35]研究了人脑类器官在OGD及再氧合条件下的基因表达谱。研究发现,过氧化物酶体增殖物激活受体信号通路和丙酮酸激酶M2同工酶是神经细胞响应氧糖剥夺/再灌注的关键标记物。上述结果表明,基于人脑类器官的缺血性脑卒中模型能够为抗脑卒中治疗及相关药物开发提供一个可行的研究平台。
3.3 脑类器官体外模型的不足脑类器官体外模拟脑卒中仍有很大挑战。首先,缺乏血管和免疫环境是使用脑类器官的重大障碍。现已产生了血管化的脑类器官,但是在类器官中仍然难以建立免疫生态位[29-30]。其次,脑类器官虽然为治疗神经系统疾病带来了便利,但是也存在伦理挑战,包括一系列法律和道德问题等[36],特别是随着类器官技术的发展,精细而复杂的大脑类器官可能会变得有意识。因此,完善相关的指导方针和建立监督机构对于脑类器官研究是必要的[37]。
4 脑类器官治疗脑卒中 4.1 脑卒中后的微环境改变脑卒中后梗死的核心区域会迅速发生细胞坏死和组织丢失,而缺血半暗带可以存活数小时甚至数天[38],这为治疗脑卒中提供了时间窗口。脑卒中后的主要病理、生理微环境改变包括缺氧、炎症、酸中毒和血脑屏障破坏等。
缺氧是脑卒中微环境的一个决定性特征,据报道,在大鼠脑缺血模型中,脑缺血核心区域的间质氧分压迅速下降至正常值的大约4%,而缺血半暗带的氧分压则降至缺血发生前的约30%[39]。脑血流中断后,缺血脑区的神经元会因氧气和营养供应不足,最终导致不可逆的坏死。炎症是影响脑卒中进展的关键病理特征。脑缺血后,凋亡或坏死细胞释放各种危险相关的分子[40],进而刺激炎性细胞因子和趋化因子的积累。炎性细胞因子会介导小胶质细胞分化为促炎性M1表型[41],进而引起许多促炎因子的释放[42],导致神经元损伤。缺血后释放的基质金属蛋白酶也会破坏内皮细胞之间的紧密连接,使血脑屏障通透性增加,导致离子和水的稳态失调,最终引起脑水肿[43]。
4.2 脑类器官移植治疗脑卒中既往研究明确了干细胞移植可以通过促进神经发生和血管再生来减轻脑卒中后神经损伤的作用[44],但其疗效并未令人满意,可能原因是干细胞为单一的细胞类型,直接用于移植治疗往往疗效欠佳。而脑类器官包括了神经祖细胞、神经干细胞、神经元和神经胶质细胞等多种细胞类型,因此,脑类器官移植在一定程度上克服了干细胞移植的局限性[45],有望通过多细胞类型移植取得令人鼓舞的效果。
研究表明,将脑类器官移植到小鼠双侧额叶和顶叶皮质中均显示出较高的存活率并发生血管化,同时在移植的脑类器官中观察到神经元投射,其轴突可沿宿主皮质脊髓束延伸至周围大脑皮质、胼胝体和宿主纹状体[46]。Wang等[47]将培养55 d的脑类器官移植到大脑中动脉闭塞的大鼠脑内,显著减少了脑梗死体积、改善了神经运动功能,并观察到移植的脑类器官能够分化为神经元并建立突触连接。此外,上述移植主要促进了移植区域周围的外源性神经发生以及海马和脑室下区的内源性神经发生。Cao等[48]通过光化学法诱导小鼠脑缺血模型,通过激活SHH(Sonic Hedgehog)信号通路定向诱导人iPSCs分化以生成脑类器官并移植到脑缺血小鼠的梗死皮质中,他们发现移植的脑类器官存活良好,并且主要分化为γ-氨基丁酸能中间神经元,显著促进了脑缺血小鼠的感觉运动功能恢复。移植部位的不同将影响脑类器官分化的结局,在梗死灶周围的脑类器官主要由成熟和未成熟的谷氨酰胺能神经元组成,而在梗死核心的脑类器官细胞则可分化为神经胶质细胞,上述不同的分化结果可能是由不同的炎症微环境所导致。以上研究证明了脑类器官移植治疗脑卒中的有效性并探索了初步的治疗机制。
5 小结与展望水凝胶在作为脑类器官载体的应用中,必须确保其不会引发宿主的免疫排斥反应。小胶质细胞在脑卒中后可起到调节免疫反应和炎症反应的作用,有利于神经功能的恢复[49]。然而,脑类器官中小胶质细胞的生成仍是一大难题,诱导脑类器官小胶质细胞分化将可能成为未来脑类器官移植治疗脑卒中的研究重点。因此,今后仍需进一步拓展和开发脑类器官的构建方法,以克服上述不足。
脑类器官在脑卒中研究中为开发神经保护、神经发育新分子方面提供了新研究平台,其不仅可以直接用于治疗脑卒中,还能作为体外模型开发潜在的治疗手段。总之,脑类器官在推动脑卒中研究和改善治疗方案方面具有巨大的潜力和广阔的前景,值得更深入的研究。
利益冲突 所有作者声明无利益冲突
作者贡献声明 李遥遥:选题设计及全文撰写; 王敏:文献收集与整理; 赵立军:文献查阅; 宋法寰:初稿校对及论文修订; 李恒杰:图表制作; 蔡文伟:最终审核
| [1] | GBD 2021 Stroke Risk Factor Collaborators. Global, regional, and national burden of stroke and its risk factors, 1990-2021: a systematic analysis for the Global Burden of Disease Study 2021[J]. Lancet Neurol, 2024, 23(10): 973-1003. DOI:10.1016/S1474-4422(24)00369-7 |
| [2] | Hilkens NA, Casolla B, Leung TW, et al. Stroke[J]. Lancet, 2024, 403(10446): 2820-2836. DOI:10.1016/S0140-6736(24)00642-1 |
| [3] | Maisumu G, Willerth S, Nestor MW, et al. Brain organoids: building higher-order complexity and neural circuitry models[J]. Trends Biotechnol, 2025, 43(7): 1583-1598. DOI:10.1016/j.tibtech.2025.02.009 |
| [4] | Revah O, Gore F, Kelley KW, et al. Maturation and circuit integration of transplanted human cortical organoids[J]. Nature, 2022, 610(7931): 319-326. DOI:10.1038/s41586-022-05277-w |
| [5] | Lancaster MA, Renner M, Martin CA, et al. Cerebral organoids model human brain development and microcephaly[J]. Nature, 2013, 501(7467): 373-379. DOI:10.1038/nature12517 |
| [6] | 宋奕萱, 张明亮. 脑类器官技术的发展与应用[J]. 中国细胞生物学学报, 2021, 43(6): 14. |
| [7] | Rheinwald JG, Green H. Serial cultivation of strains of human epidermal keratinocytes: the formation of keratinizing colonies from single cells[J]. Cell, 1975, 6(3): 331-343. DOI:10.1016/s0092-8674(75)80001-8 |
| [8] | Sato T, Vries RG, Snippert HJ, et al. Single Lgr5 stem cells build crypt-villus structures in vitro without a mesenchymal niche[J]. Nature, 2009, 459(7244): 262-265. DOI:10.1038/nature07935 |
| [9] | Eichmüller OL, Knoblich JA. Human cerebral organoids: a new tool for clinical neurology research[J]. Nat Rev Neurol, 2022, 18(11): 661-680. DOI:10.1038/s41582-022-00723-9 |
| [10] | 庞溦, 刘彦彤, 向阳飞. 脑类器官技术研究进展[J]. 中国科学: 生命科学, 2023, 53(2): 161-74. DOI:10.1360/SSV-2021-0278 |
| [11] | Thomson JA, Itskovitz-Eldor J, Shapiro SS, et al. Embryonic stem cell lines derived from human blastocysts[J]. Science, 1998, 282(5391): 1145-1147. DOI:10.1126/science.282.5391.1145 |
| [12] | Takahashi K, Yamanaka S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors[J]. Cell, 2006, 126(4): 663-676. DOI:10.1016/j.cell.2006.07.024 |
| [13] | Kadoshima T, Sakaguchi H, Nakano T, et al. Self-organization of axial polarity, inside-out layer pattern, and species-specific progenitor dynamics in human ES cell-derived neocortex[J]. Proc Natl Acad Sci USA, 2013, 110(50): 20284-20289. DOI:10.1073/pnas.1315710110 |
| [14] | Ryu JO, Seong YJ, Lee E, et al. Applications and research trends in organoid based infectious disease models[J]. Sci Rep, 2025, 15(1): 25185. DOI:10.1038/s41598-025-07816-7 |
| [15] | Sun YB, Ikeuchi Y, Guo F, et al. Bioengineering innovations for neural organoids with enhanced fidelity and function[J]. Cell Stem Cell, 2025, 32(5): 689-709. DOI:10.1016/j.stem.2025.03.014 |
| [16] | Sidhaye J, Knoblich JA. Brain organoids: an ensemble of bioassays to investigate human neurodevelopment and disease[J]. Cell Death Differ, 2021, 28(1): 52-67. DOI:10.1038/s41418-020-0566-4 |
| [17] | Xiang YF, Cakir B, Park IH. Deconstructing and reconstructing the human brain with regionally specified brain organoids[J]. Semin Cell Dev Biol, 2021, 111: 40-51. DOI:10.1016/j.semcdb.2020.05.023 |
| [18] | Miura Y, Li MY, Birey F, et al. Generation of human striatal organoids and cortico-striatal assembloids from human pluripotent stem cells[J]. Nat Biotechnol, 2020, 38(12): 1421-1430. DOI:10.1038/s41587-020-00763-w |
| [19] | Qian XY, Nguyen HN, Song MM, et al. Brain-region-specific organoids using mini-bioreactors for modeling ZIKV exposure[J]. Cell, 2016, 165(5): 1238-1254. DOI:10.1016/j.cell.2016.04.032 |
| [20] | Jo J, Xiao YX, Sun AX, et al. Midbrain-like organoids from human pluripotent stem cells contain functional dopaminergic and neuromelanin-producing neurons[J]. Cell Stem Cell, 2016, 19(2): 248-257. DOI:10.1016/j.stem.2016.07.005 |
| [21] | Atamian A, Birtele M, Hosseini N, et al. Human cerebellar organoids with functional Purkinje cells[J]. Cell Stem Cell, 2024, 31(1): 39-51. e6. DOI:10.1016/j.stem.2023.11.013 |
| [22] | Pereira I, Lopez-Martinez MJ, Villasante A, et al. Hyaluronic acid-based bioink improves the differentiation and network formation of neural progenitor cells[J]. Front Bioeng Biotechnol, 2023, 11: 1110547. DOI:10.3389/fbioe.2023.1110547 |
| [23] | Simsa R, Rothenbücher T, Gürbüz H, et al. Brain organoid formation on decellularized porcine brain ECM hydrogels[J]. PLoS One, 2021, 16(1): e0245685. DOI:10.1371/journal.pone.0245685 |
| [24] | Xue XF, Kim YS, Ponce-Arias AI, et al. A patterned human neural tube model using microfluidic gradients[J]. Nature, 2024, 628(8007): 391-399. DOI:10.1038/s41586-024-07204-7 |
| [25] | Lancaster MA, Corsini NS, Wolfinger S, et al. Guided self-organization and cortical plate formation in human brain organoids[J]. Nat Biotechnol, 2017, 35(7): 659-666. DOI:10.1038/nbt.3906 |
| [26] | Gong YT, Wu MY, Huang YQ, et al. Research developments in the neurovascular unit and the blood-brain barrier (Review)[J]. Biomed Rep, 2025, 22(5): 88. DOI:10.3892/br.2025.1966 |
| [27] | Li TT, Li DY, Wei QY, et al. Dissecting the neurovascular unit in physiology and Alzheimer's disease: Functions, imaging tools and genetic mouse models[J]. Neurobiol Dis, 2023, 181: 106114. DOI:10.1016/j.nbd.2023.106114 |
| [28] | Licata JP, Schwab KH, Har-El YE, et al. Bioreactor technologies for enhanced organoid culture[J]. Int J Mol Sci, 2023, 24(14): 11427. DOI:10.3390/ijms241411427 |
| [29] | Cakir B, Xiang YF, Tanaka Y, et al. Engineering of human brain organoids with a functional vascular-like system[J]. Nat Methods, 2019, 16(11): 1169-1175. DOI:10.1038/s41592-019-0586-5 |
| [30] | Mansour AA, Gonçalves JT, Bloyd CW, et al. An in vivo model of functional and vascularized human brain organoids[J]. Nat Biotechnol, 2018, 36(5): 432-441. DOI:10.1038/nbt.4127 |
| [31] | Jalink P, Caiazzo M. Brain organoids: filling the need for a human model of neurological disorder[J]. Biology (Basel), 2021, 10(8): 740. DOI:10.3390/biology10080740 |
| [32] | 付程文, 卢国庆, 刘欣茹, 等. 血管化类器官的构建与应用的研究进展[J]. 齐齐哈尔医学院学报, 2025, 46(14): 1380-1386. DOI:10.3969/j.issn.1002-1256.2025.14.016 |
| [33] | Wang SN, Wang Z, Wang XY, et al. Humanized cerebral organoids-based ischemic stroke model for discovering of potential anti-stroke agents[J]. Acta Pharmacol Sin, 2023, 44(3): 513-523. DOI:10.1038/s41401-022-00986-4 |
| [34] | De Paola M, Pischiutta F, Comolli D, et al. Neural cortical organoids from self-assembling human iPSC as a model to investigate neurotoxicity in brain ischemia[J]. J Cereb Blood Flow Metab, 2023, 43(5): 680-693. DOI:10.1177/0271678X231152023 |
| [35] | Iwasa N, Matsui TK, Iguchi N, et al. Gene expression profiles of human cerebral organoids identify PPAR pathway and PKM2 as key markers for oxygen-glucose deprivation and reoxygenation[J]. Front Cell Neurosci, 2021, 15: 605030. DOI:10.3389/fncel.2021.605030 |
| [36] | 黄斌. 人脑类器官的伦理问题探析[J]. 医学与哲学, 2025, 10. DOI:10.12014/j.issn.1002-0772.2025.10.03 |
| [37] | 马永慧, 徐雅洁, 吕建伟. 人脑替代模型研究的伦理和治理建议[J]. 厦门大学学报(自然科学版), 2024, 63(5): 983-92. DOI:10.6043/j.issn.0438-0479.202407002 |
| [38] | Walther J, Kirsch EM, Hellwig L, et al. Reinventing the penumbra-the emerging clockwork of a multi-modal mechanistic paradigm[J]. Transl Stroke Res, 2023, 14(5): 643-666. DOI:10.1007/s12975-022-01090-9 |
| [39] | Liao J, Li Y, Fan L, et al. Bioactive ceria nanoenzymes target mitochondria in reperfusion injury to treat ischemic stroke[J]. ACS Nano, 2024. DOI:10.1021/acsnano.3c10982 |
| [40] | DeLong JH, Ohashi SN, O' Connor KC, et al. Inflammatory responses after ischemic stroke[J]. Semin Immunopathol, 2022, 44(5): 625-648. DOI:10.1007/s00281-022-00943-7 |
| [41] | Li RQ, Zhou Y, Zhang SS, et al. The natural (poly)phenols as modulators of microglia polarization via TLR4/NF-κB pathway exert anti-inflammatory activity in ischemic stroke[J]. Eur J Pharmacol, 2022, 914: 174660. DOI:10.1016/j.ejphar.2021.174660 |
| [42] | Yu YL, Liao XL, Xie XY, et al. The role of neuroglial cells communication in ischemic stroke[J]. Brain Res Bull, 2024, 209: 110910. DOI:10.1016/j.brainresbull.2024.110910 |
| [43] | Mou Y, Du Y, Zhou LX, et al. Gut microbiota interact with the brain through systemic chronic inflammation: implications on neuroinflammation, neurodegeneration, and aging[J]. Front Immunol, 2022, 13: 796288. DOI:10.3389/fimmu.2022.796288 |
| [44] | Kim HJ, Kim DH, Choi JI, et al. Human pluripotent stem cell-derived neuronal progenitor cells promote neurogenesis and functional recovery by attenuating neuroinflammation and via extracellular vesicles in a subacute stroke model[J]. Front Immunol, 2025, 16: 1650092. DOI:10.3389/fimmu.2025.1650092 |
| [45] | Sidhaye J, Knoblich JA. Brain organoids: an ensemble of bioassays to investigate human neurodevelopment and disease[J]. Cell Death Differ, 2021, 28(1): 52-67. DOI:10.1038/s41418-020-0566-4 |
| [46] | Kitahara T, Sakaguchi H, Morizane A, et al. Axonal extensions along corticospinal tracts from transplanted human cerebral organoids[J]. Stem Cell Reports, 2020, 15(2): 467-481. DOI:10.1016/j.stemcr.2020.06.016 |
| [47] | Wang SN, Wang Z, Xu TY, et al. Cerebral organoids repair ischemic stroke brain injury[J]. Transl Stroke Res, 2020, 11(5): 983-1000. DOI:10.1007/s12975-019-00773-0 |
| [48] | Cao SY, Yang D, Huang ZQ, et al. Cerebral organoids transplantation repairs infarcted cortex and restores impaired function after stroke[J]. NPJ Regen Med, 2023, 8(1): 27. DOI:10.1038/s41536-023-00301-7 |
| [49] | Shi LG, Lu LX, Hu J, et al. Repopulating microglia suppress peripheral immune cell infiltration to promote poststroke recovery[J]. CNS Neurosci Ther, 2025, 31(9): e70565. DOI:10.1111/cns.70565 |
 2026, Vol. 35
2026, Vol. 35