上消化道出血是指屈氏韧带以上的消化道,包括食管、胃、十二指肠或胰胆等病变引起的出血,胃空肠吻合术后的空肠病变出血亦属这一范围。危险性急性上消化道出血是指在24 h内大量出血至血流动力学紊乱、器官功能障碍,是急诊常见的危重症,起病急,病情凶险,如不及时合理地诊治,易导致患者死亡[1-2]。本研究总结北京积水潭医院急诊科2013年11月1日至2017年5月31日来收治的危险性急性上消化道出血的病例,分析主要治疗方法,并采取3种评分系统进行预后评估。
1 资料与方法 1.1 一般资料收集北京积水潭医院急诊科2013年11月1日至2017年5月31日危险性急性上消化道出血患者的临床资料。收集标准:呕血和(或)黑便,同时伴有以下之一者:(1)休克;(2)心动过速(心率>100次/min);(3)中重度贫血(Hb < 80 g/L)。纳入的所有患者给以急诊药物治疗的同时,联系消化科、放射介入科、外科等多科会诊,根据病情联合内镜、三腔二囊管压迫、介入治疗、外科手术等止血措施。
1.2 研究终点及诊断标准研究起始点:确诊为危险性急性上消化道出血,记录住院期间患者的预后转归情况(有无死亡及再出血)。将院内死亡或30 d内死亡作为临床研究终点。
再出血判断:①新发呕血,黑便次数增多、便质稀薄、血便;②经积极补液、输血治疗后周围循环衰竭症状改善不明显,或好转后又加重;③经胃管重新抽出新鲜血液;④血红蛋白或红细胞计数进行性下降;⑤补液和尿量充足,但血尿素氮持续升高;⑥内镜复查证实再出血。
1.3 评分及预后评估从收集的病例资料中提取AIMS65评分、Glasgow-Blatchford(GBS)评分以及Pre-Rockall评分系统中所需的各种参数,进行3种方法评分,评分标准见表 1~3。评价3种评分系统对疾病危险的诊断价值,预测患者的再出血率和病死率。结局指标:院内死亡或30 d内是否发生出血、院内死亡或30 d内是否死亡。
| 指标 | 检测结果 | 评分 |
| 收缩压(mmHg) | 100~109 | 1 |
| 90~99 | 2 | |
| < 90 | 3 | |
| 血尿素氮(mmol/L) | 6.5~7.9 | 2 |
| 8.0~9.9 | 3 | |
| 10.0~24.9 | 4 | |
| ≥25.0 | 6 | |
| 血尿素氮(mmol/L) | ||
| 男性 | 120~129 | 1 |
| 100~119 | 3 | |
| < 100 | 6 | |
| 女性 | 100~119 | 1 |
| < 100 | 6 | |
| 其他表现 | 脉搏≥100次/min | 1 |
| 黑便 | 1 | |
| 晕厥 | 2 | |
| 肝脏疾病 | 2 | |
| 心力衰竭 | 2 | |
| 注:1 mmHg=0.133 kPa | ||
采用SPSS 18.0软件进行统计分析,计量资料以均数±标准差(x ± s)表达,计数资料以例数(%)的形式表达,采用χ2检验,以P < 0.05为差异有统计学意义。
3种评分系统的临床价值采用受试者工作特征曲线(ROC)下面积法进行评估。分别绘制各种评分系统用于预测再出血率及病死率的ROC曲线图,并计算曲线下面积(AUC)。
2 结果 2.1 病例情况共收集141例,男性占70.92%,女性占29.08%。年龄20~93岁,平均年龄58.66岁。主要首发症状:呕血53.90%,黑便87.23%,晕厥14.18%。既往史:消化性溃疡9.22%,肝硬化24.11%,其中以乙肝肝硬化和酒精性肝硬化为主,有乙肝病史但无肝硬化7.80%,冠心病21.28%,高血压病28.37%,糖尿病15.60%,脑梗死9.22%,恶性肿瘤8.51%(其中肝癌6例,胃癌3例),口服阿司匹林17.02%,口服氯吡格雷4.26%,口服非甾体消炎药8.51%。主要阳性体征:收缩压 < 90 mmHg患者36.17%,心率>100次/min 61.7%,见表 4。
| 项目 | 结果 |
| 男性(例,%) | 100(70.92) |
| 年龄(岁,x ± s) | 58.66±18.37 |
| 既往史(例,%) | |
| 肝硬化 | 34(24.11) |
| 消化性溃疡 | 13(9.22) |
| 缺血性心脏病 | 30(21.28) |
| 高血压病 | 40(28.37) |
| 糖尿病 | 22(15.6) |
| 脑梗死 | 13(9.22) |
| 饮酒 | 8(5.67) |
| 恶性肿瘤 | 12(8.51) |
| 用药情况(例,%) | |
| 阿司匹林 | 24(17.02) |
| 氯吡格雷 | 6(4.26) |
| 非甾体消炎止痛药 | 12(8.51) |
| 首发症状(例,%) | |
| 呕血 | 76(53.9) |
| 黑便 | 123(87.23) |
| 晕厥 | 20(14.18) |
| 体征(例,%) | |
| HR > 100次/min | 87 (61.7) |
| SBP < 90 mmHg | 51 (36.17) |
| 实验室检查 | |
| 首次血红蛋白(g/L) | 77.63±22.45 |
| 血尿素氮(mmol/L) | 13.43±7.07 |
| 血白蛋白(g/L) | 34.84±5.63 |
| INR | 1.21±0.23 |
| 治疗及预后(例,%) | |
| 内镜检查 | 92 (65.25) |
| 金属夹止血 | 8 (5.67) |
| 硬化治疗 | 4 (2.84) |
| 三腔二囊管压迫 | 4 (2.84) |
| 输血 | 101 (71.63) |
| 放射介入治疗 | 12 (8.51) |
| 栓塞治疗 | 9 (6.38) |
| TIPS | 3 (2.13) |
| 院内/30 d内再出血 | 20 (14.18) |
| 院内/30 d内死亡 | 16(11.35) |
| 评分 | |
| AIMS65 | 1.28±1.17 |
| GBS | 12.39±3.10 |
| Pre-Rockall | 2.94±1.64 |
141例患者来诊后行内镜检查92例(65.25%),检查的时间为1 h~1个月。经过内镜检查,仅1例未明确出血原因,前三位病因分别为:十二指肠溃疡(38.04%,35/92)、胃溃疡(18.48%,17/92)、肝硬化并静脉曲张破裂(10.87%,10/92)。在49例未做内镜的患者中,根据既往史、辅助检查结果,临床推测出血病因,其中肝硬化并静脉曲张破裂最多,占44.90%,见表 5。
| 出血病因 | 内镜诊断 | 临床推测 |
| 十二指肠溃疡 | 35(38.04) | 2(4.08) |
| 胃溃疡 | 17(18.48) | 1(2.04) |
| 复合溃疡 | 5(5.43) | — |
| 吻合口溃疡 | 2(2.17) | — |
| 食管溃疡 | 3(3.26) | — |
| NASAID相关性溃疡 | — | 5(10.20) |
| 贲门黏膜撕裂 | 5(5.43) | — |
| 胃炎 | 7(7.60) | — |
| 肝硬化并静脉曲张破裂 | 10(10.87) | 22(44.90) |
| 肝癌 | — | 5(10.20) |
| 胃癌 | 5(5.43) | 2(4.08) |
| 反流性食管炎 | 1(1.07) | — |
| 不明原因 | 1(1.07) | 11(22.45) |
| 血管畸形 | 1(1.07) | — |
所有患者来诊后直接进入抢救室,予以心电监护,吸氧,开放静脉通路,补充血容量。每例患者均静脉应用质子泵抑制剂(80 mg+8 mg/h),静脉曲张破裂出血者同时持续静点生长抑素(252 μg/h),并根据失血情况输血。内镜下喷洒凝血酶或去甲肾上腺素等止血药物,其中金属止血夹治疗8例,硬化治疗4例。有无内镜检查对患者死亡的影响,差异有统计学意义,表明内镜检查及治疗,可以降低病死率。但是不同内镜检查时间对患者死亡的影响,差异无统计学意义(表 6~7)。留置三腔二囊管4例。难以控制的大出血,联系放射科行介入治疗,栓塞及经颈静脉肝内门-体静脉支架分流术(TIPS)共12例。外科手术止血2例。再出血率是14.18%,病死率为11.35%。
| 内镜检查 | 存活 | 死亡 | 总计 | P值 |
| 无 | 36(28.8) | 13(81.25) | 49 | < 0.01 |
| 有 | 89(71.2) | 3(18.75) | 92 | |
| 总计 | 125 | 16 | 141 |
| 检查时间 | 存活 | 死亡 | 总计 | P值 |
| ≤6 h | 13(14.61) | 2(66.67) | 15(16.30) | 0.173 |
| 7~12 h | 13(14.61) | 1(33.33) | 14(15.22) | |
| 13~24 h | 17(19.10) | 0(0) | 17(18.48) | |
| 25~48 h | 24(26.97) | 0(0) | 24(26.09) | |
| > 48 h | 22(24.71) | 0(0) | 22(23.91) | |
| 总计 | 89 | 3 | 92 |
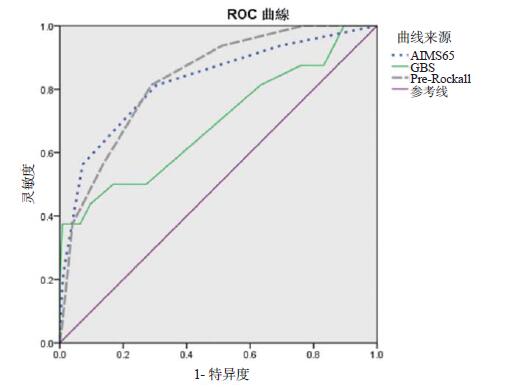
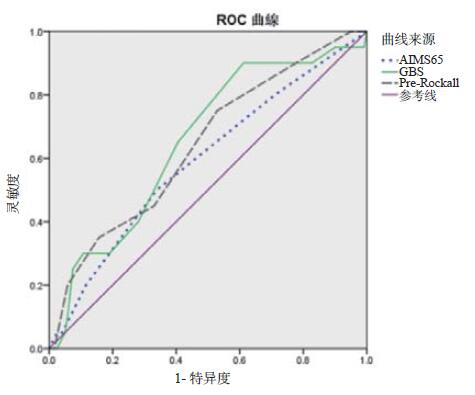
绘制计算ROC曲线,计算3种评分方法按不同指标绘制的AUC,结果表明,在预测院内死亡或30 d内病死率方面,最优的为Pre-Rocall评分,其次是AMIS65评分,最差的为Glasgow-Blachford(GBS)评分,AUC值分别为0.833、0.822、0.693。在预测院内死亡或30 d内再出血率方面,三个评分的AUC均不高,优选顺序依次为GBS评分、Pre-Rocall评分、AMIS65评分,AUC值分别为0.652、0.639、0.591,见表 8及图 1~2。
| 评分项目 | AUC | 95%CI |
| 院内死亡或30 d内死亡 | ||
| AIMS65 | 0.822 | 0.700~0.944 |
| GBS | 0.693 | 0.525~0.851 |
| Pre-Rockall | 0.833 | 0.737~0.929 |
| 院内再出血或30 d内再出血 | ||
| AIMS65 | 0.591 | 0.454~0.728 |
| GBS | 0.652 | 0.526~0.777 |
| Pre-Rockall | 0.639 | 0.509~0.768 |
|
| 图 1 AIMS65评分、Glasgow-Blachford(GBS)评分、Pre-Rockall评分用于预测院内/30 d内死亡的ROC曲线 Figure 1 ROCs for AIMS65 score, Glasgow-Blachford(GBS) score and Pre-Rockall score as predictors of inpatient/30 days mortality |
|
|
|
| 图 2 AIMS65评分、Glasgow-Blachford(GBS)评分、Pre-Rockall评分用于预测院内/30 d内再出血的ROC曲线 Figure 2 ROCs for AIMS65 score, Glasgow-Blachford(GBS) score and Pre-Rockall score as predictors of inpatient/30 days rebleeding |
|
|
成年人急性上消化道出血每年发病率为(100~180)/10万,危险性急性上消化道出血患者往往首诊于急诊科,临床占有的比例为15%~20%。这类出血多为累及较大血管的出血,包括严重的消化性溃疡出血、食管胃底静脉曲张破裂出血和侵蚀大血管的恶性肿瘤出血[1, 6]。本组研究中,经内镜检查,首位出血病因为消化性溃疡,占64.12%,其次食管静脉曲张破裂出血,占10.87%,这与国外文献报道有一定的差异。El-Kersh等[7]分析入住ICU的危险性出血患者133例,出血病因中首位也是消化性溃疡,但仅占21.1%,静脉曲张破裂出血为第三位,占14.3%。本研究中消化性溃疡的比例高,考虑与肝硬化、门脉高压的患者选择内镜检查少有关。未行内镜检查的患者,经临床推断的出血病因中,肝硬化并静脉曲张破裂出血者占44.9%,该类患者往往出血凶猛,病情危重,难以完成内镜检查,而有些患者合并肝癌,倾向于拒绝有创诊疗。
药物治疗是危险性急性上消化道出血的首选治疗手段,对于病情危重的患者,应立即予以生命支持和容量复苏,并采取“经验性联合用药”,方案为:静脉应用生长抑素+质子泵抑制剂[1]。本组研究中所有患者均给予质子泵抑制剂,其中静脉曲张破裂出血者联用生长抑素,以最大限度地降低严重并发症的发生率及病死率。危险性出血往往出血量大,病变严重,单纯的药物治疗难以控制。早在2000年,Blachford等[4]应用GBS评分来预测患者需要内镜、输血、手术、介入等治疗的可能性。GBS≥6分为高危患者,其中50%的患者需要多种治疗手段。评分越高,胃镜越有必要[8]。本组研究中,GBS评分仅2例为4分,其余都>6分,因此药物抢救的同时,联系消化科,根据患者的情况、意愿、医院条件,制定内镜检查计划。目前专家们一致认为,在出血24 h内,血流动力学稳定后,无严重合并症的患者应尽快行急诊内镜,对有高危征象的患者,应在12 h内行紧急内镜检查[1, 9-10]。内镜检查可以明确病因,并且通过喷洒药物、注射硬化剂、套扎、金属夹夹闭等进行镜下止血,但是内镜治疗的时机并不是越早越好。Lim等[11]进行的一个回顾性研究,纳入934例患者,分析GBS≥12分的高危患者,发现内镜检查的延迟是院内全因死亡相关的独立危险因素,存活组与死亡组之间的内镜检查的时间截点是13 h。本组研究中,GBS评分平均数为12.4,符合高危患者的标准,内镜组与未行内镜组相比,病死率降低(P < 0.01)。在92例完成内镜的患者中,< 12 h占29.22%,13~24 h占19.10%,>24 h占51.68%,内镜时机与病死率之间无明显相关,这与Kumar等[12]的报道基本一致,他们分析结果是低危组(GBS < 12)行紧急内镜(< 12 h)反而更容易达到复合终点事件(院内死亡、再出血、介入、手术等),而高危组(GBS≥12)是否行紧急内镜对于复合终点的发生率影响差异无统计学意义。另外,对于出血量大的危重患者,往往需要多科协作,这在赵蕊等[13]的研究提示有良好的抢救效果, 值得借鉴。
对于难以控制的危险性大出血患者应当及早考虑行介入治疗,包括血管造影及栓塞(TEA)、经颈静脉肝内门-体静脉支架分流术(TIPS),具有创伤小、成功率高、并发症少的特点,是药物和(或)内镜治疗失败患者的有效抢救措施[1]。已发表的多项研究表明,TEA在技术和临床上的成功率均较高,分别为69%~100%和63%~67%[14],因此近年来,对于高危出血患者,无论是否行内镜检查,TEA已经取代了手术治疗[15]。TIPS能在短期内显著降低门静脉压,对静脉曲张破裂出血的即刻止血成功率达90%~99%,目前提出实施早期TIPS的概念,即72 h内,最好24 h内实施[16]。本组研究中,共有12例(8.51%)患者行介入治疗,经药物、内镜下治疗后止血失败。3例TIPS应用于肝硬化并静脉曲张破裂出血,其中1例联合栓塞治疗,其他9例单纯栓塞治疗。2例栓塞治疗失败,1例死亡,1例手术补救成功。3例介入治疗后再出血,出血后1例手术,1例再次行TIPS,1例药物治疗,均未死亡。总结本组研究,介入治疗后即刻止血10例,成功率达83.33%(10/12),提示对于危险性大出血患者,应及早考虑介入治疗。
三腔二囊管压迫止血是一项传统的急救措施,可以为内镜、介入或手术止血争取时间及创造条件,适用于静脉曲张破裂大出血,也可应用于食管溃疡及贲门黏膜撕裂所致的大出血[17],其止血率80%,并发症发生率为10%~20%(主要是吸入性肺炎、气道阻塞等),再出血率25%~50%[1, 18]。但随着内镜技术的发展,三腔二囊管的应用已越来越少。本组研究中,留置三腔二囊管4例,3例明确为肝硬化,1例疑诊乙肝肝硬化,均表现为持续反复呕血,血流动力学不平稳,难以短时间内完成内镜或介入治疗。2例在留置过程中出现大呕血,其中1例迅速出现心搏呼吸停止。4例中3例死亡,均于来诊后30 h内死亡。压迫止血效果差的原因考虑与该组患者肝硬化、肝功能明显障碍等有关,亦不除外与三腔二囊管并发症的发生相关。留置时刺激咽喉部可加重恶心呕吐,大量呕血至气道堵塞窒息。另外,胃囊嵌顿在贲门或食管下端,通过胃迷走神经反射而引起致命性心律失常[19]。因此,本研究提示,三腔二囊管压迫止血在临床应用中应该根据病情及医疗条件进行合理选择。
急性上消化道出血的临床表现差异很大,病情较轻者可不治而愈,但对于危险性急性上消化道大出血患者则需要进行早期的个体化治疗,否则危及生命,因此准确、及时地评估患者的临床干预需求,预测患者的预后十分重要。目前常用的评分系统是Rockall评分、Glasgow-Blatchford评分(GBS)、AIMS65评分系统以及Child-Pugh分级[1]。Rockall评分≥5分为高危,死亡风险较高。其缺点为变量中有内镜诊断内容,限制了在早期急救的应用。为此,有文献将内镜内容去除,将剩下的几项变量组合成一种简化的评分系统,称为内镜前Rockall评分(Pre-Rockall)。GBS的特点是不需要内镜检查,且灵敏度高,适合在急诊救治中早期应用,在预测对治疗需求或死亡风险方面,优于Rockall评分。但GBS评分指标多,指标的分级过于复杂,不便于临床应用。AIMS65评分系统是新近推出的,可用于预测住院患者病死率,仅有5项变量。多项研究证实,在住院病死率方面,AIMS65评分具有良好预测作用[20]。Thandassery等[21]研究显示,评分为0~4分患者病死率分别为3%,7.8%,20%,36%,40%。本组研究通过回顾性研究,纳入141例急性危险性上消化道大出血的患者,来诊时有休克和(或)血红蛋白 < 80 g/L,初次评估均为高危,提示死亡风险高,因此为进一步评估该类患者的危险性,分别采用AIMS65评分、GBS评分以及Pre-Rokcall评分系统进行评价,比较三种评分系统评估院内死亡或30 d内死亡及再出血的准确性。从AUC的评价,发现Pre-Rockall评分和AIMS65评分评估死亡的准确性优于GBS,前两种评分的AUC均>0.8,显著高于GBS(AUC=0.693)。在评估再出血方面,三个评分的AUC值均不高,在0.55~0.7之间,准确性较低,其中GBS(AUC =0.652)最优。AMIS65评分和GBS的评估结果,与Martinez-Cara等[22]及陈剑等[23]近年来发表的研究得出的结论基本一致。本组研究还比较了Pre-Rockall评分系统,并发现其在预测病死率具有和AMIS65同样的准确性。因此,通过本组研究初步得出一个结论,Pre-Rockall和AIMS65均可准确地预测高危出血患者的院内死亡或30 d内病死率,并且这两个评分系统中的变量少,计算简单,都不需要内镜诊断内容,特别适用于急诊科的早期应用,为急诊医师正确判断病情及预后提供参考,从而指导临床进一步加强治疗,及时选择有效的止血手段,以达到降低病死率及再出血率的目的。
| [1] | 中国医师协会急诊医师分会. 急性上消化道出血急诊诊治流程专家共识[J]. 中国急救医学, 2015, 35(10): 865-873. DOI:10.3969/j.issn.1002-1949.2015.10.001 |
| [2] | Chen ZY, Martin L. Management of upper gastrointestinal bleeding emergencies: evidence-based medicine and practical considerations[J]. World J Emerg Med, 2011, 2(1): 5-12. DOI:10.5847/wjem.j.1920-8642.2011.01.001 |
| [3] | Rockall TA, Logan RF, Devlin HB, et al. Risk assessment after acute upper gastrointestinal haemorrhage[J]. Gut, 1996, 38(3): 316-321. DOI:10.1136/gut.38.3.316 |
| [4] | Blatchford O, Murray WR. A risk score to predict need for treatment for upper-gastrointestinal hemorrhage[J]. Lancet, 2000, 356(9238): 1318-1321. DOI:10.1016/s0140-6736(00)02816-6 |
| [5] | Saltzman JR, Tabak YP, Hyett BH, et al. A simple risk score accurately predicts in-hospital mortality, length of stay, and cost in acute upper GI bleeding[J]. Gastrointest Endosc, 2011, 74(6): 1215-1224. DOI:10.1016/j.gie.2011.06.024 |
| [6] | Hearnshaw SA, Logan RF, Lowe D, et al. Acute upper gastrointestinal bleeding in the UK: patient characteristics, diagnoses and outcomes in the 2007 UK audit[J]. Gut, 2011, 60(10): 1327-1335. DOI:10.1136/gut.2010.228437 |
| [7] | El-Kersh K, Chaddha U, Sinha RS, et al. Predictive role of admission lactate level in critically ill patients with acute upper gastrointestinal bleeding[J]. J Emerg Med, 2015, 49(3): 318-325. DOI:10.1016/j.jemermed.2015.04.008 |
| [8] | 缪青, 陈世耀. 急性消化道大出血的快速诊断和处理对策[J]. 中华医学杂志, 2015, 95(20): 1553-1554. DOI:10.3760/cma.j.issn.0376-2401.2015.20.001 |
| [9] | Gralnek IM, Dumonceau JM, Kuipers EJ, et al. Diagnosis and management of nonvariceal upper gastrointestinal hemorrhage: European society of gastrointestinal endoscopy(ESGE) guideline[J]. Endoscopy, 2015, 47: a1-46. DOI:10.1055/s-0034-1393172 |
| [10] | Fujishiro M, Iguchi M, Kakushima N, et al. Guidelines for endoscopic management of non-variceal upper gastrointestinal bleeding[J]. Dig Endosc, 2016, 28(4): 363-378. DOI:10.1111/den.12639 |
| [11] | Lim LG, Ho KY, Chan YH, et al. Urgent endoscopy is associated with lower mortality in high-risk but not low-risk nonvariceal upper gastrointestinal bleeding[J]. Endoscopy, 2011, 43(4): 300-306. DOI:10.1055/s-0030-1256110 |
| [12] | Kumar NL, Cohen AJ, Nayor J, et al. Timing of upper endoscopy influences outcomes in patients with acute nonvariceal upper GI bleeding[J]. Gastrointest Endosc, 2016, 85(5): 945-952. DOI:10.1016/j.gie.2016.09.029 |
| [13] | 赵蕊, 张丽瑶, 吴云海, 等. 45例多学科协作抢救急性上消化道大出血患者的临床分析[J]. 中华急诊医学杂志, 2014, 23(11): 1268-1270. DOI:10.3760/cma.j.issn.1671-0282.2014.11.019 |
| [14] | Lu Y, Loffroy R, Lau JY, et al. Multidisciplinary management strategies for acute non-variceal upper gastrointestinal bleeding[J]. Br J Surg, 2014, 101(1): 34-50. DOI:10.1002/bjs.9351 |
| [15] | Loffroy R, Rao P, Ota S, et al. Embolization of acute nonvariceal upper gastrointestinal hemorrhage resistant to endoscopic treatment: results and predictors of recurrent bleeding[J]. Cardiovasc Intervent Radiol, 2010, 33(6): 1088-1100. DOI:10.1007/s00270-010-9829-7 |
| [16] | Clinical Services and Standards Committee of the British Society of Gastroenterology. U. K. Guidelines on the management of variceal hamorrhage in cirrhotic patients[J]. Gut, 2015, 64(11): 1680-1704. DOI: 10.1136/gutjnl-2015-309262. |
| [17] | 王继恒, 王晓伟, 王昕, 等. 三腔二囊管治疗贲门黏膜撕裂导致的上消化道大出血[J]. 胃肠病学和肝病学杂志, 2013, 22(10): 1003-1005. DOI:10.3969/j.issn.1006-5709.2013.10.016 |
| [18] | Mitra V, Marrow B, Nayar M. Management of acute upper gastrointestinal bleeding[J]. Gastrointest Nurs, 1976, 10(7): 34-41. |
| [19] | 梁葵, 林春惠. 三腔二囊管压迫止血并发症的原因分析及护理对策[J]. 护理实践与研究杂志, 2009, 6(5): 16-18. DOI:10.3969/j.issn.1672-9676.2009.05.007 |
| [20] | Monteiro S, Gonçalves TC, Magalhães J, et al. Upper gastrointestinal bleeding risk scores: Who, When and Why?[J]. World J Gastrointest Pathophysiol, 2016, 7(1): 86-96. DOI:10.4291/wjgp.v7.i1.86 |
| [21] | Thandassery RB, Sharma M, John AK, et al. Clinical application of AIMS65 scores to predict outcomes in patients with upper gastrointestinal hemorrhage[J]. Clin Endosc, 2015, 48(5): 380-384. DOI:10.5946/ce.2015.48.5.380 |
| [22] | Martínez-Cara JG, Jiménez-Rosales R, Úbeda-Muñoz M, et al. Comparison of AIMS65, Glasgow-Blatchford score, and Rockall score in a European series of patients with upper gastrointestinal bleeding: performance when predicting in-hospital and delayed mortality[J]. United European Gastroenterol J, 2016, 4(3): 371-379. DOI:10.1177/2050640615604779 |
| [23] | 陈剑, 唐帅, 唐小华. AMIS65评分在急性上消化道出血患者危险分级及预后评估中的作用[J]. 临床急诊杂志, 2015, 16(10): 760-763. DOI:10.13201/j.issn.1009-5918.2015.10.008 |
 2018, Vol. 27
2018, Vol. 27




