2 福建省立医院急诊科,福州 350001;
3 中山大学附属孙逸仙纪念医院急诊科,广州 510120;
4 心肺脑复苏北京市重点实验室 100020
2 Department of Emergency Medicine, Fujian Provincial Hospital, Fuzhou 350001, China;
3 Department of Emergency Medicine, Sun Yat sen Memorial Hospital, Sun Yat-Sen University, Guangzhou 510120, China;
4 Beijing Key Laboratory of Cardiopulmonary Cerebral Resuscitation, Beijing Chao Yang Hospital, Capital Medical University, Beijing 100020, China
心搏骤停后综合征(post-cardiac arrest syndrome, PCAS)是影响心肺复苏(cardiopulmonary resuscitation, CPR)患者预后的重要因素,其具有独特而复杂的病理生理过程。PCAS中重要的受损靶器官之一是心脏,心功能受损是CA患者自主循环恢复(restoration of spontaneous circulation, ROSC)后未能存活出院的主要原因之一[1-2]。大量研究表明,ROSC后左心室收缩和舒张功能均受损害,且CA时间越长,复苏后心功能障碍越重[3-4]。硝酸酯类药物是使用最为广泛的非内皮依赖性抗心肌缺血药,无论内皮细胞功能和结构是否正常,均可发挥明确的血管平滑肌舒张效应。硝酸酯进入体内后通过释放一氧化氮刺激鸟苷酸环化酶,使环磷酸鸟苷浓度增加,降低细胞内钙浓度,导致血管平滑肌舒张。研究发现,硝酸异山梨酯可显著改善室颤型CA猪复苏后的心功能障碍[5],但其机制不完全清楚。本研究通过建立猪室颤型CA模型,明确硝酸异山梨酯是否能通过调控心肌细胞凋亡而改善CPR后心肌缺血-再灌注损伤和心功能。
1 材料与方法 1.1 实验动物准备本实验经首都医科大学附属北京朝阳医院伦理委员会审批,符合动物实验伦理标准。健康雄性实验用小型家猪30只,12~14月龄,体质量(30±2)kg。实验前晚间禁食,可自由饮水。耳缘静脉注射丙泊酚2 mg/kg诱导麻醉后,将猪仰卧位捆绑固定于手术台上。3%戊巴比妥钠30 mg/kg静脉推注,并以8 mg/(kg·h)持续静脉泵入以维持麻醉。芬太尼注射液以5 μg/(kg·h)速度泵入以维持镇痛。置入直径6.5 F的气管插管,接呼吸机(Drager-Evata Ⅳ, 德国德尔格公司),吸入氧体积分数为21%,通气频率为12~20次/min,潮气量为6~7 mL/kg。使用呼吸监护仪(CO2SMOplus, 美国Respironics公司)监测呼气末二氧化碳分压及潮气量。调整呼吸机参数使呼气末二氧化碳分压保持在35~40 mmHg(1 mmHg=0.133 kPa)。备皮后连接心电监护(HP-M1165,美国惠普公司),监测肢体导联心电图。将7 F鞘管置入左侧颈内静脉,用于放置双极临时起搏电极直至右心室。5 F动脉导管通过左侧股动脉置入升主动脉连接压力换能器及惠普监护仪测量主动脉压。7 F漂浮导管置入左股静脉并送入肺动脉,用以测量右房压(right atrial pressure, RAP)及心输出量(cardiac output, CO)。
1.2 心室颤动模型制作及实验过程手术结束后动物恢复30 min,按随机数字表法将动物分为:假手术组(n=6),对照组(n=12)和硝酸异山梨酯组(n=12)。对照组和硝酸异山梨酯组动物诱导室颤,即把起搏电极导线外接医用程控刺激仪(GY-600A,中国开封华南仪器有限公司),选择食道输出S1S2(300/200 ms)模式,8 : 1比例,步长-10 ms连续电刺激,直到出现室颤[6]。室颤的判断标准是动脉血压迅速下降,心电图显示室颤波形。室颤8 min后,开始进行标准程序CPR,即30 : 2按压/通气比例,按压频率100~120次/min,按压深度50 mm。每30次按压后以人工气囊通气2次(300 mL/次)。使用Q-CPR(HeartStart MRx监护/除颤仪,荷兰飞利浦公司)监测CPR质量[7]。2 min CPR后,以双向波150 J进行首次电除颤(HeartStart MRx监护/除颤仪,荷兰飞利浦公司)。如未成功,静脉给予肾上腺素(0.02 mg/kg)并再进行2 min CPR。4次除颤后仍未ROSC,则停止CPR,宣布动物死亡。ROSC标准:血压恢复,动脉压在50 mmHg以上或脉压>20 mmHg,并且持续时间超过1 min[8]。硝酸异山梨酯组在ROSC即刻给予硝酸异山梨酯(异舒吉,珠海许瓦兹制药有限公司),以2 μg/(kg·min)速度泵入6 h。假手术组及对照组以相同速度泵入生理盐水。复苏成功动物接受机械通气(参数同前)并监护4 h。4 h后除留一组静脉通路外,拔除气管插管及其他动静脉置管,放置于笼中观察至ROSC后24 h。假手术组动物除不进行致颤与CPR外,实验流程与其他各组相同。所有存活动物24 h后通过静脉注射过量麻醉剂及氯化钾被安乐死,随后解剖留取心肌标本备检。
1.3 指标测量时间及方法 1.3.1 血流动力学参数监测基础状态和CPR后2、6、12和24 h的心率、主动脉压、RAP、冠状动脉灌注压(coronary perfusion pressure, CPP)及CO。CPP定义为舒张末期主动脉压与RAP的差值。CO采用肺热稀释法通过中心静脉导管将4 ℃盐水注入右心房测定[9]。
1.3.2 心肌酶谱在以上各时间点抽取静脉血用荧光免疫分析仪(Triage MeterPro, Alere San Digeo. Inc., San Digeo, CA, USA)联合检测心肌肌红蛋白(MYO)、心肌型脂肪酸结合蛋白(H-FABP)、肌酸激酶同功酶(CK-MB)和肌钙蛋白I(cTNI)。
1.3.3 Western blot检测Bcl-2、Bax和活化Caspase-3取左室前壁心肌组织,以Western blot法检测Bcl-2(1 : 200, EMD Millipore, 美国)、Bax(1 : 500, Santa Cruz Biotechnology, 美国)、活化Caspase-3(1 : 500, Abcam Biotechnology, 英国)和GAPDH(1 : 250,Santa Cruz Biotechnology, 美国)表达。
1.3.4 病理标本检测留取左室前壁心肌组织,置于10%中性甲醛溶液中,经石蜡包埋固定、脱蜡、切片、苏木精-伊红(HE)染色,光镜下观察心肌病理学改变。采用TUNEL法常规处理各组左心室石蜡标本,实验步骤按照TUNEL试剂盒(罗氏诊断产品有限公司,德国)说明书执行。在每组5个200倍视野下观察凋亡细胞数和总细胞数。凋亡指数(%)=凋亡细胞数/总细胞数×100%。
1.4 统计学方法采用SPSS 22.0(IBM SPSS Statistics, 美国)软件进行统计学分析,正态分布的计量资料用均数±标准差(Mean±SD)表示。计量资料采用重复测量方差分析,组间两两比较采用Bonferroni检验;计数资料采用χ2检验。以P < 0.05为差异有统计学意义。
2 结果 2.1 复苏结果的评价对照组及硝酸异山梨酯组各有1只动物未复苏成功;两组动物CPR时间[(5.0±1.1)min vs(4.9±1.2)min, P > 0.05]差异无统计学意义。
2.2 血流动力学指标在基础状态下各组动物血流动力学指标的差异无统计学意义(均P > 0.05)。与假手术组相比,对照组和硝酸异山梨酯组ROSC后各个时间点的心率均显著增加,收缩末期和舒张末期主动脉压均显著降低;而上述指标在对照组和硝酸异山梨酯组之间的差异无统计学意义。对照组动物ROSC后各个时间点的舒张期RAP显著升高,而硝酸异山梨酯组显著低于对照组(P < 0.01)。硝酸异山梨酯组ROSC后12和24 h的CPP和ROSC后24 h的CO均显著高于对照组(均P < 0.05)。见表 1。
| 指标 | 基础状态 | ROSC | |||
| 2 h | 6 h | 12 h | 24 h | ||
| 心率(次/min) | |||||
| 假手术组 | 101±17 | 115±21 | 112±19 | 115±18 | 113±12 |
| 对照组 | 102±16 | 139±24a | 138±21a | 135±19a | 133±21a |
| 硝酸异山梨酯组 | 104±18 | 146±19a | 144±24a | 142±20a | 137±18a |
| sAOP(mmHg) | |||||
| 假手术组 | 136±12 | 139±10 | 134±11 | 131±13 | 132±12 |
| 对照组 | 138±14 | 95±16a | 102±18a | 109±19a | 105±19a |
| 硝酸异山梨酯组 | 134±15 | 93±15a | 91±17a | 93±19a | 99±20a |
| dAOP(mmHg) | |||||
| 假手术组 | 94±10 | 98±14 | 95±12 | 96±11 | 95±12 |
| 对照组 | 95±9 | 78±15a | 80±16a | 79±15a | 77±16a |
| 硝酸异山梨酯组 | 95±11 | 75±14a | 77±15a | 76±12a | 78±16a |
| dRAP(mmHg) | |||||
| 假手术组 | 3.2±0.5 | 4.1±0.6 | 3.9±0.5 | 3.4±0.4 | 3.3±0.5 |
| 对照组 | 3.5±0.4 | 9.2±1.1a | 9.9±1.0a | 9.7±0.9a | 9.4±0.8a |
| 硝酸异山梨酯组 | 3.6±0.3 | 4.5±0.9a | 4.2±1.1b | 4.1±1.0b | 4.0±0.8b |
| CPP(mmHg) | |||||
| 假手术组 | 91±8 | 93±10 | 92±9 | 91±12 | 91±11 |
| 对照组 | 90±9 | 68±16a | 70±17a | 68±15a | 66±14a |
| 硝酸异山梨酯组 | 89±8 | 70±13a | 73±10a | 73±7ab | 75±8ab |
| CO(L/min) | |||||
| 假手术组 | 3.5±0.3 | 3.5±0.4 | 3.4±0.2 | 3.5±0.2 | 3.2±0.4 |
| 对照组 | 3.7±0.5 | 2.2±0.9a | 2.0±0.7a | 2.1±0.8a | 2.4±0.7a |
| 硝酸异山梨酯组 | 3.6±0.6 | 2.4±0.5a | 2.3±0.6a | 2.5±0.5a | 3.1±0.4b |
| 注:CO,心输出量;CPP,冠脉灌注压;dAOP,舒张末期主动脉压;dRAP,舒张末期右房压;ROSC,自主循环恢复;sAOP,收缩末期主动脉压。与假手术组比较,aP < 0.05;与对照组比较,bP < 0.05 | |||||
ROSC后各个时间点对照组与硝酸异山梨酯组动物的肌红蛋白、H-FABP、CK-MB和cTnI均显著高于假手术组(均P < 0.05);硝酸异山梨酯组动物的上述指标均低于对照组,但只有ROSC后12和24 h的CK-MB与cTnI的组间差异有统计学意义(均P < 0.05)。见表 2。
| 指标 | 基础状态 | ROSC | |||
| 2 h | 6 h | 12 h | 24 h | ||
| 肌红蛋白(ng/mL) | |||||
| 假手术组 | 62.1±33.1 | 69.2±36.5 | 66.3±37.4 | 63.2±44.7 | 67.9±36.4 |
| 对照组 | 68.2±32.1 | 89.7±40.8a | 167.4±39.7a | 205.2±35.9a | 258.5±48.4a |
| 硝酸异山梨酯组 | 63.3±35.2 | 76.3±37.8 | 162.6±36.0a | 177.9±29.9a# | 198.5±40.4ab |
| H-FABP(ng/mL) | |||||
| 假手术组 | 2.1±0.1 | 2.5±0.3 | 2.3±0.4 | 2.6±0.2 | 2.9±0.4 |
| 对照组 | 2.2±0.2 | 9.5±1.8a | 17.4±7.7a | 24.2±8.9a | 28.5±9.4a |
| 硝酸异山梨酯组 | 2.3±0.2 | 8.7±1.5a | 14.5±7.0a | 17.9±7.9ab | 18.5±6.9ab |
| CK-MB(U/L) | |||||
| 假手术组 | 2.34±1.22 | 2.45±1.35 | 2.23±1.46 | 2.64±1.29 | 2.31±1.57 |
| 对照组 | 2.57±1.12 | 3.99±1.11a | 4.47±1.77a | 8.73±2.43a | 9.93±2.72a |
| 硝酸异山梨酯组 | 2.22±1.45 | 3.82±1.49a | 3.97±1.75a | 8.12±1.44a | 9.88±2.96a |
| 肌钙蛋白I(ng/L) | |||||
| 假手术组 | 0.09±0.01 | 0.12±0.02 | 0.10±0.02 | 0.12±0.03 | 0.11±0.02 |
| 对照组 | 0.07±0.03 | 0.69±0.11a | 0.88±0.19a | 0.93±0.15a | 1.11±0.26a |
| 硝酸异山梨酯组 | 0.09±0.03 | 0.66±0.17a | 0.86±0.12a | 0.96±0.11a | 0.99±0.29a |
| 注:CK-MB, 肌酸激酶同功酶-MB; H-FABP, 心肌型脂肪酸结合蛋白; ROSC, 自主循环恢复。与假手术组比较, aP < 0.05;与对照组比较, bP < 0.05 | |||||
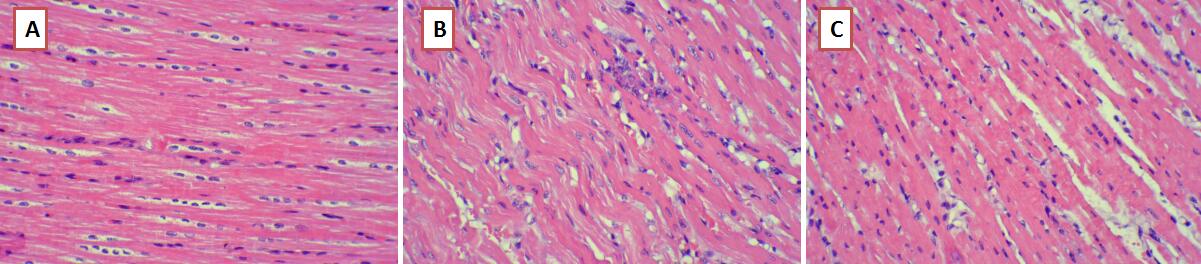
HE染色结果显示,假手术组心肌细胞膜完整,心肌纤维走行整齐,无炎性细胞浸润,心肌组织未见明显病理改变。对照组心肌细胞膜损伤,心肌纤维排列紊乱,细胞胞浆深染,心肌纤维断裂伴有大量炎性细胞浸润。与对照组相比,硝酸异山梨酯组心肌细胞变性程度以及炎性细胞浸润程度均有所减轻(图 1)。
|
| A:假手术组心肌细胞膜完整,心肌纤维走行整齐,无炎性细胞浸润。B:对照组心肌细胞膜损伤,心肌纤维排列紊乱,细胞胞浆深染,心肌纤维断裂伴有大量炎性细胞浸润。C:硝酸异山梨酯组心肌细胞变性程度以及炎性细胞浸润程度均有所减轻 图 1 心肌HE染色(×200) Fig 1 HE stain of cardiac tissue (×200) |
|
|
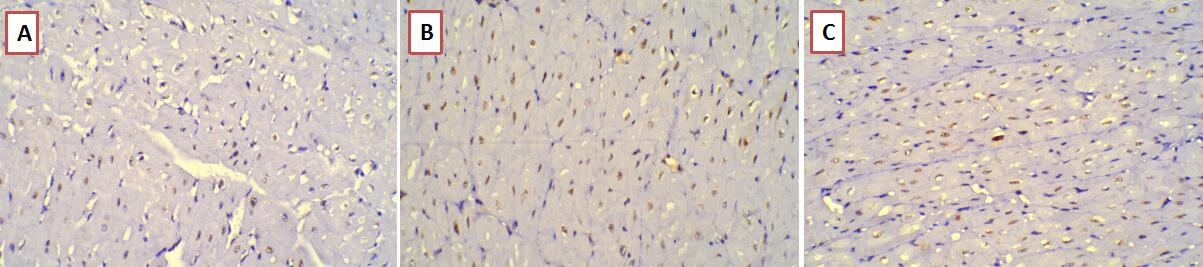
对照组心肌细胞凋亡指数显著高于假手术组[(55.4±19.9)% vs(13.1±0.5)%,P < 0.05,图 2];与对照组相比,硝酸异山梨酯组心肌细胞凋亡指数[(37.8±15.5)%]显著降低(P < 0.05)。
|
| A假手术组;B对照组;C硝酸异山梨酯组。TUNEL染色显示棕染细胞为凋亡细胞。对照组心肌细胞凋亡显著增加,硝酸异山梨酯组心肌细胞凋亡显著降低。 图 2 心肌TUNEL染色 Fig 2 TUNEL stain of cardiac tissue |
|
|
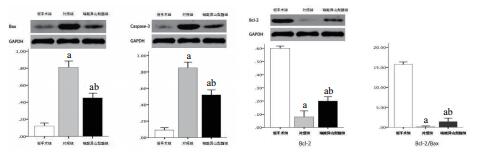
与假手术组相比,ROSC后24 h对照组Bax和活化Caspase-3表达显著升高,Bcl-2及Bcl-2/Bax显著降低(均P < 0.05,图 3)。而与对照组相比,ROSC后24 h硝酸异山梨酯组Bax和活化Caspase-3表达显著降低,Bcl-2及Bcl-2/Bax显著升高(均P < 0.05)。
|
| 与假手术组相比较,aP < 0.05;与对照组相比较,bP < 0.05 图 3 心肌细胞凋亡指标Western blot结果 Fig 3 Western blot analysis of apoptosis indexes of cardiac cells |
|
|
CA引起血流突然中断,导致心肌缺血、缺氧。即使在成功复苏后心排血量也减少至原来的1/3或1/2,引起主动脉压及CPP下降,从而进一步加重心肌缺血,这是造成复苏后心功能障碍的主要原因,也是CPR指南推荐在此期间优化血流动力学治疗的理论基础[10]。即便能够成功达到ROSC,缺血-再灌注损伤导致的进一步损伤也会降低最终的复苏成功率。心肌缺血-再灌注损伤主要表现为心律失常、心肌顿抑、微管阻塞(无复流现象)和再灌注引起的心肌细胞死亡[11-12],而细胞凋亡是再灌注损伤引起的心肌细胞死亡的主要形式[13]。缺血-再灌注过程中,心肌细胞的凋亡途径涉及信号分子很多,如细胞色素C、Bcl-2、Bax等,但Caspase-3是大部分信号途径下游的共同通路[14-15]。预防再灌注引起的心肌细胞凋亡是防止缺血-再灌注损伤的关键。因此,寻找一种效的改善心功能障碍药物,以降低CA患者复苏后的病死率是亟待研究解决的问题。
硝酸异山梨酯是一种在临床上广泛使用的改善心肌缺血药物。关于硝酸酯类药物在CPR中的应用,Schultz等[16]发现其可以改善CPR后实验动物的颈脉动脉血流和呼气末CO2,提高ROSC率。硝酸酯类药物的血管效应呈剂量依赖性,随着递增依次扩张静脉、大中动脉和外周阻力小动脉。扩张静脉血管,可以减少回心血量,使心脏前负荷和室壁张力下降;扩张外周阻力小动脉,可以使血压和心脏后负荷下降,两者均可降低心肌氧耗量。本研究中,在硝酸异山梨酯干预后实验动物表现出的血流动力学效能可能主要与静脉系统扩张有关,表现为RAP明显降低,而对主动脉压并未产生显著影响,与对照组比较差异无统计学意义。最终使CPP显著增加,改善了CPR后心肌灌注。同时,硝酸异山梨酯还可以扩张冠状动脉和侧支循环血管,使冠状动脉血流重新分布,增加缺血区域尤其是心内膜下的血液供应。在临床常用剂量范围内不引起微动脉扩张,可避免“冠状动脉窃血”。随着冠脉供血的改善,心功能也随之改善,表现为CO的增加。这在硝酸异山梨酯组动物CPR后24 h表现得尤为明显。因此,本实验的研究结果表明硝酸酯类药物可改善机体的血流动力学,改善心肌能量代谢,提高左室射血分数,减轻心肌细胞缺血-再灌注损伤。心肌细胞损伤的改善也被MYO及H-FABP的显著降低所证实。但由于CK-MB和c-TnI峰出现较为迟缓,本实验持续时间相对较短,未观察到硝酸异山梨酯组中CK-MB和c-TnI的显著变化。在今后的研究中,如能延长实验时间,也可能会有进一步发现。
| [1] | Tang W, Weil MH, Sun S, et al. Epinephrine increases the severity of postresuscitation myocardial dysfunction[J]. Circulation, 1995, 92(10): 3089-3093. DOI:10.1161/01.CIR.92.10.3089 |
| [2] | Gazmuri RJ, Weil MH, Bisera J, et al. Myocardial dysfunction after successful resuscitation from cardiac arrest[J]. Crit Care Med, 1996, 24(6): 992-1000. DOI:10.1016/0300-9572(96)89072-1 |
| [3] | Kern KB, Hilwig RW, Rhee KH, et al. Myocardial dysfunction after resuscitation from cardiac arrest: an example of global myocardial stunning[J]. J Am Coll Cardiol, 1996, 28(1): 232-240. DOI:10.1016/0735-1097(96)00130-1 |
| [4] | Tang W, Weil MH, Sun S, et al. Progressive myocardial dysfunction after cardiac resuscitation[J]. Crit Care Med, 1993, 21(7): 1046-1050. DOI:10.1097/00003246-199307000-00022 |
| [5] | 杭晨晨, 王涛, 唐子人, 等. 硝酸异山梨酯改善猪心肺复苏后的心功能障碍[J]. 中华急诊医学杂志, 2016, 25(9): 1136-1141. DOI:10.3760/cma.j.issn.1671-0282.2016.09.009 |
| [6] | 武军元, 李春盛. 应用程控刺激的心脏骤停模型[J]. 中华急诊医学杂志, 2008, 17(10): 1063-1065. DOI:10.3760/j.issn:1671-0282.2008.10.014 |
| [7] | Wu J, Li C, Liu Z, et al. A comparison of 2 types of chest compressions in a porcine model of cardiac arrest[J]. Am J Emerg Med, 2009, 27(7): 823-829. DOI:10.1016/j.ajem.2008.07.001 |
| [8] | Yannopoulos D, Matsuura T, McKnite S, et al. No assisted ventilation cardiopulmonary resuscitation and 24-hour neurological outcomes in a porcine model of cardiac arrest[J]. Crit Care Med, 2010, 38(1): 254-260. DOI:10.1097/CCM.0b013e3181b42f6c |
| [9] | Von Spiegel T, Wietasch G, Bursch J, et al. Cardiac output determination with transpulmonary thermodilution: An alternative to pulmonary artery catheterization?[J]. Anaesthetist, 1996, 45: 1045-1050. DOI:10.1007/s001010050338 |
| [10] | Perkins GD, Jacobs IG, Nadkarni VM, et al. Cardiac arrest and cardiopulmonary resuscitation outcome reports: update of the Utstein Resuscitation Registry Templates for Out-of-Hospital Cardiac Arrest: a statement for healthcare professionals from a task force of the International Liaison Committee on Resuscitation (American Heart Association, European Resuscitation Council, Australian and New Zealand Council on Resuscitation, Heart and Stroke Foundation of Canada, InterAmerican Heart Foundation, Resuscitation Council of Southern Africa, Resuscitation Council of Asia); and the American Heart Association Emergency Cardiovascular Care Committee and the Council on Cardiopulmonary, Critical Care, Perioperative and Resuscitation[J]. Circulation, 2015, 132(13): 1286-1300. DOI:10.1161/CIR.0000000000000144 |
| [11] | Hausenloy DJ, Yellon DM. Myocardial ischemia-reperfusion injury: a neglected therapeutic target[J]. J Clin Invest, 2013, 123(1): 92-100. DOI:10.1172/JCI62874 |
| [12] | Vander Heide RS, Steenbergen C. Cardioprotection and myocardial reperfusion: pitfalls to clinical application[J]. Circ Res, 2013, 113(4): 464-477. DOI:10.1161/CIRCRESAHA.113.300765 |
| [13] | Webster KA. Programmed death as a therapeutic target to reduce myocardial infarction[J]. Trends Pharmacol Sci, 2007, 28(9): 492-499. DOI:10.1016/j.tips.2007.07.004 |
| [14] | Wang XB, Huang XM, Ochs T, et al. Effect of sulfur dioxide preconditioning on rat myocardial ischemia/reperfusion injury by inducing endoplasmic reticulum stress[J]. Basic Res Cardiol, 2011, 106(5): 865-78. DOI:10.1007/s00395-011-0176-x |
| [15] | Scarabelli TM, Stephanou A, Pasini E, et al. Different signaling pathways induce apoptosis in endothelial cells and cardiac myocytes during ischemia/reperfusion injury[J]. Circ Res, 2002, 90(6): 745-748. DOI:10.1161/01.RES.0000015224.07870.9A |
| [16] | Schultz JC, Segal N, Caldwell E, et al. Sodium nitroprusside-enhanced cardiopulmonary resuscitation improves resuscitation rates after prolonged untreated cardiac arrest in two porcine models[J]. Crit Care Med, 2011, 39(12): 2705-2710. DOI:10.1097/ccm.0b013e31822668ba |
 2019, Vol. 29
2019, Vol. 29




