2 漳州市医院 普外一科, 363000;
3 漳州市医院急诊科
急性胆囊炎是胆囊管梗阻和细菌感染引起的炎症,是普外科的常见急腹症之一,急诊手术治疗是急性胆囊炎目前较为普遍的治疗方式[1-2]。但由于急性胆囊炎症状重,术前基础情况差,术后并发症发生率高,尤其是对于老年患者,据最新的系统回顾和Meta分析报告显示术后病死率可高达17 %[3]。随着超声介入诊疗技术的发展,超声引导下PTGBD术在治疗高危急性胆囊炎中发挥了重要作用,相较于临床上传统的治疗急性胆囊炎的一般方法,无论是急诊开腹胆囊切除术还是腔镜胆囊切除术,超声引导下PTGBD术均具有术前准备时间短、患者对手术的耐受度高、手术过程简单、创伤小等优势,且可进行床旁操作,最新的临床指南中已把PTGBD列为更加优先的级别[4-5]。
由于胆囊壁在急性炎症期常出现水肿、增厚,常常影响普通二维超声对其轮廓显示的清晰度及对胆囊壁连续性的判断,同时,PTGBD术后可能出现出血、胆汁外漏等并发症[4],普通二维超声对上述并发症的诊断敏感性较差,当腹腔出血或胆汁漏出达到一定的量之后才能被普通二维超声发现,延误救治的最佳时机[5],本研究旨在分析双模态超声造影在PTGBD术前评估及术中引流效果判断、并发症诊断方面的应用价值。
1 资料与方法 1.1 一般资料本组33例,男21例,女12例。年龄60~96岁,(78.9±3.90)岁。30例主诉为右上腹疼痛,疼痛视觉模拟评分(VAS)平均(6.0±1.4)分,3例以高热及消化道症状就诊。起病时间6~90 h,(30.8±4.9)h。查体:入院时腋下体温为37. 9~41.3℃,(38.9±0.4)℃,均有右上腹压痛,23例有反跳痛,20例可触及肿大的胆囊。辅助检查:血常规:白细胞计数平均16. 3±3.6(8. 6~29. 8) × 109/L,中性粒细胞百分比88.2%±6.3% (65.0% ~95.1 %)。均经急诊超声或急诊CT提示急性胆囊炎,其中结石性胆囊炎21例; 胆囊颈部结石嵌顿7例; 合并疾病:缺血性脑血管疾病3例; 心血管系统疾病13例(冠心病9例,高血压病19例,心律失常6例); 糖尿病18例; 呼吸系统疾病8例(呼吸衰竭3例,慢性阻塞性肺疾病8例,肺炎3例); 肾病3例(肾功能衰竭1例,肾功能不全2例)。合并2项或2项以上异常者19例。参照中华医学会外科学分会胆道外科学组制定的《急性胆道系统感染的诊断和治疗指南(2011版)》的标准,本组急性胆囊炎均为Ⅲ级。本组病例根据体质状况和对手术危险性评估,按美国麻醉医师协会(ASA)分级均为Ⅲ级及以上。排除标准:(1)患者凝血功能明显异常,有严重出血倾向者; (2)有大量腹水的患者(3)无安全进针路径(4)无法配合操作的患者。
1.2 仪器材料 1.2.1主要仪器迈瑞公司M9彩色多普勒超声诊断仪,配备超声造影软件。穿刺时使用凸阵探头,频率2~5 MHz; 超声造影检查采用CnTI低机械指数造影技术,MI < 0.1。
1.2.2 穿刺管选择用6~10 F猪尾导管(SKATER, PBN Medical, Denmark),由金属穿刺针、支撑管及”J”形引流管及引流管内固定线构成,选用18G-PTC针及0.89 mm导丝。超声造影剂:意大利Bracco公司所生产的超声造影剂声诺维(SonoVue)。使用前用5 mL 0.9%生理盐水溶解25 mg SonoVue冻干粉,震荡混匀,配制成悬浊液待静脉造影使用; 抽取0.1 mL SonoVue悬浊液加至20 mL 0.9%生理盐水中,待引流管造影使用。上述造影剂配置后限6 h内使用。
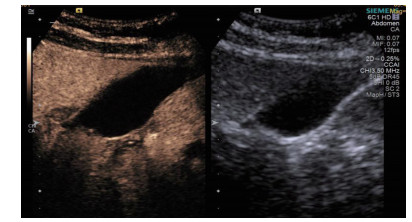
1.3 手术过程 1.3.1术前经肘静脉超声造影:行PTGBD前半h经肘静脉快速团注SonoVuel 5 mL,在对比脉冲序列造影成像模式下进行观察,根据不同组织造影剂凝聚的时间及浓度差异,判断胆囊周围组织黏连程度、胆囊壁完整程度(图 1),如出现胆囊壁造影剂充盈缺损(图 2、3),则考虑胆囊壁坏死或穿孔,根据静脉造影情况选择合适的置管入路,避开胆囊穿孔的部位及黏连组织。
|
| 图 1 经肘静脉超声造影胆囊图像,造影图(左),二维超声图(右) |
|
|
|
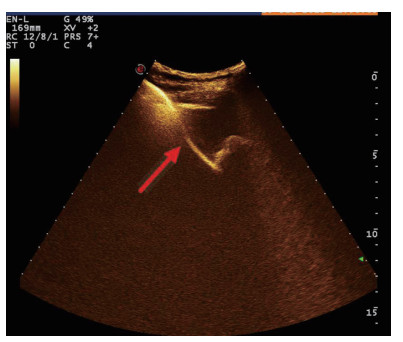
| 图 2 穿刺后经引流管超声造影,显示置管路径(箭头处) |
|
|
|
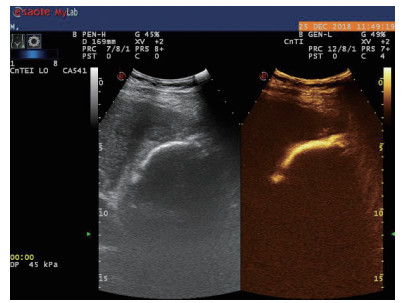
| 图 3 经引流管造影胆囊超声显像,二维图像(左),造影图像(右) |
|
|
均采用塞丁格(Seldinger)技术置入引流管(图 4):穿刺穿刺点的选择①左侧卧位,超声确定胆囊床方位,取腋前线肋间或肋缘下进针; ②经肝的路径长度应大于2.0 cm胆囊穿刺点为中上部距离胆囊颈约1 /3的位置; ③穿刺路径上尽量避开大血管及大胆管结构; ④结合术前经肘静脉超声造影情况,避开胆囊穿孔部位及周边黏连组织。操作过程:由超声介入治疗组专业医师单人操作,为获得更自由的穿刺角度以及在穿刺过程中根据患者呼吸活动随时对进针角度进行调整,本组操作均未使用超声探头引导架。操作步骤①常规碘伏皮肤消毒,2%利多卡因局部麻醉至肝脏被膜。操作医师一手持超声探头,清晰显示进针入路,一手持18 G PTC穿刺针经皮经肝由胆囊床穿刺进入胆囊,拔出针芯,可见胆汁自行流出或用20 mL注射器回抽见胆汁。②沿针鞘置入导丝,超声探查见导丝进入胆囊,拔出针鞘。③扩张器扩张针道。④根据抽出胆汁的混浊程度,沿导丝置入合适型号的引流管,确定引流管通畅后拔出导丝,拉紧猪尾导管的外置固定线,使导管弯曲头牢固卷曲,形成内固定,皮肤缝线外固定引流管,双重固定更加有利于引流管留置于可靠位置,有效避免脱管。术后再次皮肤消毒,覆盖无菌贴膜。接引流袋。⑤术中及术后半h均予心电监测,术后常规送胆汁细菌培养,密切观察患者症状体征改善情况。
|
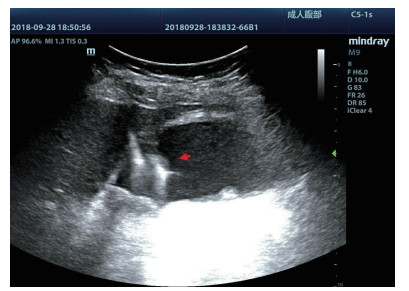
| 图 4 胆囊置管过程,导丝进入胆囊腔内(箭头处) |
|
|
术后再次经肘静脉超声造影同时经引流管超声造影:PTGBD后,再次经肘静脉快速团注SonoVuel 2 mL,在造影成像模式下进行观察肝脏被膜、胆囊床穿刺路径有无造影剂外渗,腹腔内有无外渗凝聚的造影剂,判断有无活动性出血及出血程度,如判断出血速度快、出血量较大,考虑动脉性出血,及时改为开腹或腔镜手术止血。PTGBD术后经引流管超声造影,置管成功后快速抽出胆囊内残留胆汁,减轻胆囊压力后,在超声造影模式下直接经引流管注入配制待用的稀释声诺维造影剂20 mL,实时动态的观察造影剂在胆囊腔内的充盈范围(图 2、3),评估引流管的通畅程度及引流范围、观察其在胆囊腔内的位置走形及卷曲情况、观察胆囊周边及腹腔内有无造影剂外渗。如患者腹痛症状加剧,结合经引流管超声造影判断有胆汁漏出表现,应持续监测观察患者生命体征及保守治疗效果,必要时及时改行开腹或腔镜手术治疗。
1.4 穿刺后治疗① 每日2次用生理盐水10 mL冲洗管道保持引流通畅。②禁食期间通过静脉补液,腹痛缓解后逐渐恢复饮食。③静脉输注广谱抗生素(三代头抱+甲硝哩)抗感染,根据胆汁细菌培养结果调整抗生素。④感染得以控制,复查超声胆囊无明显肿大,胆囊壁水肿消退,无盆腹腔积液时予带管出院。出院4周后再次返院评估患者全身状况、胆囊结石及胆囊炎症情况。若为无胆囊结石、无胆囊炎再发症状,先夹闭胆囊引流管,观察3 d,无胆囊肿大、胆囊炎再发,予拔除引流管; 对于有结石存在的胆囊炎患者若评估可接受手术,予行腹腔镜胆囊切除+引流管取出术; 若评估一般情况差,仍无法耐受麻醉及手术,则选择长期带管,问断予引流管冲洗。
1.5 观察指标① 穿刺时间:从消毒开始到固定穿刺管。②术后腹痛缓解时间,体温和白细胞(白细胞计数、中性粒细胞分类)降至正常时间,开始进食流质食物时间,术后住院时间(腹痛消失、体温正常、恢复半流食后可出院)。③并发症类型及发生率。
2 结果33例均顺利完成超声引导下PTGBD,其中术前静脉路超声造影诊断2例胆囊穿孔局限性胆汁性腹膜炎,先经腹腔穿刺抽吸胆囊周围积液,再经皮经肝穿刺胆囊。置管成功后,经静脉团注声诺维超声造影剂2.0 mL,其中1例注射造影剂注10 s后,于穿刺处的肝脏表面见高回声造影剂持续向肝外溢出,同时见肝肾间隙、右侧髂窝造影剂聚集且逐渐增多。遂于急诊行腹腔镜探查止血成功。其余32例无明显造影剂溢出或仅为极少量溢出且无动态增多趋势,评估为穿刺后无活动性出血。置管成功后快速抽出胆囊内残留胆汁,减轻胆囊压力后,在超声造影模式下直接经引流管注入配制待用的稀释声诺维造影剂20 mL,实时动态的观察造影剂在胆囊腔内的充盈范围,观察胆囊周边及腹腔内有无造影剂外渗,其中3例(9.1%)出现不同程度的造影剂外渗。均为自胆囊床处渗入肝肾间隙,同时伴随着患者腹痛症状加剧,立即予改变体位(头高脚底位,减轻膈肌刺激)及镇痛处理,其中1例渗出量较大者出现明显急腹症表现伴有血压降低,予行急诊剖腹探查+胆囊切除+腹腔冲洗术,术中见胆囊为系膜胆囊,腹腔内见褐色胆汁样积液,予行胆囊切除+腹腔冲洗术,术后生命征平稳,抗感染及腹腔引流后病情稳定出院。住院期问未发生胆囊引流管脱落事件。全部患者穿刺引流后继续给予抗感染等治疗,腹部症状明显好转,体温逐渐正常,血白细胞有明显下降趋势,其中102例患者胆囊炎症及全身情况逐渐好转后择期出院。除中转腹腔镜手术2例外,其余31例患者于PTGBD后4 h内疼痛均减轻,从术前(6.0±1.4)分,术后4 h降至(4.2±1.0)分,术后24 h为(3.1±0.9)分; 术后(33.0±3.6)h体温降至正常,(34.6±6.8)h白细胞计数正常,(38.4±3.3)h中性粒细胞百分比正常,术后(1.6±1.0)d恢复饮食,其中29例患者胆囊炎症及全身情况逐渐好转后于术后(6.8±1.3)d出院,2例患者住院期间临床死亡,死亡原因为肺部感染1例(3.0%)、心功能不全1例(3.0%)。所有病例未出现与穿刺有关的气胸、腹腔出血、胆道出血、胆漏、胃肠道损伤等并发症,穿刺抽取胆汁培养,23例(69.7%)胆汁细菌培养呈阳性,其中大肠埃希菌19例(82.6%),克雷伯菌属4例(17.4)。
31例患者病情好转后出院,具体序贯治疗方案及随访情况如下:3例(9.1%)非结石性胆囊炎,置管4周后试夹闭引流管3 d后无明显胆囊炎发作,予拔除引流管,未发生胆漏及胆汁性腹膜炎,随访期问无再发胆囊炎; 22例(66.7%)经评估可耐受手术治疗,于置管后4周至3个月择期行腹腔镜胆囊切除术,术中视野清晰,无明显炎症黏连表现,术后无严重并发症及死亡发生; 4例评估后仍无法耐受麻醉及手术,长期带管,间断于门诊行引流冲洗,随访期间未再发胆囊炎,其中1例(3.0%)长期带管患者随访期间死亡,死亡原因为心肺功能不全,全部病例无胆囊炎再发并加重导致死亡情况出现。
3 讨论高手术风险(高龄高危等因素)患者的急性胆囊炎是临床十分棘手的疾病。虽然腹腔镜胆囊切除术已成为目前急性胆囊炎的标准治疗方法之一,有较为可靠的安全性和有效性[8]。然而对某些高手术风险患者来说,由于合并脏器功能衰退,基础情况较差,往往不能耐受全身麻醉,即使是腹腔镜手术,仍存在较大的手术风险[9]。胆囊造瘘术曾经一度作为高手术风险的急性胆囊炎的治疗方式,操作相对简单,但同样有较高的麻醉风险,病死率也高达6%-20%[10]。对高危患者而言,经皮经肝胆囊穿刺置管术(PTGBD)不仅可以避免急诊胆囊切除手术的临床风险,同时能迅速对胆囊减压,缓解症状,通过同步全身抗感染治疗的配合,使急性胆囊炎得以治愈或为需要胆囊切除但暂无法耐受急诊手术的患者创造手术条件[11-12]。在便携式彩超机的辅助下,PTGBD操作具有很强的机动性,且仅需局部麻醉下进行操作,尤其适用于急诊抢救室和重症监护室的患者(有研究表明,重症监护室患者非结石性胆囊炎的发生率高达10%),床旁PTGBD术可降低高危患者的转运风险[13]。
超声造影是利用超声造影剂微泡(本组应用的是声诺维超声造影剂微泡)在低机械指数声波照射下发生共振,产生线性及非线性谐波回声信号,形成造影增强图像的技术,是近年来新兴的超声技术,具有实时、可连续观察、无辐射、可重复性好、毒不良反应少等优势,为临床提供了全新的诊疗手段[14]。经肘静脉注入的标准配置超声造影剂是一种血池造影剂,可以反映组织的血流灌注情况同时亦被广泛应用于肝、脾、肾等实质性脏器破裂的诊断,其诊断的敏感性及特异性均明显优于二维超声,且与增强CT有较好的一致性[15-16]。本组病例术前经肘静脉注入标准配置造影剂后,胆囊壁均显影增强,胆囊穿孔及周边积液处表现为造影无充盈区,穿刺置管后再次静脉路超声造影,迅速发现术后出血部位且可敏感评估是否为活动性出血(经手术证实)。除1例因活动性出血中转腹腔镜手术外,其余32例置管成功后经引流管口注入稀释造影剂20 mL(1:200稀释),评价引流管位置、引流范围及是否出现胆汁外漏取得良好效果,所有引流导管均能够清晰显示引流导管置入路径、引流管形态及引流范围,引流管置入恰当者,头端位于胆囊内,全管显影清晰,造影剂弥散区域与胆囊大小吻合; 置管后胆汁漏出者,可见造影剂沿引流管周边渗出[17-18],本组中3例出现造影剂外渗,其中两例渗出范围局限于胆囊床附近,未渗出至游离腹腔,患者腹痛症状稍有加剧,经胆囊减压及对症处理后好转,其中1例见造影剂渗出至肝肾间隙,患者腹痛症状加剧明显,考虑置管位置不当,余行急诊腹腔镜手术治疗,术中证实为系膜胆囊,且可见引流管侧孔部分外露。笔者的经验是,术前选择静脉路超声造影有助于对胆囊情况的评估及穿刺点的选择,术中正确选择穿刺针的入路有利于提高穿刺引流的成功率。首先是胆囊穿刺部位的选择应选择在靠近胆囊颈侧,此处胆囊位置比较固定,受体位影响较小,且胆囊床结缔组织较为固定,有助于将漏出胆汁包裹局限,其次是进针方向与胆囊床尽可能保持垂直,减少进针位置的偏移,同时置管成功后应即刻尽量抽尽胆囊内的感染性胆汁,生理盐水冲洗后行经引流管稀释超声造影有助于判断置管位置、引流范围及是否出现胆汁漏出,减少不必要的并发症发生率。穿刺引流后可以根据患者的营养状况待窦道形成稳定后择期拔除引流导管。对全身情况改善适合手术治疗且有手术意愿者可以考虑择期胆囊切除术。
| [1] | Okamoto K, Suzuki K, Takada T, et al. Tokyo Guidelines 2018 flowchart for the management of acute cholecystitis[J]. J Hepatobiliary Pancreat Sci, 2017, 25(1): 55-72. DOI:10.1002/jhbp.516 |
| [2] | Lee SO, Yim SK. Management of acute cholecystitis[J]. Korean J Gastroenterol, 2018, 71(5): 264. DOI:10.4166/kjg.2018.71.5.264 |
| [3] | 陈敏捷, 郑剑波. 经皮经肝胆囊穿刺序贯腔镜胆囊切除治疗老年急性重症胆囊炎效果比较[J]. 安徽医学, 2013, 34(6): 756-758. DOI:10.3969/j.issn.1000-0399.2013.06.031 |
| [4] | Miura F, Takada T, Strasberg SM, et al. TG13 flowchart for the management of acute cholangitis and cholecystitis[J]. J Hepato-biliary-pancreatic Sci, 2013, 20(1): 47-54. DOI:10.1007/s00534-012-0563-1 |
| [5] | Okamoto K, Takada T, Strasberg SM, et al. TG13 management bundles for acute cholangitis and cholecystitis[J]. J Hepato-biliary-pancreatic Sci, 2013, 20(1): 55-59. DOI:10.1007/s00534-012-0562-2 |
| [6] | Jia B, Liu K, Tan L, et al. Evaluation of the safety and efficacy of percutaneous transhepatic gallbladder drainage combined with laparoscopic cholecystectomy for treating acute complicated cholecystitis[J]. Am Surg, 2018, 84(1): 133-136. |
| [7] | 朱玉红, 高永雯. 彩色多普勒超声诊断胆囊穿孔的实用价值及误诊分析[J]. 实用医技杂志, 2018, 25(10): 1105-1106. DOI:10.19522/j.cnki.1671-5098.2018.10.018 |
| [8] | 王小军, 陈大伟, 费哲为, 等. 腹腔镜胆囊切除术治疗老年急性胆囊炎[J]. 中国微创外科杂志, 2013, 13(3): 236-239. DOI:10.3969/j.issn.1009-6604.2013.03.014 |
| [9] | Na BG, Yoo YS, Mun SP, et al. The safety and efficacy of percutaneous transhepatic gallbladder drainage in elderly patients with acute cholecystitis before laparoscopic cholecystectomy[J]. Ann Surg Treat Res, 2015, 89(2): 68-73. DOI:10.4174/astr.2015.89.2.68 |
| [10] | Huang CC, Lo HC, Tzeng YM, et al. Percutaneous transhepatic gall bladder drainage: a better initial therapeutic choice for patients with gall bladder perforation in the emergency Department[J]. Emerg Med J, 2007, 24(12): 836-840. DOI:10.1136/emj.2007.052175 |
| [11] | 雷道雄, 王凤飚, 刘森, 等. 经皮胆囊穿刺引流术治疗高危急性胆囊炎25例[J]. 中华普通外科杂志, 2014, 29(11): 839-842. DOI:10.3760/cma.j.issn.1007-631X.2014.11.007 |
| [12] | 陈健, 李立波, 胡红杰, 等. 经皮经肝胆囊穿刺引流术在高危急性胆囊炎患者中的应用[J]. 中华普通外科杂志, 2012, 27(3): 239-240. DOI:10.3760/cma.j.issn.1007-631X.2012.03.023 |
| [13] | 潘凡, 江艺, 张小进, 等. 床旁经皮经肝胆囊穿刺引流术在高龄急性化脓性胆囊炎患者中的应用价值[J]. 临床肝胆病杂志, 2012, 28(1): 21-22. |
| [14] | Piscaglia F, Nolsøe C, Dietrich C F, et al. EFSUMB and WFUMB guidelines and recommendations on the clinical practice of contrast enhanced ultrasound (CEUS). update 2011 on hepatic (EFSUMB and WFUMB) and non-hepatic applications (EFSUMB)[J]. Ultraschall Med, 2011, 33(01): 33-59. DOI:10.1055/s-0031-1297212 |
| [15] | 陈明, 陈红, 王康健, 等. 床旁常规超声及超声造影联合应用在腹膜后血肿中的诊断价值[J]. 中华急诊医学杂志, 2016, 25(4): 512-514. DOI:10.3760/cma.j.issn.1671-0282.2016.04.025 |
| [16] | 黄云健, 张生光, 李伟伟, 等. 二维超声和声学造影诊断1027例脾破裂及对治疗决策的影响[J]. 中华急诊医学杂志, 2013, 22(12): 1426-1429. DOI:10.3760/cma.j.issn.1671-0282.2013.12.031 |
| [17] | Ignee A, Jenssen C, Cui XW, et al. Intracavitary contrast-enhanced ultrasound in abscess drainage – feasibility and clinical value[J]. Scand J Gastroenterol, 2016, 51(1): 41-47. DOI:10.3109/00365521.2015.1066423 |
| [18] | Mao R, Xu EJ, Li K, et al. Usefulness of contrast-enhanced ultrasound in the diagnosis of biliary leakage following T-tube removal[J]. J Clin Ultrasound, 2010, 38(1): 38-40. DOI:10.1002/jcu.20622 |
 2019, Vol. 28
2019, Vol. 28




