中暑(heat stroke)作为一种严重威胁人类生命安全的危重症疾病,不仅可以表现为高热导致的严重的水电解质代谢紊乱以及中枢神经系统功能障碍,还可以并发多器官功能障碍(multiple organ dysfunction syndrome, MODS),甚至导致患者出现死亡[1-2]。研究表明因高热所导致的的血管内皮细胞的直接及间接损伤是引起全身炎症反应综合征(systemic inflammatory response syndrome, SIRS)以及MODS发生的主要原因[3-4]。
丙酮酸乙酯(ethyl pyruvate,EP)属于丙酮酸的简单衍生物,是能够清除活性氧的重要内源性代谢产物。研究证实丙酮酸乙酯可以改善急性胰腺炎、酒精性肝损伤、急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)、急性病毒性心肌炎、急性肾损伤、败血症等多种动物模型的全身性炎症反应和多器官功能障碍[5]。有研究证实丙酮酸乙酯可以抑制热打击所致的肝细胞中促炎因子的释放[6],但是丙酮酸乙酯是否能够影响热打击所致的血管内皮细胞的增殖活性尚不明确。本研究旨在通过丙酮酸乙酯进行干预来明确其对于热打击后血管内皮细胞增殖活性的影响。
1 材料与方法 1.1 实验材料人脐静脉内皮细胞(HUVECs)购自美国ScienCell Research Laboratories,无菌细胞培养皿及培养瓶均购于中国Nest Biotechnology公司,DMEM/F12培养基、胎牛血清均购自美国Gibco公司,胰酶、双抗购自于美国Invitrogen公司,丙酮酸乙酯(EP)购自美国Sigma-Aldrich公司,CCK-8检测试剂盒购于日本同仁公司。
1.2 细胞的复苏与培养将从液氮罐中取出的HUVECs放置在温度为37℃的恒温水浴锅中融化,然后转移至10 mL的离心管中,并加入5 mL的DMEM/F12细胞培养基,1 000 r/min的速率离心5 min,弃上清,加入含10%胎牛血清的DMEM/F12细胞培养基使细胞重悬,再将其转入培养瓶中,加入完全培养基(即含有10%胎牛血清,l00 U/mL的青霉素,l00 U/mL的链霉素)以防止细菌生长。最后将培养瓶置于37℃5% CO2及饱和湿度条件下继续培养,隔天换一次液, 每2~3 d可用0.25%的胰酶对其进行消化传代,传代可以按照1:3~1:5的比例进行,取对数生长期的细胞进行后续的实验。
1.3 HUVECs热打击模型的建立及分组将HUVECs按照上述方法传代并接种于无菌细胞培养皿中,将细胞密度控制在1×105/mL。实验分组:将HUVECs按照热打击设置的温度不同分为37℃对照组(CONT),39℃、41℃、43℃热打击组,其中43℃热打击组又按照不同的热打击时间分为2 h、3 h、4 h组。对照组始终放置在37 ℃的细胞培养箱中进行培养。通过将细胞培养箱内的温度设置至不同点(即37℃,39℃,41℃,43℃)来对各组细胞实施热打击,并实时监测培养箱内的温度及湿度,以保证在进行热打击的过程中细胞培养箱内温度分别稳定在(37±0.5)℃, (39±0.5)℃, (41±0.5) ℃及(43±0.5) ℃,箱内湿度始终>90%。
1.4 丙酮酸乙酯进行干预将丙酮酸乙酯用细胞培养液配置成终浓度为10 mmol/L的液体,然后在对各组细胞实施热打击之前将其细胞培养基更换成含有丙酮酸乙酯的细胞培养基,再接受不同条件的热打击,热打击完毕再进行后续的实验。
1.5 镜下观察细胞形态变化在实施不同条件的热打击之后,将细胞培养瓶放置在倒置显微镜下观察每组细胞的形态学变化并拍照(分别取100倍及200倍)。
1.6 CCK-8法检测细胞增殖活性取处于对数生长期的细胞,按照2×103个/孔的密度接种于可拆卸的96孔板中,培养6 h,待细胞贴壁后再将培养基更换为无血清的高糖DMEM培养基过夜,每孔约100 μL,然后更换为高糖DMEM完全培养基进行不同条件的热打击,每组分别设置4个复孔。热打击结束后,分别在各组细胞培养上清中加入10 μL的CCK-8溶液,然后将其置于温度为标准37℃、含5% CO2及饱和湿度的培养箱中继续孵育2 h,最后用酶联检测仪在450 nm处读取其OD值(A值)。计算细胞增殖率,细胞增殖率=(检测时相A值/前一个时相A值)x 100%。
1.7 统计学方法所有数据均采用SPSS 17.0软件(SPSS, USA)进行统计学分析。计量资料以均数±标准差(Mean±SD)表示。采用单因素方差分析对结果进行统计学比较。以P < 0.05为差异有统计学意义。
2 结果 2.1 热打击后细胞的形态变化根据预先设置的分组分别对HUVECs进行热打击之后,再在倒置显微镜下观察HUVECs的贴壁情况,结果如图 1及图 2所示。通过镜下观察发现,对于不同的热打击强度,或相同的热打击强度不同热打击时间,血管内皮细胞表现出的状态各异,其中对照组(37℃组)的细胞形态呈多形性,细胞饱满,贴壁情况及生长状态均显示良好,胞质胞核的结构清晰,然而随着热打击的温度不断升高或热打击的时间不断延长,镜下细胞形态发生变化,43℃持续热打击2 h时大部分细胞呈现肿胀状态,43℃持续热打击3 h或41℃持续热打击4 h时部分细胞逐渐变圆或呈长梭形改变,细胞形态不再饱满,胞质部分逐渐减少,失去原有的形状,而43℃持续热打击4 h后细胞形态变化最为明显,多数细胞周边伸出伪足,或只见被细胞膜包裹的细胞核,还有部分细胞脱壁,悬浮于细胞培养基中(如图 1及图 2所示)。

|
| 图 1 不同温度热打击后镜下HUVECs生长情况 Fig 1 HUVECs after heat stress in different temperature |
|
|

|
| 图 2 43℃不同时间热打击后HUVECs镜下生长情况 Fig 2 HUVECs after heat stress in 43℃ for different time |
|
|
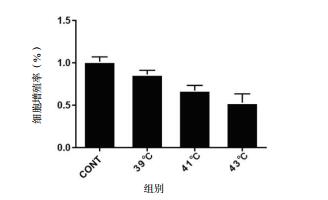
根据预先设定的分组,将HUVECs置于不同温度环境中(即39℃,41℃,43℃)分别实施热打击4 h,对照组则始终置于37℃细胞培养箱中培养,然后采用CCK-8法检测细胞的增殖活性,结果显示在相同的热打击时间前提下,随着热打击温度的不断升高,细胞的增殖活性逐渐降低,且与对照组(CONT)相比,43℃热打击4 h组细胞的增殖活性降低最为显著(如图 3所示),差异有统计学意义(F=108.2,P < 0.001)。
|
| 图 3 不同温度热打击4 h后细胞增殖情况 Fig 3 The proliferation of HUVECs after heat stress in different temperature |
|
|
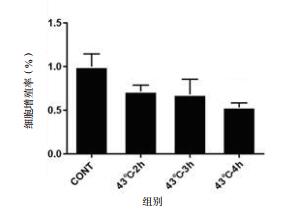
将HUVECs置于相同的热打击温度下(即43℃),实施不同时间的热打击(分别为2 h,3 h,4 h),同样将对照组置于37℃细胞培养箱中进行培养,然后用CCK-8法检测各组细胞的增殖活性,结果显示:在相同的热打击温度下,随着热打击时间的不断延长,细胞的增殖活性呈现逐渐下降的趋势,且与对照组(CONT)相比,43℃热打击4 h组细胞增殖活性下降最为明显(如图 4所示),差异有统计学意义(F= 25.79,P < 0.001)。
|
| 图 4 43℃热打击不同时间后细胞增殖情况 Fig 4 The proliferation of HUVECs after heat stress in 43℃ for different time |
|
|
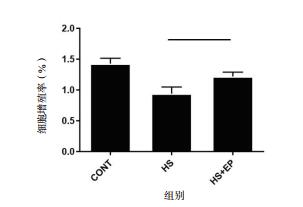
根据前两组实验的结果,最终选取43℃热打击4 h为最终干预点(heat stress, HS),用浓度为10 mmol/L的丙酮酸乙酯进行干预。然后采用CCK-8法来检测对照组(37℃即CONT组)、热打击组(43℃4 h即HS组)及EP干预组(HS+EP)的HUVECs细胞增殖活性,结果发现,与热打击组相比,EP干预组的血管内皮细胞的增殖活性明显增高(如图 5所示),且差异有统计学意义(F =44.77,P < 0.001)。
|
| 图 5 EP对热打击后细胞增殖活性的影响 Fig 5 Effects of heat stress on the proliferation of HUVECs after ethyl pyruvate pre-intervention. |
|
|
中暑意味着机体处于一种严重的病理状态,它的发生与机体遭受严重热打击后的内皮功能障碍密切相关,尤其是血管内皮和肠道内皮功能的障碍,到目前为止,已经有大量研究证实血管内皮细胞的损伤在整个中暑的发病过程中所发挥的关键作用[7-9]。
血管内皮细胞作为机体重要的内分泌及代谢器官之一,它既属于感知细胞,又属于效应细胞,它们不仅能感知血流变化所带来的切应力和压力的改变,血液中炎性信号及激素水平等相关参数的变化,而且还能针对以上信息参数的变化来通过分泌多种血管活性物质作出反应[10-11]。当机体遭遇热打击时,血管内皮细胞能够最先做出反应,因此它便成为了中暑发病过程中出现形态及功能变化最常见的细胞之一。研究证实血管内皮细胞在中暑发病过程中不仅受到的高热所致的直接刺激,同时还受到来自因全身炎症反应而被激活的大量炎症因子的间接刺激[12-13]。有研究者观察到热打击可以直接影响HUVECs的活性,及其对炎症因子IL-6及TNF-α的释放[14]。热打击还可以使HUVECs的细胞形态发生改变,抑制其增殖,以上效应均呈温度依赖性,且在复温过程中以上效应持续存在[15]。但从没探讨过丙酮酸乙酯这种具有广谱抗炎效应的药物对于热打击所带来的HUVECs这种增殖变化的影响。
本次研究通过对HUVECs实施不同温度相同时间的热打击及相同温度不同时间的热打击,在倒置显微镜下观察到了细胞的形态学变化,从最初的饱满,贴壁及生长状况良好,胞质胞核结构清晰,到部分细胞逐渐变圆脱壁或呈长梭形改变,细胞周围伸出伪足,胞质部分逐渐减少,甚至只剩下细胞膜包裹的细胞核,上述表现证实了热打击对于血管内皮细胞的直接毒性效应,这种毒性效应在设置的温度梯度范围内,当环境温度达到41℃时开始出现,到43℃时最为明显,而在设置的43℃热打击的时间梯度范围内,则是在热打击3 h的时候开始有所表现,4 h最为明显。此外本次实验还观察到热打击对于HUVECs增殖活性的影响也呈现出温度依赖性及时间依赖性,都是在43℃持续热打击4 h最为明显,因此选择了43℃热打击4 h作为干预点,用丙酮酸乙酯对其进行干预,结果发现丙酮酸乙酯可以明显减轻热打击带给HUVECs的增殖活性的影响。由此可见丙酮酸乙酯有助于缓解高热所造成的血管内皮细胞活性的改变。这为丙酮酸乙酯治疗中暑提供了一个新的依据。当然,对于丙酮酸乙酯是否可以影响高热所致的血管内皮细胞活化后所发挥的生物学效应,还有待进一步研究证实。
利益冲突 所有作者均声明不存在利益冲突。
| [1] | R L L A B. Heat Stroke[J]. Compr Physiol, 2015. DOI:10.1002/cphy.c140017 |
| [2] | Epstein Y, Yanovich R. Heat stroke[J]. N Engl J Med, 2019, 380(25): 2449-2459. DOI:10.1056/NEJMra1810762 |
| [3] | Leon L R. Heat stroke and cytokines[J]. 2007: 481-524. DOI: 10.1016/S0079-6123(06)62024-4. |
| [4] | Heled Y, Fleischmann C, Epstein Y. Cytokines and their role in hyperthermia and heat stroke[J]. J Basic Clin Physiol Pharmacol, 2013, 24(2): 85-96. DOI:10.1515/jbcpp-2012-0040 |
| [5] | Yang R, Zhu S, Tonnessen T Ⅰ. Ethyl pyruvate is a novel anti-inflammatory agent to treat multiple inflammatory organ injuries[J]. Inflammation, 2016, 13(1): 37. DOI:10.1186/s12950-016-0144-1 |
| [6] | Geng Y, Ma Q, Liu Y N, et al. Heatstroke induces liver injury via IL-1beta and HMGB1-induced pyroptosis[J]. J Hepatol, 2015, 63(3): 622-633. DOI:10.1016/j.jhep.2015.04.010 |
| [7] | 苏磊, 古正涛. 内皮细胞热损伤机制及其对重要脏器功能的影响[J]. 解放军医学杂志, 2017, 42(4): 271-278. DOI:10.11855/j.issn.0577-7402.2017.04.01 |
| [8] | Bouchama A, Hammami M M, Haq A, et al. Evidence for endothelial cell activation/injury in heatstroke[J]. CRITICAL CARE MEDICINE, 1996, 24(7): 1173-1178. DOI:10.1097/00003246-199607000-00018 |
| [9] | Roberts G T, Ghebeh H, Chishti M A, et al. Microvascular injury, thrombosis, inflammation, and apoptosis in the pathogenesis of heatstroke: a Study in baboon model[J]. Arterioscler Thromb Vasc Biol, 2008, 28: 1130-1136. DOI:10.1161/ATVBAHA.107.158709 |
| [10] | Sturtzel C. Endothelial cells[J]. Adv Exp Med Biol, 2017. DOI:10.1007/978-3-319-57613-8_4 |
| [11] | Onat D, Brillon D, Colombo P C, et al. Human Vascular endothelial cells: A model system for studying vascular inflammation in diabetes and atherosclerosis[J]. Curr Diab Rep, 2011, 3(11): 193-202. DOI:10.1007/s11892-011-0182-2 |
| [12] | ZT G, L L, F W. Heat stress induced apoptosis is triggered by transcription-independent p53, Ca2+ dyshomeostasis and the subsequent bax mitochondrial translocation[J]. Sci Rep, 2015, 5: 11497. DOI:10.1038/srep11497 |
| [13] | Tong H, Tong H, Wan P, et al. Vascular endothelial cell injury partly induced by mesenteric lymph in heat stroke[J]. Inflammation, 2014, 37(1): 27-34. DOI:10.1007/s10753-013-9708-x |
| [14] | 潘志国, 耿焱, 张剑明, 等. 热刺激对体外培养的血管内皮细胞损伤及IL-6、TNF-α释放的影响[J]. 山东医药, 2012, 52(3): 32-35. DOI:1002-266X(2012)03-0032-0 |
| [15] | 耿焱, 彭娜, 刘亚楠, 等. 热打击对培养人脐静脉内皮细胞增殖能力的影响[J]. 感染、炎症、修复, 2013, 14(1): 7-10. DOI:10.3969/j.issn.1672-8521.2013.01.002 |
 2020, Vol. 29
2020, Vol. 29




